Cuando se mezclan dos disoluciones que dan lugar a un compuesto iónico poco soluble en agua, éste precipita como sólido y queda alojado en el fondo del recipiente. Por ejemplo, al mezclar una disolución de de cloruro de cadmio con otra de sulfuro de potasio, precipitará sulfuro de cadmio debido a que su producto de solubilidad es muy pequeño:
| Sal muy soluble |
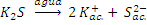 |
| Sal muy soluble |
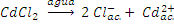 |
| Sal muy poco soluble |
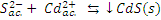 |
El equilibrio que se establece entre la fase sólida y la líquida lo podemos representar así:
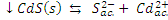
|
Ks= [S2-]·[Cd2+] = 4·10-29 a 20ºC |
|


