| |
|
Descarga |
 |
Cinética química
Unidad didáctica
Los principales objetivos son:
* El estudio de la velocidad de cambio hacia el equilibrio (velocidad de reacción) en la reacción química.
* La descripción de los factores que influyen en la velocidad de la reacción.
* Caracterización de la energía implicada en los procesos iniciales de la reacción química (energía de activación).
* Interpretación del comportamiento macroscópico del sistema en función de sus características microscópicas, expresadas como interacción entre moléculas.
Área: Química
Nivel: Bachillerato y Universidad
Autor: Enric Ripoll Mira
|
 |
 |
Tabla Periódica
Escena interactiva
Tabla periódica interactiva con información relativa a grupos, periodos y elementos.
.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Juan Guillermo Rivera Berrío |
 |
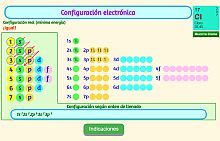 |
Configuración electrónica
Escena interactiva
Con esta escena interactiva e puede determinar la configuración electrónica de cualquier átomo en particular y se pueden "construir" las estructuras en el orden de los números atómicos siguiendo el principio del "Aufbau".
.
Área: Ciencias básicas - Química
Nivel: Bachillerato y Universidad
Autor: Juan Guillermo Rivera Berrío |
 |
 |
Elementos y compuestos
Unidad didáctica. Proyecto EDAD
Los objetivos de esta unidad son:
Identificar las propiedades características de los elementos químicos.
Clasificar los elementos.
Conocer cómo se unen los átomos para formar estructuras más complejas (moléculas, cristales...)
Identificar el nombre y las propiedades de algunos compuestos. Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Enric Ripoll Mira |
 |
 |
Los gases y la estructura de la materia
Unidad didáctica. Proyecto EDAD
Los objetivos de esta unidad son:
Distinguir los distintos estados de la materia.
Sus propiedades.
Concretar el modelo de gas que vamos a utilizar.
Utilizar la idea de presión ejercida por un gas y sus unidades.
Establecer la escala absoluta de temperaturas.
Llegar razonadamente a las leyes de los gases mediante varias experiencias utilizando el Método Científico.
Establecer la ecuación de estado del GAS IDEAL.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Pepa Grimá y Javier Soriano |
 |
 |
Termoquímica
Unidad didáctica. Proyecto Newton
La termodinámica es la parte de la ciencia que estudia los intercambios de energía asociados a los procesos físicos y a los químicos (reacciones). Una reacción puede liberar o absorber energía, y un cambio físico puede hacer lo mismo (por ejemplo, la fusión del hielo o la ebullición del agua). La termoquímica se centra en los intercambios de energía entre el sistema en estudio y su entorno. La termoquímica es útil para predecir la evolución de un sistema según la energía intercambiada en combinación con las determinaciones de la entropía, que también se utiliza para predecir si una reacción es espontánea o no espontánea
.Las reacciones endotérmicas absorben calor. Las reacciones exotérmicas liberan calor. La termoquímica funde los conceptos de la termodinámica con el concepto de energía en forma de enlaces químicos. Esto incluye el cálculo de magnitudes tales como la capacidad calorífica, el calor de la combustión, la entalpía, la entropía, la energía libre...
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Enric Ripoll Mira |
 |
 |
Reacciones químicas - 1
Unidad didáctica - Proyecto EDAD
Los objetivos de esta unidad son:
Reconocer los cambios químicos y diferenciarlos de los cambios físicos.
Conocer qué es una reacción química y sus componentes.
Conocer las características y leyes de las reacciones químicas: ley de conservación de la masa, energía y velocidad de reacción.
Saber ajustar reacciones químicas y escribir correctamente la notación de las mismas.
Interpretar el funcionamiento, a nivel microscópico, de las reacciones químicas.
Reconocer reacciones químicas que se producen continuamente en la naturaleza.
Saber interpretar el significado de las reacciones químicas.
Valorar la importancia del estudio de las reacciones químicas.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Jesú Manuel Muñoz Calle |
 |
 |
Reacciones químicas - 2.
Unidad didáctica. Proyecto EDAD
Los objetivos de esta unidad son:
Iniciarse en la estequiometría química.
Comprender y utilizar correctamente las magnitudes y leyes básicas necesarias para realizar cálculos en las reacciones químicas.
Conocer y comprender las relaciones entre las magnitudes químicas relacionadas con la estequiometría.
Deducir información a partir de una reacción química dada.
Realizar cálculos de masa y de volumen a partir de reacciones químicas.
Comprender el concepto de rendimiento de una reacción química.
Conocer distintas formas de clasificar las reacciones químicas.
Conocer algunas reacciones químicas de interés.
Valorar la importancia que tienen las reacciones químicas y por tanto la necesidad de su estudio y conocimiento. .
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Jesús Manuel Muñoz Calle |
 |
 |
Transformaciones químicas
Unidad didáctica. Proyecto EDAD
Los objetivos de esta unidad son:
Diferenciar los cambios químicos de los físicos.
Conocer las principales características de las reacciones químicas y su notación correcta.
Saber que existen diferentes tipos de reacciones y reconocer algunas de ellas.
Comprender y utilizar correctamente las magnitudes y leyes básicas necesarias para realizar cálculos en las reacciones químicas.
Conocer y comprender los conceptos básicos de la estequiometría.
Interpretar correctamente las relaciones cuantitativas que se establecen entre los reactivos y productos de una reacción.
Resolver correctamente los problemas relacionados con las relaciones cuantitativas de las reacciones.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Jesús Manuel Muñoz Calle |
 |
 |
Equilibrio químico
Unidad didáctica. Proyecto Newton
En el tema del equilibrio químico estudiaremos las reacciones reversibles y las condiciones que se tienen que cumplir para su establecimiento.
Cualquier sistema en equilibrio se encuentra en un estado dinámico en el cual dos o más procesos están ocurriendo a la vez y a la misma velocidad.
Los análisis químicos, las reacciones en la naturaleza y los principales procesos industriales de producción de sustancias son en su mayor parte reversibles, es decir, se desarrollan a la vez y en direcciones opuestas.
Así son, por ejemplo, la síntesis del amoníaco y del ácido sulfúrico, la solución saturada de carbonato de calcio y el equilibrio del ozono troposférico y estratosférico con el oxígeno diatómico.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Enric Ripoll Mira |
 |
 |
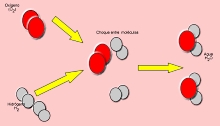
Reacciones de oxidación y reducción
Unidad didáctica - Proyecto Newton
Históricamente, el término de oxidación fue introducido por Lavoisier para explicar la combustión y, en general, todos los procesos en los que una sustancia se combina con el oxígeno. De forma independiente, se identificaban los procesos de reducción como aquellos en los que un óxido de metal se convertía en un metal con una disminución resultante en peso, de ahí probablemente su nombre.
Hay una serie de reacciones semejantes a la combustión que no se pueden explicar con la definición anterior. Con el tiempo se demostró que las reacciones de combustión, que se caracterizan por la energía desprendida en forma de calor y de luz, podían llevarse a cabo en presencia de elementos distintos al oxígeno, como la reacción del cloro con el sodio. Además, los metales pueden ser obtenidos a partir de otras sustancias distintas a la de sus óxidos (podemos obtener aluminio o potasio a partir de sus cloruros). También, cuando se pone el hierro en una solución de sulfato de cobre (II), se observa la precipitación de Cu metálico. Por tanto se hizo necesario el uso de una definición diferente a la usada por Lavoisier para englobar todas estas reacciones en un tipo común.
Hoy en día clasificamos como reacciones de oxidación y de reducción (redox) a todas las reacciones químicas en las que los átomos cambian su número (o estado) de oxidación.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Enric Ripoll Mira.
|
 |
 |
La química del carbono
Unidad didáctica - Proyecto EDAD
Los objetivos de esta unidad son:
Saber qué estudia la química orgánica o química del carbono.
Conocer el origen y una breve historia de esta parte de la química.
Reconocer la importancia de la química del carbono, tanto por número de compuestos, como por la utilidad de los mismos.
Conocer las principales características de las sustancias orgánicas.
Estudiar las características de los principales elementos que componen las sustancias orgánicas, especialmente del átomo de carbono.
Analizar la combinación y tipos de enlaces de los elementos en los compuestos orgánicos como grupos funcionales y cadenas hidrocarbonadas.
Iniciarse en la formulación y nomenclatura de los compuestos orgánicos.
Sentar las bases generales que permitan estudios posteriores de esta rama de la química.
.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Jesús Manuel Muñoz Calle |
 |
 |
Compuestos del carbono
Unidad didáctica - Proyecto EDAD
Los objetivos de esta unidad son:
Los hidrocarburos y su importancia como recursos energéticos. Reacciones de combustión.
Las reacciones de polimerización. Usos y aplicaciones de polímeros.
Macromoléculas: importancia en la constitución de los seres vivos.
Los efectos de la industria química: el problema del incremento del efecto invernadero, la lluvia ácida, vertidos. Causas y medidas para su prevención.
El papel de la química en la comprensión del origen y desarrollo de la vida.
Área: Ciencias básicas - Química
Nivel: Bachillerato, Ingeniería y Tecnología
Autor: Luis Ramírez Vicente |
 |