Introducción a la Química.
Margarita Patiño-Jaramillo
John Jairo García-Mora
Sonia Jaquelliny Moreno-Jiménez
Instituto Tecnológico Metropolitano, ITM
Línea Gestión del Conocimiento y Nuevas Tecnologías Aplicadas a la Educación
Grupo GNOMON
Título de la obra:
Introducción a la Química
Autores:
Margarita Patiño-Jaramillo
John Jairo García-Mora
Sonia Jaquelliny Moreno-Jiménez
Código JavaScript para el libro: Joel Espinosa Longi, IMATE, UNAM.
Recursos interactivos: DescartesJS
Fuentes: Lato y UbuntuMono
Diseño de cubierta: Margarita Patiño-Jaramillo
Fórmulas matemáticas: $\KaTeX$
Núcleo del libro interactivo: julio 2022
Fondo Editorial Pascual Bravo
Calle 73 73A-226
PBX: (574) 4480520
Apartado 6564
Medellín, Colombia
www.pascualbravo.edu.co
ISBN: 978-958-52963-5-0
Esta obra está bajo una licencia Creative Commons 4.0 internacional: Reconocimiento-No Comercial-Compartir Igual. Todos los objetos interactivos y los contenidos de esta obra colectiva están protegidos por la Ley de Propiedad Intelectual.
Este libro digital interactivo se ha diseñado con fundamento en la filosofía del Proyecto Descartes: con la intención de entregarlo a la comunidad académica de la aldea global, sin ánimo de lucro, solo con el objetivo de iniciar las competencias en química para estudiantes de bachillerato y universidad, esperando tan solo como retribución el uso y difusión de estos contenidos. El contenido del libro, al igual que los objetos interactivos se han diseñado de tal forma que se puedan leer en ordenadores y dispositivos móviles sin necesidad de instalar ningún programa o plugin. El libro se puede descargar para su uso en local sin dependencia con la red, a excepción de los ocho vídeos incluidos en el texto. Algunos de los objetos interactivos se han diseñado con el Editor DescartesJS.
La herramienta Descartes se caracteriza por una innata interactividad, por permitir realizar representaciones de objetos bi y tridimensionales, por gestionar expresiones de texto y de fórmulas, por integrar objetos multimedia como imágenes, audios y vídeos, por tener la posibilidad de reflejar casos concretos y también potenciar la conceptualización de tareas y procedimientos mediante la utilización de semillas aleatorias y controles numéricos, gráficos y de texto, y con ellos poder abordar la evaluación de manera automática, tanto la correctiva como la formativa. Con Descartes es posible el diseño y desarrollo de objetos educativos que promueven el aprendizaje significativo, posibilitando esa deseada construcción del conocimiento.Véase http://proyectodescartes.org/iCartesiLibri/descripcion.htm.
El libro se basa en documentos que han sido editados de manera altruista, semejante a la nuestra y, es el primero de una serie de textos en química, como son el volumen I y II de química bajo la filosofía del Proyecto Descartes, con el propósito de orientar a los iniciados en la materia de química, a nivel básica secundaria y primeros niveles de la universidad en el área de ciencias e ingeniería.
Esta primera parte de los textos de química, recrea los conceptos básicos de esta ciencia, para introducir a los estudiantes en el mundo científico, por lo que se presenta de manera sencilla cada una de las teorías, incluyendo las reacciones naturales de los seres humanos ante el enamoramiento, para así mostrar que la química es tan sencilla que todos la llevamos en nuestro sentir; es por ello, que se encuentran conceptos fundamentales desde la historia, una breve introducción al método científico, materia y sus propiedades, estados de agregación, se habla de medición cuando presentamos la medición cuantitativa de la materia, recreando luego la teoría atómica, inicios de la teoría cuántica y la sinigual tabla periódica, para dar una breve presentación de nomenclatura, para luego mostrar desde el laboratorio distintas prácticas cotidianas que permiten observar los distintos cambios que con el devenir diario, ni hemos notado, pero, estas prácticas de laboratorio nos permiten mostrar ciertos productos que utilizamos a diario, tanto para el aseo como en la estética.
Agradecimientos
Para esta producción, se ha requerido el apoyo de personas que con su sapiencia nos han apoyado y dirigido, como ha sido el maestro Juan Guillermo Rivera Berrío, Vicerrector académico de la Institución Universitaria Pascual Bravo, así mismo quienes han permitido utilizar sus imágenes, texto que a su vez se produjo sin ánimo de lucro como ha sido el Instituto Profesional providencia, miembro de la Ilumno, Sistema Universitario de las Américas, IPP, a la Señora Ángela López Berrocal, responsable de Proyectos y Oficina de Prensa del Foro Química y Sociedad en España, a mi compañero Jhon Jairo García quien me acompaña y apoya con los objetos interactivos y producción del texto.
Nota: se hace mención a PNGTREE, productores de imágenes en formato png, a quien se ha comprado la licencia para el uso de las imágenes que hacen honor a la tierra y en general al medio ambiente.
De los autores
Margarita Emilia Patiño-Jaramillo

John Jairo García-Mora

Sonia Jaquelliny Moreno-Jiménez

La química es una ciencia fundamental para el mundo que nos rodea, se encuentra en la naturaleza, y en toda la sociedad. Ella existe desde la antigüedad pero, a su vez, es una ciencia moderna con gran desarrollo en el siglo XXI.
Pero, aunque se le considera una ciencia ancestral, sus fundamentos modernos se instituyeron en el siglo XIX, cuando inician los avances en tecnología lo mismo que la presencia de estudiosos en el tema, quienes permitieron a los científicos separar las sustancias en los más pequeños componentes y, por consiguiente, explicar muchas de sus características físicas y químicas.
El rápido desarrollo de una tecnología cada vez más avanzada a lo largo del presente siglo nos ha dado más herramientas para estudiar lo que no puede verse a simple vista.
Utilizando computadoras y microscopios electrónicos, los químicos pueden analizar, por ejemplo la estructura de los átomos y de las moléculas (las unidades fundamentales en las que se basa el estudio de la química), así como diseñar nuevas sustancias con propiedades específicas, como medicamentos y productos que hagan más agradable el medio ambiente a los seres vivos, ya que esta permite dar respuesta a preguntas como ¿por qué se presentan algunos fenómenos como el fuego y la lluvia?, ¿cómo surge y se presenta la energía?, ¿por qué y cómo crecen las plantas?, ¿cómo se han formado las rocas?, ¿cómo se obtiene el plástico y el papel?, ¿por qué son tóxicas algunas sustancias?, ¿cómo se obtiene un ácido?, ¿porqué la combustión trasforma la materia en otra con propiedades completamente diferentes?
En general las preguntas que pueden surgir con base en los cambios que surgen en la naturaleza, en el laboratorio y en la cotidianidad, cuando los consumes, cuando fumas un cigarrillo, cuando lavas la ropa o cuando te bañas, cuando respiras y hasta cuando escribes en tu cuaderno.
Todo lo que tenemos a nuestro alrededor es química, no la podemos desligar de nuestra vida.

"Hay un libro abierto siempre para todos los ojos: la naturaleza". Jean Jacques Rousseau.

“Las ciencias están todas entrelazadas entre sí: es mucho más fácil aprenderlas todas a la vez que separar una de las otras”. René Descartes (1596-1650)


La alquimia, nombre que proviene del Árabe fue el albor de la actual química y era una práctica que trataba de consolidarse ciencia y disciplina filosófica que estudiaba elementos de la estructura de la naturaleza y sus proceso como la metalurgia, la física, la medicina, la astrología, la semiótica, el misticismo, el espiritualismo e incluso el arte.
Es indudable que desde la antigüedad ha existido la química, pero las primeras manifestaciones relacionadas con esta datan desde la época del fuego, cuando se da cuenta de trabajos prácticos como la cocción de los alimentos y la metalurgia, de lo que tenemos idea por los materiales usados y encontrados en los restos de las civilizaciones desaparecidas.
Los artículos normalmente encontrados son de metal, cerámica, vidrio, pigmentos y telas teñidas, así como la preparación de perfumes y cosméticos, práctica de la momificación y otros oficios análogos seguidos en las civilizaciones primitivas, lo que constituye los conocimientos sobre los que está basada la Química de hoy.
Antiguamente los metales más conocidos eran el oro, hacia el año 5000 a de C., por hallarse este metal libre en la naturaleza y por su color, su inalterabilidad y su rareza en la época, le ha permitido ser el metal precioso por excelencia, junto con otros metales y la plata.
Ellos fueron usados en las prácticas de la metalurgia, la que se practicó específicamente en civilizaciones como la de Mesopotamia y Egipto, aunque se desconocía su mecanismo.
En el siglo VI a. J.C., aparece en Grecia un poderoso movimiento intelectual y sus más grandes filósofos especularon sobre el mundo y la naturaleza de la materia, planteando claramente muchos de los problemas fundamentales de la Ciencia. La idea de la existencia o el origen de todo era algo tangible: para Tales de Mileto.
(aproximadamente 624-565 a. J.C.) fue el agua; para Anaxímenes (alrededor de 585-524 a. J.C.) era el aire, y para Heráclito de Éfeso (aproximadamente 540-475 a. J.C.) era el fuego. Más, tarde, Empédocles de Agrigento (alrededor de 500-430 a. J.C.) aceptó los elementos de sus antecesores, a los que agregó uno más, la tierra, sustituyendo así el principio único de la Escuela naturalista Jónica por los cuatro elementos: tierra agua, aire y fuego, que servían de alguna manera de soporte a las cualidades fundamentales de caliente y frío, y seco y húmedo, y dos fuerzas cósmicas, el amor y el odio, que son las raíces de todas las cosas.
Esta teoría de los cuatro elementos fue aceptada por Aristóteles de Estagira (384 - 322 antes de J.C.). En realidad, los cuatro elementos no eran más que la generalización y representación de una observación lógica, pues un cuerpo es sólido (tierra), líquido (agua) o gaseoso (aire), o bien se encuentra en estado de incandescencia (fuego).
Aristóteles fue el más influyente con los filósofos griegos, y sus ideas dominaron la filosofía natural durante casi dos milenios después de su muerte, en el 323 a.C., se creía que la materia poseía cuatro cualidades: calor, frío, humedad y sequedad.
Cada uno de los cuatro elementos estaba compuesto por pares de esas cualidades; por ejemplo, el fuego era caliente y seco, el agua fría y húmeda, el aire caliente y húmedo, y la tierra fría y seca, como se observa en la .
Esos elementos con sus cualidades se combinaban en diferentes proporciones para formar los componentes del planeta terrestre, y puesto que era posible cambiar las cantidades de cada cualidad en un elemento, se podía transformar un elemento en otro; así, se pensaba que era posible cambiar las sustancias materiales formadas por los elementos, por ejemplo, el plomo en oro.
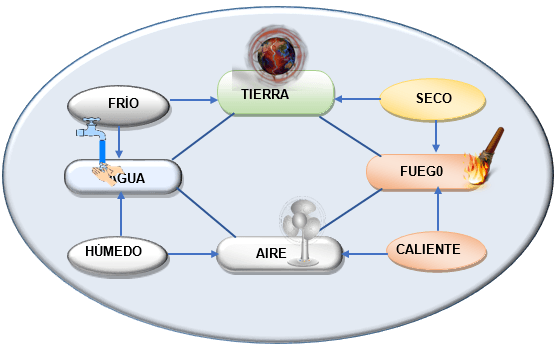
Por la misma época, Leucipo y su discípulo Demócrito de Abdera (460-370 a. J.C.), en oposición a Zenón de Elea, enseñaron la discontinuidad de la materia formada de átomos, el ser, y de vacío, el no ser, resultante de los intersticios entre aquellos, y permitiendo su movimiento. Los átomos son eternos, indivisibles (de donde deriva su nombre), y de la misma naturaleza, pero difieren en forma, por el orden en que están colocados en el cuerpo, por su posición relativa y por su magnitud.
A pesar de la tendencia positiva de las ideas de Demócrito, sus seguidores no desarrollaron su pensamiento que ofrece una estrecha relación con las teorías científicas modernas. Epicuro de Samos (342-270 a. J.C.), el más ilustre de ellos, creó la palabra átomo y le asignó un peso esencial.
El atomismo de Demócrito, expuesto en forma brillante en el inmortal poema De rerum Natura del romano Lucrecio, está construido totalmente por conceptos filosóficos, y no es hasta 1677 en que Boyle lo establece y Dalton en 1803 lo desarrolla como resultado de observaciones científicas.
La teoría de Aristóteles fue aceptada por los prácticos artesanos, especialmente en Alejandría, Egipto, que después del 300 a.C. se convirtió en el centro intelectual del mundo antiguo. Ellos pensaban que con los metales de la Tierra se podían realizar el mismo proceso más rápidamente en sus talleres, transmutando así de forma artificial los metales comunes en oro.
Comenzando el año 100 de la era cristiana, esta idea dominaba la mente de los filósofos y los trabajadores del metal, y se escribió un gran número de tratados sobre el arte de la transmutación que empezaba a conocerse como alquimia. Aunque nadie consiguió hacer oro, en la búsqueda de la perfección de los metales se descubrieron muchos procesos químicos.
Casi al mismo tiempo (y probablemente de forma independiente) apareció en China una alquimia similar. Los chinos consideraban al oro como una medicina que podía conferir larga vida o incluso la inmortalidad a cualquiera que la consumiera. Al igual que los egipcios, los chinos aumentaron sus conocimientos de la química práctica a partir de teorías incorrectas.
La alquimia y astrología se asociaron, relacionando el Sol con el oro, la Luna con la plata, Venus con el cobre, Mercurio con el mercurio, Marte con el hierro, Júpiter con el estaño y Saturno con el Plomo. (ver )

La obsesión de los alquimistas fue convertir el plomo en oro, mediante un reactivo llamado "piedra filosofal". El fracaso en esta aventura condujo a logros importantes en el conocimiento de la química de los metales y tintes. El estudio de la alquimia, nos guste o no, es antecedente de muchos procesos utilizados hoy en química, desde la metalurgia hasta la cosmética. Además no debemos de obviar que fue la primera disciplina en utilizar el método del ensayo y error, algo bastante cercano al método científico actual.
Las relaciones de la química con la medicina se conocen con el nombre de Iatroquímica. El máximo representante de esta tradición iatroquímica es Paracelso (1493-1541). Este médico y sus seguidores son los que otorgaron a la química un papel importante en la preparación de medicinas. La obtención de remedios curativos constituyó para Paracelso la finalidad de la alquimia, ya que asistir a un hombre enfermo era para él mucho más importante que dedicarse a fabricar oro y plata. Con ello introdujo un cambio importante en el enfoque de la alquimia, al apartarse de las metas clásicas de la misma. Esta nueva orientación influyó de modo considerable sobre el desarrollo posterior de la química.
Hacia (1604-68), un químico alemán, Johann Rudolf Glauber descubrió un método para preparar ácido clorhídrico por medio de la acción del ácido sulfúrico sobre la sal común. En el proceso obtuvo un residuo, el sulfato sódico, que actualmente se sigue llamando «sal de Glauber», continuó haciendo estudios y descubrió su propiedad laxante, así que la llamó “sal mirabile” (sal maravillosa) y la consideró como un cura todo, casi el elixir de la vida.
Al avanzar el siglo XVII la alquimia entró en decadencia, y en el XVIII se transformó en lo que hoy llamamos química.

Llegado el año 1564, se efectúan algunas mediciones especialmente relacionadas con la caída de los cuerpos, esta es la época de Galileo Galilei, (1590-99), tema que lo lleva a relacionar las matemáticas con la física, lo que indujo más adelante algo más o menos un siglo después a Isaac Newton a recopilar todos estos estudios en su libro “Principia Matemática”, destacándose especialmente las tres leyes de la dinámica y su teoría de la gravitación vigentes hoy día.
Años más tarde, en 1661, Robert Boyle publica (el químico escéptico o dudas y paradojas físico químicas) y sienta una de las bases de la química moderna . Y, para 1643, Evangelista Torricelli, logró probar, que el aire ejercía presión sobre los cuerpos, así entonces, demostró que el aire podía sostener una columna de mercurio de setenta centímetros de altura y con ello inventó el barómetro.

Conocido el barómetro, permite al alemán Otto von Guericke (1602-86) inventar la bomba de aire.
Continuando con los descubrimientos, en el año 1680 el físico Edme Mariotte (1630-1684), descubrió la ley de Boyle, la que relaciona el volumen y la presión de cierta cantidad de gas.
De todos modos, uno de los más dignos representantes de la química moderna ha sido Antoine Lavoisier, (1743- 1794) quien sentó su bases cuando estableció que la materia no se crea ni se destruye, ella se transforma, también demostró que el agua, el aire, el fuego no eran elementos: se interesó en estudiar la combustión, tema que en el siglo XVIII bastante controvertido, llegando así con gran éxito a mejorar las técnicas de alumbrado público en su época.
Así pues, Antoine Lavoisier fue el padre de la química moderna, fue el primero que dio cuenta de que el aire estaba formado por una composición de gases. ¿Te acuerdas? 78% de nitrógeno, 20, 9% de oxígeno, gases nobles, dióxido de carbono y vapor de agua. Pero sin duda por lo que más se le reconoce es por su famosa ley de conservación de la masa, según la cual la masa de un sistema no cambia cualquiera que sea la transformación que ocurra dentro de él.
Lavoisier escribió varios libros, entre ellos, Tratado elemental de química (1789), donde aclara el concepto de elemento como una sustancia simple que no se puede dividir mediante ningún método de análisis químico conocido. El señor Lavoisier es considerado el creador de la química moderna.
Biografía de Antonie Lavoisier

SIGLO XX: Esta es una época en la que se habla de la teoría de la relatividad en 1905, por Albert Einstein ( 1879 – 1955), los esposos Pierre y Marie Curie realizan estudios basados en la radiactividad, descubriendo con ello los elementos radiactivos el Polonio y el Radio, por la mitad del siglo XX los estudios se centran en los superconductores y fabricación de materiales plásticos, en 1996, se presenta el primer ser clonado.
Actualmente se conocen casi 19 millones de sustancias distintas, para el año 2050 podrían ser 300 millones.
 (Nació en Nueva Zelanda, 1871, muere en Londres, 1937) Físico y químico británico. Se trasladó a la Universidad de Cambridge (1895) para trabajar como ayudante de JJ.Thomson.Por sus trabajos en el campo de la física atómica está considerado como uno de esta disciplina.Investigo también sobre la ionización del aire producido por los rayos X, logró clasificarlas en rayos alfa, beta y gamma. Demostró (1908) que las partículas alfa son iones de hielo (mas exactamente, núcleos del átomo de hielo) y , en 1911, describió un nuevo modelo atómico (modelo atómico de Rutherford), que posteriormente seria perfeccionado por N.Bohr.) Premio Nobel de Química de 1908 en reconocimiento a sus investigaciones relativas a la desintegración de los elementos. (tomado de http://www.escolar.com/biografias/r/rutherford.html).
(Nació en Nueva Zelanda, 1871, muere en Londres, 1937) Físico y químico británico. Se trasladó a la Universidad de Cambridge (1895) para trabajar como ayudante de JJ.Thomson.Por sus trabajos en el campo de la física atómica está considerado como uno de esta disciplina.Investigo también sobre la ionización del aire producido por los rayos X, logró clasificarlas en rayos alfa, beta y gamma. Demostró (1908) que las partículas alfa son iones de hielo (mas exactamente, núcleos del átomo de hielo) y , en 1911, describió un nuevo modelo atómico (modelo atómico de Rutherford), que posteriormente seria perfeccionado por N.Bohr.) Premio Nobel de Química de 1908 en reconocimiento a sus investigaciones relativas a la desintegración de los elementos. (tomado de http://www.escolar.com/biografias/r/rutherford.html).
No cabe duda que una de las herramientas científicas para enfrentar el futuro es la ciencia química, con ella se enfrentarán los nuevos problemas del futuro, como son, la escasez de agua por lo tanto las fuentes de energía hídricas, el deterioro ambiental, y el surgimiento de nuevas enfermedades o infecciones, por lo que su relación con la física y la biología permitirán sintetizar nuevos medicamentos específicos para cada persona, de acuerdo a sus características genéticas particulares, lo más posible es que se permita una reprogramación genética para evitar malformaciones en los seres humanos e incluso el hombre, con todo ello, se lograrán cultivos más resistentes a las plagas y/o a la escasez de agua.
COPLAS: Historia de Química


"El agua es la fuerza que mueve a la naturaleza". Leonardo da Vinci.

“Comprender las cosas que nos rodean es la mejor preparación para comprender las cosas que hay más allá”. Hipatia,(aprox. 370-aprox. 415)


La Química es el estudio de la materia y los cambios que ocurren en ella (Raymond Chang).Por tanto es la ciencia que trata de la composición y propiedades de la materia (R. Petrucci)
La ciencia, la ingeniería en si la tecnología requiere del uso y las modificaciones de la química ya que la química y el lenguaje de los químicos desempeñan papeles vitales en biología, medicina, ciencia de materiales, medicina forense, ciencia ambiental y muchos otros campos. Así mismo, los inventos modernos nos proporcionan un mejor vivir, de ello, mencionamos que a principios del siglo veinte existían muy pocos automóviles y los teléfonos celulares apenas se desarrollaban, no existían fibras ópticas de hoy día, por ello y mucho más, la química desarrolló un papel importante en la transformación de la sociedad, ¿qué sería de nosotros sin la radio, la televisión, los aviones, las computadoras? Estos productos nos hacen la vida más segura, larga y placentera.
Las medicinas nos colaboran a ser más saludables y nos evitan enfermedades. Los fertilizantes y los controladores de plagas ayudan a incrementar los alimentos en cantidad y calidad.
Las transformaciones químicas ayudan a generar empleo y soportar la economía de los países. La industria química también desempeña un papel importante en la limpieza del medioambiente y a comprender nuestro mundo físico.
Todo lo que has tenido y tienes en la vida es química, es normal que si no lo sabes pienses que la química es solamente entrar a un laboratorio y preparar mezclas, realizar su análisis y hacer muchos más experimentos, pero, ¿sabías que 100% eres química?, pues tu cuerpo es todo química al estar compuesto por elementos que se encuentran en la naturaleza y que a diario escuchas hablar de ellos, si señores, tu cuerpo contiene carbono, C, hidrógeno, H, oxígeno, O, el calcio, C, que se encuentra en tus huesos, el fósforo P, el magnesio, Mg, el hierro, Fe, el potasio, K, el azufre, S.
Hasta cuando cupido, (ver ) el general del amor, hace que te sientas atraído(a) por alguien de sexo opuesto decimos que hay química, el enamoramiento desata ciertas reacciones emocionales hay energía, electricidad por las descargas neuronales, hay química porque las hormonas y otras sustancias que intervienen hacen que nuestra vida se descontrole por tan agradable pasión amorosa, las glándulas suprarrenales aumentan la producción de adrenalina y noradrenalina (neurotransmisores que comunican entre sí a las células nerviosas), haciéndose notar con el aumento de los latidos del corazón, se liberan grasas y azúcares que hacen que aumente la capacidad muscular, y mucha atención porque para los anémicos una de las más agradables medicinas, hace que aumente la producción de glóbulos rojos obteniendo así una mejor oxigenación del fluido sanguíneo.
Ustedes y la REACCIÓN QUÍMICA, si señores la pasión es una reacción química, existe una sustancia, conocida.
Hace más o menos cien años y que hace poco comenzaron los científicos a asociarla con ese gran sentimiento que usted siente por el otro, la feniletilamina (uno de los neurotransmisores más simples), es un compuesto natural semejante a la anfetamina y se presume que el cerebro la produce por eventos tan simples como una mirada o un apretón de manos.


Algunos científicos afirman que eso que llaman amor… amor… hace que el organismo por los millones de poros que posee, incluso con el aliento, manifieste la liberación de las feromonas El físico Enrico Fermi era famoso por su capacidad para estimar diversos tipos de datos con sorprendente precisión., existe la teoría que los seres humanos e incluso los animales envían mensajes de enamoramiento e incluso de peligro utilizando este medio, así que podríamos estar enviando mensajes de nuestra más oculta intimidad y deseos sexuales en forma inconsciente. Sin necesidad de que estés en un laboratorio preparando una reacción, tu organismo libera alrededor de 250 sustancias al estar frente a una persona que te resulta atractiva.
Recordando a Shakespeare, quien decía el amor es ciego” hay que ver la tonterías que somos capaces de hacer cuando estamos enamorados, Él tenía razón, diversos estudios sobre niveles de neurotransmisores en personas enamoradas muestran que el proverbio tiene razón: las personas enamoradas tienen menos serotonina, un neurotransmisor relacionado con las conductas compulsivas, pero además, sus niveles de atención, específicamente en circuitos relacionados con el pensamiento crítico, son menores. ¿Nos fijamos menos entonces en las cosas malas de nuestra pareja?
![]()
"Hay dos cosas que el hombre no puede ocultar: que está borracho y que está enamorado Antífanes -388- 311 a. C., comediógrafo griego"
![]()
Pero aquí no concluyen las reacciones químicas en el organismo, hay una segunda etapa en el enamoramiento y el amor romántico, en la que tiene que ver mucho la sustancia química llamada dopamina, la encargada de calmar, de adormecer los sentimientos, es decir, en esta fase los sentidos están adormecidos por la dopamina, en una especie de borrachera que produce euforia y no permite ver los defectos de la pareja.
Existen otras dos sustancias que llegan al cerebro para permitir que los sentimientos establecidos en la etapa del amor romántico se mantengan. Se trata de la oxitocina en las mujeres y la vasopresina en los hombres, sustancias que se mueven en el neocortex del cerebro y hacen que el amor se vuelva más racional, siendo ésta una tercera etapa del enamoramiento, la oxitocina corresponde a la misma hormona que segrega la madre cuando acaba de tener a su hijo, lo que explica que el amor durará toda la vida, y se produce tanto en un parto como en un orgasmo, pero ésta baja de nivel lo mismo que la vasopresina en los hombres, esto ocurre en el momento en que uno o el otro es descubierto en actos de infidelidad por su pareja, así digan lo que digan, el organismo es un gran complejo laboratorio de química.

![]()
“El amor es como Don Quijote: cuando recobra el juicio es para morir”. Jacinto Benavente
![]()
Iniciando el siglo XXI abundan las personas que se inclinan con pasión arraigada hacia lo natural, es hora de hacernos la pregunta: ¿por qué ese odio por la química?
No es justificable la huida que algunos emprenden cuando escuchan esta palabra, no se justifica puesto que hay elementos naturales que también hacen daño e intoxican igualmente que los obtenidos por el hombre, no debemos olvidar que la química está presente en cada segundo de nuestra vida desde que nos despertamos y volvemos a acostarnos estamos rodeados de química.
Los compuestos y procesos químicos llenan cada una de las escenas vividas durante el día, el agua que bebemos, con la que nos bañamos, el jabón que utilizamos para la limpieza , la crema dental, la que contiene fluoruro de sodio (NaF), también utilizado en Auxiliares de soldadura; Metalurgia; Industria de vidrio, fluorización del agua, el triclosán (2, 4, 4'-tricloro-2'-hidroxidifenil éter) también utilizado en la crema dental, es un potente antibacteriano utilizado además en productos hospitalarios (soluciones para lavado de manos quirúrgico, jabones para lavado de pacientes) y productos de consumo como los desodorantes. Y qué decir del cepillo utilizado para el aseo dental, conformado por fibras sintéticas con soporte de plástico, el cual es producto de un riguroso proceso químico.
Todos los productos utilizados en casa, son el resultado de aplicar diferentes técnicas químicas, las cremas que las señoras se ponen en la cara para su humectación, los geles para el cabello, las tinturas para el cabello, el cuero utilizado para la fabricación de los zapatos, el perfume que te hace lucir más agradable y sensual con su fino aroma,
la madera con que están diseñados los muebles de tu casa, y hasta las medicinas que te ayudan a mejorar las dolencias, son resultado del buen uso de los procesos químicos.
Cuando entras a la cocina aplicas técnicas químicas aún sin saberlo, cuando trasformas una solución ácida poniéndole azúcar (la sacarosa o azúcar común cuyo nombre científico es alfa-D-glucopiranosil (1, 2)-alfa-D-fructofuranósido, es un disacárido formado por una molécula de glucosa y otra de fructosa, la que se encuentra en la caña de azúcar y la remolacha.
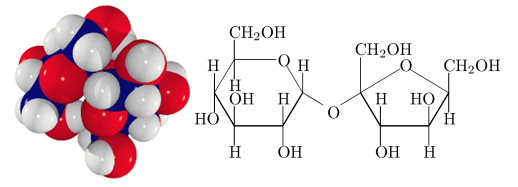
Cuando se calientan o cocinan los alimentos, mediante la conducción de calor utilizando algunas aleaciones de metales, utilizar el ácido acético, C2H4CO2, el que se compra en el supermercado como vinagre de frutas, el agua la sal, NaCl, o cloruro de sodio para dar sabor a los alimentos, carbohidratos, los que sirven como fuente de energía para todas las actividades celulares vitales, entre ellos encontramos los azúcares simples, se deben consumir con precaución, ya que de lo contrario se caería fácilmente en un exceso de energía que podría provocar aumento de peso: están también los carbohidratos de tipo complejo, son cadenas más largas de moléculas, debido a esto su sabor no es dulce ya que se no se digieren desde la boca, estos se encuentran en alimentos como pan, arroz, papa, pasta, tortillas y todos los derivados de los granos; los lípidos o grasas, conjuntamente con los carbohidratos representan la mayor fuente de energía para el organismo, estos son los que te hacen aumentar el nivel de triglicéridos y los encuentras en el aceite de cocina y las vitaminas.
Sorpréndete con las reacciones que ocurren en ese gran laboratorio que es tu organismo, como son, la glucólisis, que quiere decir "quiebre" o rompimiento (lisis) de la glucosa, lo que significa oxidación de la glucosa; también está la respiración.
Cuando deslizas tu lapicero por tu cuaderno, tu lápiz constituido de grafito, cuando miras a tu alrededor y vez las ventanas protegidas con vidrio, el hierro y su oxidación ante la intemperie, la madera que repudre, la basura que se quema, todas ellas son transformaciones que sufren estos materiales produciendo otras sustancias distintas a las originales, aquí ha ocurrido una reacción química.
Para que los alimentos lleguen a tu cocina con precios asequibles y de buena calidad solamente hay que recurrir al a química, hay que utilizar los fertilizantes, ellos están compuestos en muchos casos por nitrógeno, fósforo y potasio, boro cobre, magnesio, entre otros, los controles fitosanitarios, es decir las química moderna está protegiendo y permitiendo obtener mejores cosechas y los productos llegan al consumidor en mejores condiciones higiénicas.
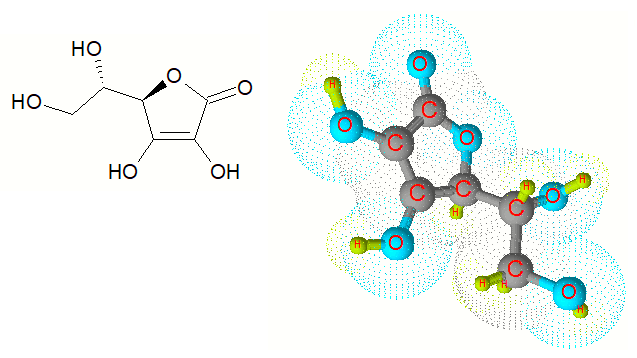
Los conservantes o aditivos que se utilizan para la protección de los alimentos ante la afección de los hogos y bacterias que deterioran la salud del hombre, igualmente los antioxidantes como la vitamina C (ácido ascórbico) y la vitamina E y sus derivados impiden el arranciamiento de las grasas; los agentes de texturas o aditivos como los antiglomerantes, como la harina, la gelatina, la clara de huevo que dan consistencia a varios platos, los polifosfatos utilizados en las charcuterías por su propiedad de retener el agua de cocción impide que las carnes tengan un aspecto fibroso, los espesantes y los emulsionantes los que permiten que se unan las grasas al agua, lo que es absolutamente necesario para la fabricación de algunas salsas, helados y chocolates.
No se puede dejar atrás el envase que se utiliza para los alimentos, gaseosas y otras sustancias de gran importancia cotidiana, ellos son admirables piezas tecnológicas, ellos deben ser permeables gases como el anhídrido carbónico o el oxígeno, deben evitar el pasote la luz y los aromas, ello solamente se consigue con la ciencia química.
Con la química tendrás más vida, en la época del imperio Romano el índice de vida era tan sólo de 25 años y en el siglo XIX había aumentado a 35años, ahora encontramos personas hasta de10 o más años, lo que significa que a lo largo de la historia el hombre ha luchado insistentemente por sobrevivir y mejorar su calidad de vida, siendo los grandes descubrimientos y científicos de los siglos XVIII y XIX quienes fundamentaron las bases de lo que habría de ser la ciencia que diera respuesta a las necesidades del hombre: LA QUÍMICA.
La química nos permite tener a nuestro alcance la salud, nos proporciona los medicamentos, las vacunas los antibióticos; el agua que ha sido considerada como fuente de vida y también de enfermedades, gracias a la química el agua se hizo milagrosamente potable gracias a la presencia del cloro; en las clínicas se utilizan gran cantidad de desinfectantes, antisépticos, diversas medicinas y antibióticos que han revolucionado la medicina, que tal cuando vas al odontólogo si no hubiera anestesia, parece increíble, pero si todo es química, no importa a dónde se mire, todo nuestro alrededor está lleno de química, está en los muebles en la pintura de las paredes, en las telas de los vestidos, en los zapatos, en el equipo de sonido, en el televisor, en la computadora, en la calculadora, en el televisor, en los CD, en las bombillas, en todo lo que hay presente en casa está presente la química, sin olvidar que tu cuerpo está constituido por átomos y moléculas.
La química nos permite preguntar espejito espejito…, nos proporciona artículos de higiene, aseo y belleza, nos proporciona el traje para cada ocasión, los bomberos dispones de trajes ignífugos, los policías de chalecos antibalas, los motociclistas cuentan con trajes impermeables.
Porque existe la química podemos contar con tintes para darle color a la ropa, unos 23000 colores diferentes, existen los elastómeros, es decir, polímeros que muestran comportamiento elástico, con la existencia de la química se cuenta con zapatos más anatómicos, los que se fabrican con poliuretano, poliamida y siliconas que proporcionan una mayor flexibilidad, menor peso, mayor agarre y absorción a impactos.
Gracias a la química materiales como la madera que han estado por miles de años expuestos a los hongos y bacterias ha podido ser remplazados por los plásticos, ahora el hombre dispone de raquetas más livianas para el juego de tenis, cremas, gafas, palos de golf más livianos, accesorios en general para todo tipo de deporte.
¿Qué decir del transporte?, gracias a la química los automóviles cuentan con autopartes más livianas, permitiendo crear autos más ligeros, eficientes, duraderos, ecológicos, silenciosos y cómodos, seguros con la creación de los airbag, los cinturones de seguridad y los líquidos para frenos.
Gracias a la química los automóviles cuentan con autopartes más livianas, permitiendo crear autos más ligeros, eficientes, duraderos, ecológicos, silenciosos y cómodos, seguros con la creación de los airbag, los cinturones de seguridad y los líquidos para frenos.
¿Por qué pudo llegar el hombre a la luna?, gracias a la química, con ella se pudo crear el combustible y trajes espaciales, los materiales resistentes con recubrimientos cerámicos que permitieron la creación de los transbordadores espaciales.
La química también previene el medio ambiente: es importante conocer que un automóvil actual genera la décima parte de la contaminación de la que generaba uno hace unos 50 años, pues la química ha permitido crear materiales más ligeros y combustibles con aditivos que generan día a día menos contaminación.
Sin la química no existiría la computadora, de productos químicos están constituidas todas sus partes, los ships que las conforman están elaborados de silicio o arseniuro de galio, los soportes magnéticos, los DVD, los CD, están fabricados con material plástico como policarbonato, la carcasa, el teclado, los cables, el ratón están hechos con material polimérico. Las carcasas de estos aparatos de comunicación, las pantallas de cristal líquido, los circuitos, los chips, los teléfonos celulares y sus baterías hacen parte de la investigación en química.

En un futuro no muy lejano, el avance en los estudios de la química proporcionará lo inimaginable, se proporcionarán nuevos materiales, nuevas medicinas que permitirán curar la enfermedad que hoy es incurable, la nanotecnología y la química supramolecular son hoy día las protagonistas de la ciencia.Con el estudio de esta ciencia podrás predecir y entender lo impredecible de la naturaleza y tendrás la explicación de todo un mundo en fundamentos sólidos, conocimientos científicos y estudios de investigación, todo por medio de una gran ciencia, denominada simplemente química.
Los avances tecnológicos y las facilidades que aportan los nuevos aparatos electrónicos aportan, cada vez más, nuevas vías de progreso en la industria química, aunque también es cierto que, por el momento, no desbancan a los materiales básicos que un laboratorio químico debe tener en sus mesas y armarios. Sofisticados medidores digitales y balanzas de precisión conviven con probetas de vidrio y pipetas, imprescindibles para manipular los elementos.(Robles, 2010)
En cuanto a evolución tecnológica los espectrofotómetros, colorímetros, balanzas, centrífugas, baños, agitadores y, por supuesto, microscopios son algunos de los aparatos más utilizados en un laboratorio y que la tecnología ha permitido avanzar hasta conseguir que las mediciones, pesados y calibraciones sean precisas y procesables en ordenadores que calculan las variaciones y errores de cálculo invisibles al ojo humano. El microscopio es uno de los elementos de laboratorio que más ha evolucionado, mejorando la capacidad de aumentos y contrastes (García, 2018).
![]()
"La química, a diferencia de otras ciencias, surgió originalmente de delirios y supersticiones, y en su comienzo fue a la par con la magia y la astrología." Thomas Thomson
![]()

"El agua es crítica para el desarrollo sostenible, incluyendo la integridad del medio ambiente y el alivio de la pobreza y el hambre, y es indispensable para la salud y bienestar humanos". Naciones Unidas.

"La química, a diferencia de otras ciencias, surgió originalmente de delirios y supersticiones, y en su comienzo fue a la par con la magia y la astrología." Thomas Thomson


La química parte de la ciencia que estudia la composición, estructura, propiedades y transformaciones de la materia, de su interpretación teórica, de cambios energéticos que tienen lugar en trasformaciones y efectos producidos en las mismas , así mismo añadir o extraer energía de las mismas.
En la naturaleza y en la vida misma todo está sujeto a cambios, lo mismo que al interior del organismo de los seres vivos y ello es ocasionado por la química, todo lo que hay a nuestro alrededor es química, entonces ¿qué es química?
 La química es una ciencia experimental que se ocupa de la composición de las sustancias y los cambios que sufren, desde los siguientes puntos de vista:
La química es una ciencia experimental que se ocupa de la composición de las sustancias y los cambios que sufren, desde los siguientes puntos de vista:
Al ser la química la ciencia que trata de la constitución de la materia, no hay ninguna rama de la ciencia que posea una extensión tan amplia e incluso, un examen cuidadoso del contenido de todas ellas revela que la química tiene una relación estrecha con cualquier ciencia particular.Así, la Biología incluye el estudio de las transformaciones químicas que ocurren en las minúsculas células integrantes del organismo vivo durante los procesos de digestión y crecimiento;la geología constituye un prodigioso lienzo natural en el que se muestran los cambios químicos verificados en las rocas durante las diversas eras geológicas; la Física se ocupa de las distintas formas de energía, pero los efectos de la energía sobre la materia son casi siempre de naturaleza química; y la astronomía se apoya en la Química al buscar información acerca de la estructura y constitución de los astros.
Como toda ciencia, la ciencia química puede dividirse en distintos campos como se observa en al
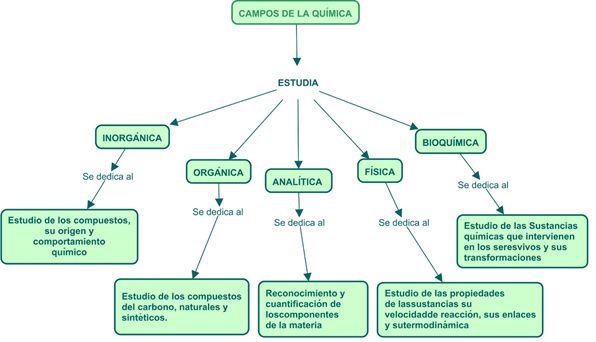
También puede encontrarse como:
Estudia los conceptos fundamentales de la estructura, de la materia, leyes, principios teorías y las reglas de escritura y nomenclatura.
Es una rama de la química que estudia las características, propiedades y composición de las sustancias, así como las reacciones de estas con otras y sus formas de obtención. Se encarga del estudio de los metales alcalinos, los metales alcalinotérreos, los elementos térreos, los elementos carbonoideos, los elementos nitrogenoideos, los elementos anfígenos y los elementos halógenos y estudia algunos compuestos concretos como el amoníaco, los óxidos de nitrógeno, el ácido nítrico, los óxidos de azufre y el ácido sulfúrico. Esta parte de la química se divide a su vez en dos ramas: la química inorgánica y la orgánica.
Estudia y utiliza instrumentos y métodos para separar, identificar y cuantificar la materia, se aplica en la industria, la medicina entre otras ciencias su finalidad es el estudio de la composición química de un material determinando los componentes de la muestra. Se divide en cualitativa y cuantitativa.
Es la disciplina que apoyada en procesos de química pura soluciona problemas prácticos.
Al ser la química una ciencia, significa que no se va a consistir en una mera acumulación de datos observados sobre las características o sobre las transformaciones de la materia.
En sus primeros tiempos lo que se llamaba química no era, efectivamente, más que eso: desde los egipcios, pasando por las distintas civilizaciones antiguas y por los estudios de los alquimistas, se fueron conociendo multitud de fenómenos sobre el comportamiento de la materia. Sin embargo, no podía concedérsele a la Química el calificativo de ciencia, ya que no existía una justificación teórica para estos fenómenos. Por otra parte, los griegos trataron sobre la naturaleza de la materia, pero de una manera más bien filosófica, alejada de los hechos experimentales.
La Química se hace ciencia cuando el hombre se dedica al estudio del fenómeno químico y es capaz de dar esa justificación teórica al hecho observado. Es decir, cuando se unen hecho experimental y teoría. Esto no ocurrirá plenamente hasta el siglo XIX, cuando se conectan las propiedades y comportamientos de la materia con su estructura a nivel microscópico., aunque también efectúan observaciones nivel macroscópico, y submicroscópico.
Así entonces el estudio de la química es el estudio de la vida. A medida que avance en el estudio de esta ciencia aprenderá acerca de las estructuras e interacciones fundamentales de las cosas que cree conocer, el agua, el aire que respira, los alimentos que consume. Por lo tanto, conocerá su composición interna y sus reacciones con otros compuestos o elementos de la naturaleza.
El método científico es la combinación de las observaciones y experimentos junto con la formulación de leyes, hipótesis y teorías.
El método científico se ilustra mediante el diagrama de la . A veces los científicos desarrollan un patrón de pensamiento en su campo del saber, conocido como un paradigma, cuyo éxito es grande al principio, pero después no lo es tanto. Puede ser necesario un nuevo paradigma. De alguna manera, el método de búsqueda que denominamos método científico es también un paradigma, y hay quien piensa que también necesita ser cambiado. Es decir, las distintas actividades de los científicos modernos son más complejas que la simple descripción del método científico aquí descrito. En cualquier caso, el éxito científico no está garantizado si simplemente se siguen una serie de procedimientos semejantes a los de un libro de cocina.
En sus comienzos, este proceso consiste en la simple observación de los fenómenos, tal como ocurren en la Naturaleza, y en describirlos lo más exactamente posible. Después, al multiplicarse las observaciones, se encuentran en grupos de ellas ciertas regularidades que pueden formularse como leyes. Cada ley científica o ley natural se refiere a un gran número de hechos resumidos de modo abreviado y que puede generalizarse a otros fenómenos análogos. En general, las leyes pueden expresarse en forma matemática. Las leyes no constituyen una explicación de la Naturaleza sino, tan sólo, una descripción.
Según, como opera la ciencia, el método científico conlleva entre otras las siguientes etapas:

En realidad, es este último aspecto el que constituye la verdadera función de la especulación teórica al dar lugar, fundamentalmente, al avance continuo en nuestro conocimiento del mundo físico y al control del mismo para nuestro beneficio.

La química, igual que las otras ciencias utiliza términos muy específicos, que a su vez es necesario tenerlos muy claros.
La materia es todo aquello que ocupa un lugar en el espacio, tiene cuerpo y no puede alterar su estado de reposo o movimiento por sí solo, esto es lo que llamamos inercia.
Por ejemplo, el agua, la madera, el hierro, el papel, etcétera.
La materia está conformada por átomos, o por la unión de átomos que reciben el nombre de moléculas.
Un átomo es la partícula más pequeña de un elemento que conserva las propiedades características de dicho elemento, y siendo tan pequeña es posible su división.
Las substancias que pueden descomponerse por medios químicos apropiados en Todo lo que hay a nuestro alrededor está formado por grupos de átomos unidos que forman conjuntos llamados moléculas. Los átomos que se encuentra en una molécula se mantienen unidos debido a que comparten o intercambian electrones.
Las moléculas están hechas de átomos de uno o más elementos. Algunas moléculas están hechas de un sólo tipo de átomo. Por ejemplo, dos átomos de oxígeno se unen para formar una molécula de O2, la parte del aire que necesitamos para respirar y vivir. Otras moléculas son muy grandes y complejas. Por ejemplo, las moléculas de proteína contienen cientos de átomos.
El 23 de junio de 2015 el registro de sustancias del Chemical Abstract Service ha llegado a los cien millones. La velocidad a la que se generan nuevas sustancias es de varios miles al día, una cantidad ingenteInvestigación y Ciencia. Edición española de Scientific American. En: https://www.investigacionyciencia.es/blogs/fisica-y-quimica/24/posts/son-cien-millones-13300.
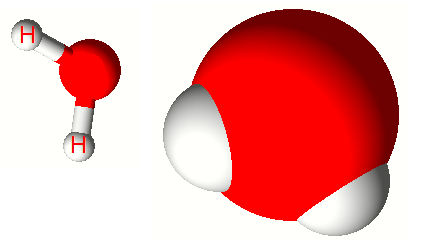
Cuando los elementos entran a formar parte de un compuesto, sus propiedades originales, como el color, su dureza y punto de fusión son remplazadas por las propiedades características del compuesto. Considere la sal común (sal de cocina), el cloruro de sodio, NaCl, está formada por dos elementos, el cloro y el sodio.
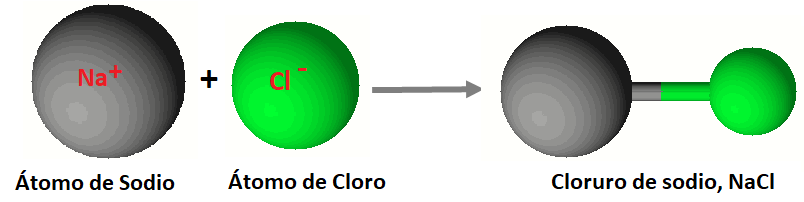
El sodio es un metal brillante que interacciona en forma violenta con el agua. Está formado por átomos de sodio fuertemente unidos.
El cloro es un gas amarillo claro, de olor fuerte y sofocante, es irritante para los tejidos humanos. El elemento está formado por dos moléculas de cloro, Cl2 enlazadas fuertemente.
El cloruro de sodio o sal común es un sólido cristalino con propiedades completamente distintas a los dos elementos que lo constituyen. Dos o más sustancias elementales se denominan compuestos.
Una sustancia es toda porción de materia que comparte determinadas propiedades intensivas.
Es aquella sustancia pura que está formada por átomos de un mismo elemento.
Se denomina Sustancia Pura a todo aquel sistema homogéneo formado por uno o varios componentes, también con un aspecto homogéneo; si esta sustancia está conformada por un solo componente corresponde a un elemento químico, como el oro, la plata, el magnesio, el cloro, el mercurio, el oxígeno, el calcio, entre otros y si está conformada por dos o más componentes será un compuesto químico, como lo es el ácido acético, el etilenglicol, el alcohol, el agua, enter otros.
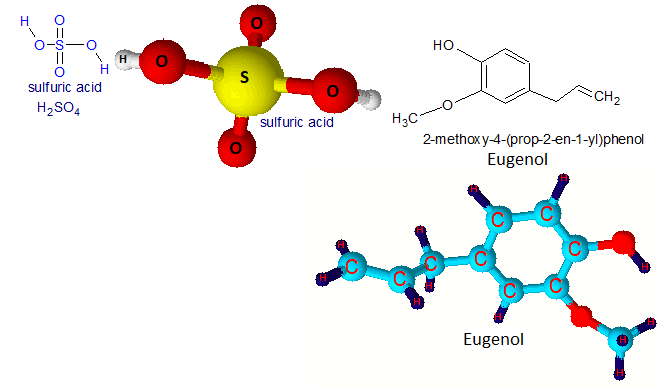
Es aquella sustancia pura en cuya composición encontramos varias clases de átomos en una proporción constante, por ejemplo: el azúcar, la sal de cocina (cloruro de sodio), el vinagre o ácido acético), el ácido sulfúrico, el aceite de clavo o eugenol, el agua,5 etc. como se muestra en la .
En 1847, el químico alemán Hermann Kolbe sintetizó el ácido acético por primera vez a partir de elementos inorgánicos. Secuencia de reacciones: a) cloración de disulfuro de carbono para obtener tetracloruro de carbono, b) pirólisis produciendo tetracloroetileno, c) cloración en disolución acuosa para dar ácido tricloroacético, d) reducción electrolítica a ácido acético. El ácido acético, también conocido como ácido metilcarboxílico o ácido etanoico, es un compuesto químico orgánico, ya que tiene un átomo de carbono en su formula química. (Crédito: https://acidoacetico.info/) - El ácido sulfúrico (H2SO4) o sulfato de hidrógeno, es un líquido incoloro, viscoso y un ácido inorgánico fuerte. Es altamente corrosivo y en contacto con la piel puede ocasionar quemaduras de alto grado (Crédito: https://www.acidosulfurico.org/).
Es toda aquella sustancia que no se puede descomponer en otras más simples mediante procesos químicos. Ejemplos de elementos son: cobre, oro, sodio, hidrógeno, oxígeno, nitrógeno, el flúor, el oro, el yodo, la plata, el sodio, el carbono, el mercurio, etc.
Para representar a los elementos se emplea un conjunto de símbolos químicos que son combinaciones de letras. La primera letra del símbolo químico es siempre mayúscula acompañada por una segunda y hasta una tercera, que son siempre minúsculas.
Los símbolos de algunos elementos provienen de su nombre en latín, por ejemplo, el elemento sodio se simboliza Na (natrium), el hierro, Fe (ferrum), otros están relacionados con una zona geográfica, el galio (Ga) y el germanio (Ge), uno sólo, el del tungsteno, W, proviene de la palabra en alemán wolfram.
Los elementos con número mayor de 92, llamados transuránicos, son producidos por aceleradores de partículas, por ejemplo, ciclotrones y tradicionalmente el grupo que produce el elemento por primera vez le asigna el nombre, a estos elementos se les encuentra con cada una de sus propiedades en la tabla periódica.
Al descubrirse los elementos 104 y 105 surgió un problema, ya que para el elemento 105 un grupo de Berkeley, California, propuso el nombre Rutherforio y otro grupo de Dubna, Rusia, propuso el nombre Kurchatovio, la Unión Internacional de Química Pura y Aplicada (IUPAC) decidió entonces recomendar que los elementos nuevos que se descubrieran llevarán los nombres correspondientes a su número atómico hasta que se estableciera fehacientemente la prioridad de su descubrimiento.
Los símbolos de estos elementos se forman de acuerdo a su número atómico y consisten en tres letras, cada una de las cuales es la primera de las siguientes raíces:
Algunos elementos químicos se listan a continuación, con su respectivo símbolo, en la :
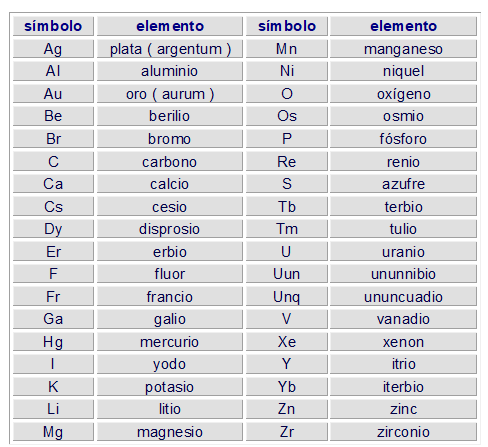
De los 118 elementos actualmente conocidos, 21 han sido producidos artificialmente en estos últimos años y no se han encontrado en la naturaleza. De los 92 elementos naturales restantes, muchos se hallan en proporción tan pequeña que parece existen tan sólo por excepción.
Unos pocos elementos, como el oxígeno, el nitrógeno, el carbono, el oro, la plata y el platino, entre pocos más, se encuentran en estado libre o sin combinar; los otros existen combinados. Muchos de los elementos como el hierro, oro, cobre, plata, mercurio, plomo, aluminio, níquel, estaño, azufre, oxígeno, nitrógeno, hidrógeno, carbono, cinc, helio, radio y uranio nos son familiares, pero esta familiaridad no quiere decir que sean los más abundantes.
Existe un elemento que por su abundancia en la corteza terrestre ocupa el segundo lugar, después del oxígeno y continuamente estamos en contacto con muchos de sus compuestos. Este elemento es el silicio, básico en la industria electrónica, el cual forma parte de la arena, vidrio, cemento, arcilla, carborundo, asbesto, mica y demás silicatos. Un 47% aproximadamente de la arena del desierto está constituida por silicio.
La materia se caracteriza por sus propiedades y su composición, las propiedades de la materia se clasifican en dos grandes categorías, propiedades físicas y Propiedades químicas.
Son aquellas propiedades en las que no cambia la composición de la sustancia, ellas son el color, el olor, el sabor, la solubilidad, la densidad, el punto de fusión, el punto de ebullición, la viscosidad, índice de refracción, brillo, conductividad del calor y de la electricidad, transparencia, dureza, maleabilidad, ductilidad. Los valores numéricos de estas propiedades, depende de la presión y de la temperatura.
Así por ejemplo, el oro y su color amarillo, el cobre y su color rojizo, así como se observa en la

Las propiedades físicas como el sabor, olor, color, son detectadas por los sentidos, por lo tanto, reciben el nombre de propiedades organolépticas, por que se perciben con los órganos de los sentidos.
Todas las propiedades físicas de la materia pertenecen a dos categorías: las propiedades extensivas y las propiedades intensivas.
Estas dependen de la cantidad de materia considerada. La longitud, la masa y el volumen son propiedades extensivas, puesto que cualquiera de éstas aumenta al aumentar la materia, lo mismo que el volumen, peso, número de moles, inercia, la porosidad.
Estas propiedades tienen que ver más con la estructura química interna de la materia, como la temperatura, el punto de fusión, el punto de ebullición, el calor específico o la concentración, tenacidad, acidez, elasticidad, magnetismo, maleabilidad, combustibilidad, electronegatividad; estas propiedades no dependen de la cantidad de materia presente. Las propiedades intensivas son importantes pues ayudan a identificar y a caracterizar una sustancia pura, aquella que está compuesta por un solo tipo de molécula, como el agua, que está formada sólo por moléculas de agua (H2O).
Esta propiedad se define como la cantidad de masa entre el volumen que ocupa. Al dividir dos propiedades extensivas, que dependen de la cantidad de materia, obtenemos una propiedad intensiva (la densidad no depende de la cantidad de materia, pero SI de la masa y el volumen. es una propiedad intensiva.
La densidad en forma matemática se define como la relación entre la masa y el volumen, para su cálculo se utiliza la siguiente expresión, la cual es la relación o cociente entre la masa del cuerpo dividida entre el volumen que ocupa y se expresa por la siguiente ecuación:
$$\textsf{densidad}(d) = \frac{\textsf{masa}(m)}{\textsf{volumen}(v)} \tag{3.1}$$Se ha de tener presente que aunque toda la materia posee masa y volumen la misma masa de sustancias diferentes ocupan distintos volúmenes, así notamos que el hierro o el cobre son pesados, mientras que la misma cantidad de algodón o plástico son ligeras por lo tanto, ocuparán más volumen. La propiedad que nos permite medir la ligereza o pesadez de una sustancia recibe el nombre de densidad. Cuanto mayor sea la densidad de un cuerpo, más pesado nos parecerá. La densidad se mide en Kg/m3, también en g/cm3.
Como podemos observar, la densidad tiene en cuenta la masa y el volumen, así entonces, dos objetos que tienen el mismo volumen, por ejemplo un bloque de madera y un ladrillo, pero pueden diferir en su masa y peso, por lo tanto tendrán diferente densidad.
Si se conocen dos cantidades cualesquiera de estas tres (masa, volumen y densidad) para una muestra de materia, es posible calcular la tercera. Por ejemplo, la masa de un objeto es el producto de su densidad por su volumen. pero también es posible conocer el volumen:
$$\textsf{masa}(g) = \textsf{volumen}(cm^3) × \textsf{densidad} \left(\frac{g}{cm^3} \right) \tag{3.2}$$Hay propiedades que pueden cambiar en una misma muestra, tal como la presión, la temperatura, el estado de reposo o de movimiento, la carga eléctrica, etc. La presión y la temperatura son cualidades muy importantes, pues siempre están adscritas a los cuerpos, determinando las propiedades de los mismos.
Veamos en qué consiste cada una de estas propiedades físicas, que además son intensivas:
La dureza es la resistencia que opone un cuerpo a ser rayado. La tenacidad es la resistencia a la ruptura.
Esta propiedad depende de la cantidad de materia, por lo que podemos decir que es mensurable (se puede medir), y es la propiedad de los cuerpos que hace que éstos tiendan a conservar su estado de reposo o de movimiento.
Es la propiedad de los cuerpos que les permite recuperar su forma original después de una deformación, es decir después de estirarse.
Este método se puede utilizar para encontrar la masa de un cuerpo, conocido su volumen y densidad:
Se tienen $25 cm^3$ de ácido acético, su densidad es $1, 0439 g/cm^3$, con cuánta masa del ácido se cuenta en este instante?
Solución
Remplazando los valores del volumen y de la densidad, podemos conocer la masa:
$$\textsf{masa} = \textsf{densidad} × \textsf{volumen} \to$$ $$\textsf{masa de ácido acético} = 1.0439 \frac{g}{c\cancel{m^3}} × 25 c\cancel{m^3}$$ $$\textsf{masa de ácido acético} = 26.1g$$El etilenglicol HO - CH2 – CH2 – OH, es utilizado como anticongelante, y para un experimento se cuenta con 60000 ml, además, se sabe que su densidad es de 1.1101 g/ml, a cuántos gramos equivale su masa?
Solución
$$\textsf{masa de etilenglicol} = 60.000 \cancel{ml} × 1.1101 \frac{g}{\cancel{ml}}$$ $$\textsf{masa de etilenglicol} = 606.606 g$$En tablas 3.2 a 3.7 encontraremos algunos valores de densidades comunes para los cálculos de estas propiedades:
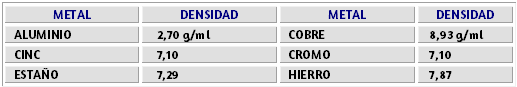
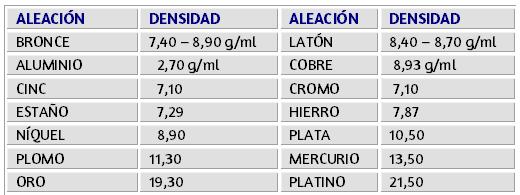
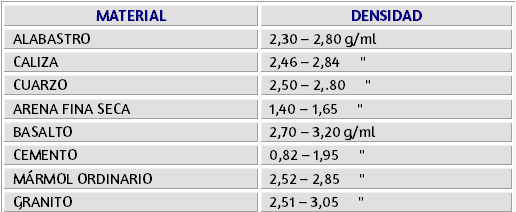
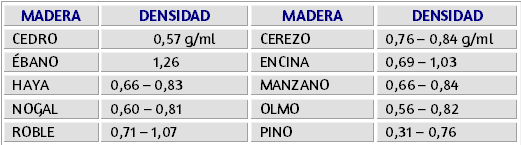
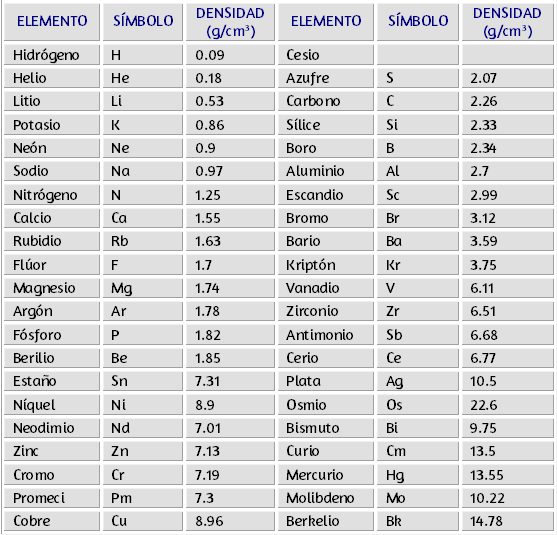
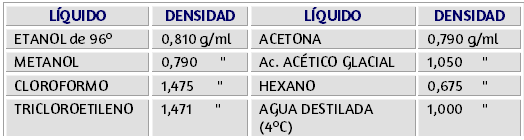
Es una propiedad física general de toda la materia, corresponde a los huecos que pueden ser llenados, también puede decirse que la porosidad es la presencia de pequeñas aberturas o espacios dentro de un material, esta aberturas pueden ser macro-aberturas como las que ocurren en el suelo, o micro-aberturas como los poros en la piel.
La porosidad está directamente relacionada con la permeabilidad, esta es la propiedad que tienen los cuerpos de permitir el paso de fluidos, bien sean, membranas, o el suelo.
Es una característica propia de los metales que permite la obtención de láminas muy delgadas. Esta propiedad aumenta al aplicar calor. Entre los metales más maleables en orden de precedencia se tienen: oro, plata, platino, cobre, estaño, plomo, cinc, hierro, níquel.
Es la propiedad que presentan algunos metales y aleaciones cuando se les aplica una fuerza se pueden estirar sin experimentar ruptura para obtener alambres o hilos.
Es la rapidez con que se quema un material, es la medida de la facilidad con la que una sustancia se incendia, ya sea a través de fuego o combustión.
Es una de las fuerzas fundamentales de la naturaleza, como lo es la gravedad. Al igual que la gravedad, que hace que los objetos se atraigan entre sí, la fuerza del magnetismo proviene de las propiedades de cargas eléctricas que ocasionan el movimiento en los átomos de un cuerpo.

Es otra propiedad útil de los elementos y los compuestos es la temperatura a la cual se funde el sólido (su punto de fusión) o hierve el líquido (su punto de ebullición).
La temperatura es una magnitud que refleja el nivel térmico de un cuerpo (su capacidad para ceder energía calorífica), da la idea de mayor o menor grado de agitación que poseen las moléculas.
El calor es la energía total del movimiento molecular en una sustancia, mientras temperatura es una medida de la energía molecular media. El calor depende de la velocidad de las partículas, su número, su tamaño y su tipo.
La temperatura no depende del tamaño, del número o del tipo. Por ejemplo, la temperatura de un vaso pequeño de agua puede ser la misma que la temperatura de un cubo de agua, pero el cubo tiene más calor porque tiene más agua y por lo tanto más energía térmica total.

El calor es lo que hace que la temperatura aumente o disminuya. Si añadimos calor, la temperatura aumenta. Si quitamos calor, la temperatura disminuye. Las temperaturas más altas tienen lugar cuando las moléculas se están moviendo, vibrando y rotando con mayor energía.
Si tomamos dos objetos que tienen la misma temperatura y los ponemos en contacto, no habrá transferencia de energía entre ellos porque la energía media de las partículas en cada objeto es la misma.
Pero si la temperatura de uno de los objetos es más alta que la otra, habrá una transferencia de energía del objeto más caliente al objeto más frío hasta que los dos objetos alcancen la misma temperatura.

La temperatura no es energía sino una medida de ella, sin embargo, el calor sí es energía.
Para medir la temperatura se han desarrollado varias escalas termométricas y son cinco escalas de temperatura las que están en la actualidad: la Celsius, conocida también como escala centígrada, la Fahrenheit, la Kelvin, la Ranking, y la escala internacional de temperatura termodinámica.
La escala centígrada, con un punto de congelación de $0° C$ y un punto de ebullición de $100°C$, La escala Fahrenheit, usada en países de habla inglesa es usada no solo con propósitos de trabajo científico sino con otros y con base en el termómetro de mercurio, el punto de congelación del agua se define en $32° F$ y el punto de ebullición en $212° F$.
En la escala Kelvin, la más usada, el cero se define como el cero absoluto de la temperatura, que es, $-273.15°C$ ó - $459.67°F$ ($459.70F$).
Otra escala que emplea el cero absoluto como su punto más bajo es la escala de Rankine, en la cual cada grado de temperatura es equivalente a un grado de la escala Fahrenheit. El punto de congelación del agua en la escala de Rankine es de $491.7° R$, y el punto de ebullición es de $671.7°R$.
Las dos escalas más comúnmente utilizadas son la centígrada, que divide la medición de temperatura en 100 partes iguales, denominadas grados centígrados, y la Fahrenheit, que también la divide en 180 partes iguales que se denominan grados Fahrenheit.
El grado centígrado representa un intervalo de temperatura mayor que el Fahrenheit. Un grado Fahrenheit es igual a $5/9$ de grado centígrado. La lectura en la escala centígrada indica directamente un intervalo de temperatura referido a uno de los puntos fijos que se toma como cero. La escala Fahrenheit se usa, sin embargo, en muchos países de habla inglesa.
La escala de temperaturas adoptada por el SI es la llamada escala absoluta o Kelvin. En ella el tamaño de los grados es el mismo que en la Celsius, pero el cero de la escala se fija en el $- 273, 16 °C$.
Este punto llamado cero absoluto de temperaturas es tal que a dicha temperatura desaparece la agitación molecular, (no hay movimiento de las partículas), no tiene sentido hablar de valores inferiores a él. El cero absoluto constituye un límite inferior natural de temperaturas, lo que hace que en la escala Kelvin no existan temperaturas bajo cero (negativas).
La escala kelvin es llamada escala de temperatura absoluta, porque no tiene valores negativos de temperatura, como se ha mencionado antes. La temperatura de ebullición del agua a una atmósfera en la escala kelvin es de $373.15 K$ y la temperatura de fusión es $273.15 K$, es imposible conseguir temperaturas de $K$, pero por medio de técnicas especiales se han obtenido temperaturas inferiores a $1K$.
Se le da el valor de $32°$ a la temperatura de fusión del agua y el valor de $212°$ a la de ebullición del agua. El intervalo de dichas temperaturas se divide en 180 partes, cada una de las cuales se denomina grado Fahrenheit ($°F$).
La temperatura de fusión del agua se designa por cero grados ($0°$) y la ebullición del agua por $80°$, dividiéndose el intervalo entre ellas en 80 partes, cada una de las cuales se denomina grado Réaumur ($°R$).
Es la escala absoluta correspondiente al Fahrenheit, donde el punto cero corresponde a $-459.7°F$. El punto de congelación del agua es de $492 °R$, y la temperatura de ebullición.
A una atmósfera es de $672°R$, es importante tener en cuenta que en la escala ranking el $0°R$ y el K coinciden. Comparativamente las diferentes escalas se pueden representar de acuerdo a la , la que representa las equivalencias entre las escalas de temperatura:
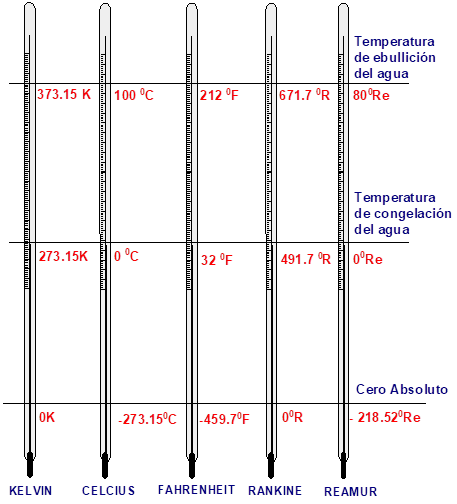
Muchos trabajos científicos y de laboratorio requieren representar las medidas de temperatura en términos de otra, lo que puede realizarse denominando los puntos de congelación en las diferentes escalas en la forma siguienteGARCÍA R, Arcesio. AUBAD L. Aquilino. ZAPATA P. Rubén. Química General, Corporación para investigaciones biológicas. Impresiones la pluma de oro. 1980:
$Reamur = Re$ y relacionando estos puntos con la diferencia entre el punto de congelación y de ebullición del agua en las diferentes escalas. Estas diferencias son las siguientes, Centígrada $= 100°C$, Kelvin $= 373.15 – 273.15 = 100 K$, Fahrenheit $= 212 – 32 = 180°F$, Ranking $671.7 – 491.7 = 180°R$ y Reaumur $= 80°Re$.

La temperatura no es energía sino una medida de ella, sin embargo, el calor sí es energía.
La conversión de una escala a otra se realiza estableciendo una proporción entre estos dos puntos, los cálculos se realizan como sigue:
Convertir $300C$ a las escalas Kelvin, Fahrenheit, Ranking y Reaumur.

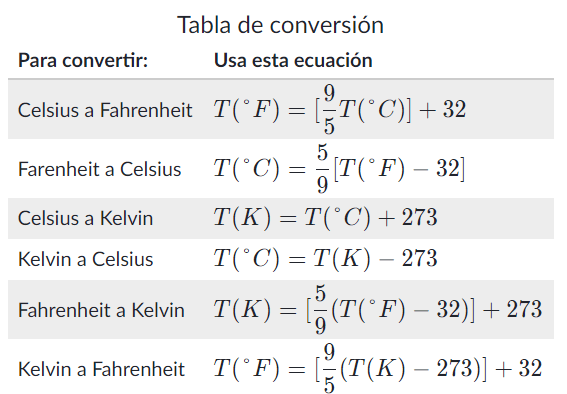
Resumiendo:
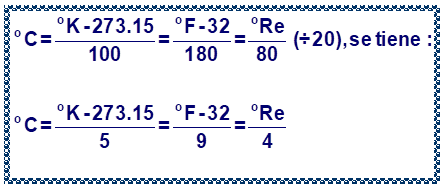
Para los siguientes ejercicios utilice las ecuaciones de conversión entre escalas para determinar la temperatura solicitada.
 Determinar la temperatura en grados centígrados y en grados Fahrenheit de un cuerpo, cuyo valor en Kelvin es de $77°K$.
Determinar la temperatura en grados centígrados y en grados Fahrenheit de un cuerpo, cuyo valor en Kelvin es de $77°K$.
Solución: Para la conversión de $K$ en $C$ se emplea la ecuación: $t(°C) = t(K) - 273$.

Convierta – $25°F$ a grados Celsius y Kelvin.
El primer termómetro fue inventado por Galileo Galilei (1564-1642) en 1602. El termómetro estaba compuesto por un pedazo de vidrio redondeado, llamado bulbo y un cuello fino, también de vidrio, que servía para ser sumergido en un recipiente que contuviera agua y colorante.
Crédito: Escuelapedia.com. http://www.escuelapedia.com/historia-del-termometro/
Es la temperatura a la que el líquido desprende vapor, en el seno del líquido pueden observarse burbujas, esta temperatura depende de la presión. A mayor altitud (menor presión), menor temperatura de ebullición. Por otra parte, los compuestos más ligeros se evaporan a menor temperatura que los más pesados. Esto es así debido a que los átomos de agua están tan fuertemente unidos que se necesita mucha energía (calor) para separarlas (convirtiéndolas en gas). El agua a una atmósfera de presión ebulle a $100°C$ y en una olla a presión, como el vapor de agua no puede escapar, aumenta la presión y así aumenta la temperatura de ebullición del agua, situándose por encima de los $100°$ y consiguiendo que los alimentos se cocinen más rápidamente.
Es la temperatura a la cual una sustancia empieza a cambiar de estado sólido a estado líquido. El hielo funde a la temperatura de $0°C$ y también, cuando el hielo funde, su temperatura permanece invariable ($°C$) hasta que todo el hielo se ha transformado en agua.
La siguiente tabla interactiva es adaptación de EDAD_3eso_estados_materia-JS/EDAD_3eso_estados_materia-JS.
Las propiedades químicas de los cuerpos se ponen de manifiesto cuando la sustancia sufre un cambio en su composición, así, cuando el hierro se oxida, el alcohol o la gasolina se queman, que el cloro reacciona con el sodio y se obtiene otra materia con propiedades completamente diferentes, ella es el cloruro de sodio o sal común, la que se utiliza en la cocina para darle sabor a los alimentos, de la combustión de un material también se obtiene otra sustancia con propiedades completamente diferentes.
No se debe olvidar que lo que está ocurriendo es un cambio químico, que la sustancia se está transformando en otra distinta y por consiguiente con propiedades diferentes. Los métodos de determinación de las propiedades químicas de los cuerpos constituyen la base del análisis químico.
En conclusión, la materia, o las sustancias experimentan transformaciones físicas y transformaciones químicas.

Un cambio físico modifica algunas propiedades de la sustancia pero no, hay motivos para suponer que se ha formado una nueva.
Por el contrario, en los cambios químicos, conocidos como reacciones, tiene lugar una modificación de todas las propiedades del cuerpo, lo que obliga a suponer que se ha formado una nueva sustancia.
Observa la figura siguiente y notarás la trasformación que han sufrido la materia que interviene en el proceso:

Las sustancias varían tan sólo en lo que respecta a la modificación producida y en una extensión que depende de ella, pero las propiedades químicas de estas substancias permanecen inalteradas; ha tenido lugar en cada caso un fenómeno físico.
Si se llega a fundir el pedazo de azufre o si el cloro se licua, las propiedades físicas cambian totalmente, y el comportamiento químico del azufre fundido o el del cloro líquido es el mismo que el del azufre sólido o el del cloro gaseoso, por lo que el proceso de fusión o el de licuación es también un cambio físico que afecta únicamente al estado de agregación de la sustancia correspondiente.
En cambio, si se calienta óxido mercúrico, polvo rojo, en un tubo de ensayo, se desprende oxígeno y en la parte superior del tubo se condensa mercurio en forma de minúsculas gotas; ha tenido lugar un cambio químico.
Así, por ejemplo, la formación de $1 g$ de agua a temperatura ambiente, a partir de hidrógeno y oxígeno, desprende cerca de $3800$ calorías, mientras que la solidificación a hielo de $1 g$ de agua o la condensación a agua líquida a $100 °$ de $1 g$ de vapor de agua desprende tan sólo, respectivamente, cerca de $80$ ó de $540$ calorías.
En algunos casos, tal como en la disolución del cloruro de hidrógeno gaseoso o incluso del cloruro sódico en agua o la simple dilución del ácido sulfúrico concentrado, parece difícil decidir claramente si un proceso es químico o físico, ya que ofrece aspectos de uno y otro tipo de transformaciones.
El planeta tierra, el Sol, las estrellas, y todo lo que el hombre ve, toca o siente, es materia; incluso, los propios hombres, lo que observas en tu salón de clase, las sillas, el tablero, los marcadores, el borrador, etc.; las plantas y los animales.
La materia existe en tres estados físicos sólido, líquido, gaseoso, dependiendo de la temperatura, la presión atmosférica, y las características específicas del tipo de materia. Una misma materia se puede encontrar en los tres estados. Por ejemplo, el agua, que normalmente es líquida, cuando se enfría se convierte en sólido y, si se le aplica calor, se transforma en gas.

Un gas es una sustancia formada por moléculas que se encuentran separadas entre sí. Los gases no tienen forma propia, ya que las moléculas que los forman se desplazan en varias direcciones y a gran velocidad.Por esta razón, ocupan grandes espacios, pueden fluir, son compresibles y poseen alta dilatación, ya que las fuerzas de atracción entre sus partículas son extremadamente débiles comparadas con los sólidos; esto explica la difusión de los gases.
debido a que los gases tienen sus partículas muy separadas éstos ocupan todo el volumen del recipiente que los aloja, por lo tanto, la forma de los gases variable debido a que adoptan la forma del recipiente donde se encuentran.Entre las propiedades que se pueden medir fácilmente en un gas, se encuentran; su volumen, su temperatura y presión.
Este corresponde al espacio en donde se mueven las moléculas, y corresponde al volumen del recipiente que o contiene, el volumen de un gas se puede expresar en centímetros cúbicos ($cm^3$), metros cúbicos ($m^3$), litros o mililitros, siendo la unidad de volumen más utilizada cuando se trabaja con gases el litro. El volumen de un gas, puede decirse que es variable, puesto que a éstos se les puede comprimir o expandir.
Si se aumenta la presión de un gas, lo que se logra es disminuir el espacio que hay entre cada partícula que lo conforma, caso que no ocurre con los demás estados de la materia.Los gases son fluidos, al igual que los líquidos éstos pueden fluir, por ello reciben este nombre.
La presión puede asociarse con la idea de fuerza, es decir, es la fuerza por unidad de área, $P = F/A$ por lo tanto, la presión será la fuerza que actúa en un área determinada producida por las partículas del gas al chocar contra las paredes del recipiente.
La presión direcciona el flujo del gas, sus unidades son milímetros de mercurio ($mmHg$), Pascales ($Pa$) o Kilopascales ($KPa$), la unidad estándar en el Sistema Internacional de medidas es el Pascal o $Newton/metro^2$ ($N/m^2$).La presión atmosférica puede medirse utilizando un barómetro de mercurio, ésta es la presión ejercida por el aire sobre la superficie de la tierra y varía según la altura sobre el nivel del mar.
El manómetro consiste en un aparato que está formado por un tubo de vidrio de longitud mayor a $76 cm$. que se encuentra cerrado en uno de sus extremos. El tubo se llena con mercurio y se invierte sumergiéndolo en un recipiente con este metal. Se debe tener cuidado para que al realizar la operación no entre aire al tubo. Cuando el tubo se invierte de esta manera, parte del mercurio sale del tubo, pero parte permanece dentro de la columna.
La superficie de mercurio que se encuentra fuera del tubo sufre la fuerza completa dela atmósfera terrestre por cada unidad de área. Sin embargo, la atmósfera no está en contacto con la superficie de mercurio dentro del tubo. La atmósfera empuja al mercurio haciendo que suba hasta la presión debida al peso del mercurio se iguale a la presión atmosférica.La presión atmosférica medida a nivel del mar a $0°C$ da como resultado unos $760 mm Hg$ que son el equivalente a $1$ atmósfera de presión, a $101, 3KPa$, a $1, 0332Kg/cm^2$, a $7, 6x10^2 torr$ (torricelli, un $torr = 1 mmHg$ o a $1, 01325 bares$, dependiendo de la unidad en que se requiera expresar la presión.

La presión de los gases se mide con un aparato llamado manómetro, el cual tiene principios de operación similares a los del barómetro, para medir la presión de gases que se encuentran en espacios cerrados. La siguiente imagen (a) muestra un manómetro de tubo cerrado, éste se utiliza para medir presiones por debajo de la presión atmosférica. La presión es justamente la diferencia en la altura del nivel de mercurio en las dos ramas.
Un manómetro de tubo abierto tal como el que se muestra en la Imagen (b) y (c) se utiliza con frecuencia para medir las presiones de gases cercanas a la presión atmosférica. La diferencia en la altura de las columnas de mercurio en los dos brazos del manómetro relaciona la presión del gas con la presión atmosférica . Si la presión del gas que se encuentra encerrado es la misma que la presión atmosférica, el nivel en los dos brazos es el mismo.
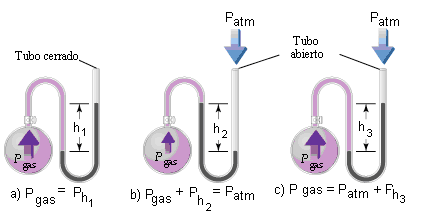
Si la presión del gas encerrado es menor que la presión atmosférica, el mercurio se encuentra a una altura menor en el brazo que está expuesto a la atmósfera, tal como se ilustra en la Imagen (b). Si la presión atmosférica es menor que la presión del gas, el mercurio alcanza un nivel inferior en el brazo que está en contacto con el gas, como se muestra en la Imagen (c).
La temperatura mide el grado de agitación de las partículas de un cuerpo o un sistema. Por lo tanto, cuando aumenta la temperatura, también lo aumenta el movimiento de las partículas o moléculas del gas o del sólido, o líquido, según de la clase de materia que se trate. La temperatura, se expresa en grados, bien sea grados Celsius o grados Kelvin, pero la más utilizada es la escala absoluta, es decir, la escala Kelvin.
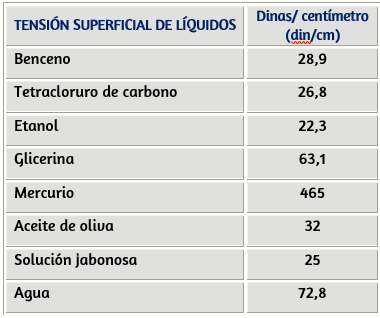
Los líquidos tienen propiedades bien definidas, que los diferencian de los estados sólido y gaseoso; éstas son: Tener volumen constante, forma variable; pueden fluir, son poco compresibles. Además, poseen características especiales como son: la viscosidad variable, la tensión superficial, la capilaridad.Los líquidos son fluidos porque no tienen forma propia, sino que toman la del recipiente que los contiene.
Es la resistencia interna a fluir que presenta un líquido.
Esta propiedad es una consecuencia de las atracciones intermoleculares que ocurre en el seno de los líquidos. Una molécula es atraída en todas direcciones con la misma intensidad por las moléculas que la rodean, pero una molécula en la superficie de separación de la fase líquida con la fase vapor está expuesta a atracciones como se muestra en la .

Para observar este fenómeno sin necesidad de sacrificar un insecto, lo puedes hacer utilizado un alfiler o una aguja, un trozo de papel higiénico, un plato hondo que contenga agua y procede de la siguiente manera:Primero que todo, debes llenar el plato con agua trata de colocar la aguja o el alfiler sobre el agua, notarás que de inmediato se hunde porque al tocar el agua con tus dedos estás rompiendo la atracción entre las moléculas, por lo tanto, debes coger un cuadro pequeño de papel higiénico y colocarlo sobre el agua e inmediatamente colocar la aguja o el alfiler sobre éste, observarás que el papel se deposita en el fondo del plato cuando se humedece, pero, la aguja o alfiler que estás utilizando en el experimento queda sobre el agua.

Tabla de tensiones superficiales de líquidos a $20 °C$ Propiedades físicas de los gases. http://materias.unq.edu.ar/qui01/silvina/seminarios/gasS.doc
Esta es una propiedad física del agua, debida a la tensión superficial, en la que un líquido asciende por un tubo muy estrecho debido a las fuerzas atractivas entre sus moléculas y la superficie interior del tubo que son fuerzas de adhesión, esta superficie interior del tubo es de unos milímetros o micras de diámetro, llamado capilar.
La capilaridad es bastante importante y aplicable en la cotidianidad, por ejemplo cuando se moja una servilleta, cuando dejas un cubo de azúcar cobre un poco de líquido, esta propiedad permite que el el líquido sea absorbido por el azúcar en cubo, cuando la humedad sube por la pared, y es la propiedad que permite que las raíces de las plantas lleven el agua hasta las hojas donde se realiza la fotosíntesis. La ilustra la propiedad de capilaridad Capilaridad. (crédito: Las propiedades del agua y el medio ambiente. Investigando las propiedades del agua. La capilaridad del agua. http://cidta.usal.es/cursos/agua/modulos/Practicas/propiedades7/capilaridad.html.
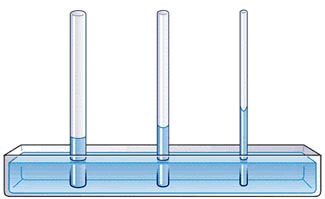
Un sólido es una sustancia formada por moléculas, que se encuentran muy unidas entre sí por una fuerza llamada Fuerza de Cohesión. Los sólidos son duros y difíciles de comprimir, porque las moléculas, que están muy unidas, no dejan espacio entre ellas.Una propiedad de los sólidos es que no son compresibles.
Los sólidos se pueden clasificar en cristalinos y amorfos, los que se diferencian entre sí por su estructura. Los sólidos cristalinos son los mismos cristales, ellos tienen las partículas acomodadas en formas geométricas definidas, un ejemplo de estos cristales son el diamante, los cristales de cloruro de sodio, las esmeraldas, sulfato de cobre. Veamos en la siguiente escena interactiva una adaptación del trabajo de Adaptación del trabajo de Enric Ripoll Mira: "Adaptación a DescartesJS"
Los sólidos amorfos son partículas dispuestas en forma irregular, por lo tanto, no tienen una forma definida como los cristales, pero difieren de los cristales por la forma en que se funden, si se controla la temperatura de un sólido cristalino en el proceso de fundición, podrá notarse que ésta permanece constante, mientras que los sólidos amorfos no poseen una temperatura de fusión definida o estable, ellos se suavizan y funden en un rango de temperatura no teniendo un punto de fusión determinado.
Un ejemplo de estos sólidos son el vidrio, los polímeros naturales y plásticos.
La siguiente escena es también una adaptación del trabajo de Enric Ripoll Mira.
Un cambio de estado es la evolución de la materia entre varios estados de agregación sin que ocurra un cambio en su composición. Teniendo presente que los tres estados fundamentales de la materia son el sólido, líquido y gaseoso, se van a considerar los cambios que acompañan a estos tres estados de la materia; teniendo en cuenta que cada uno de los cambios va acompañado con una transformación de calor; veamos como ocurren estas transformaciones y cambios de energía:
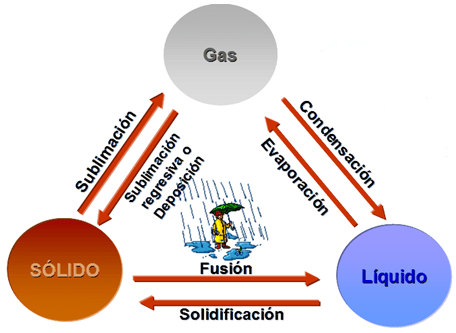
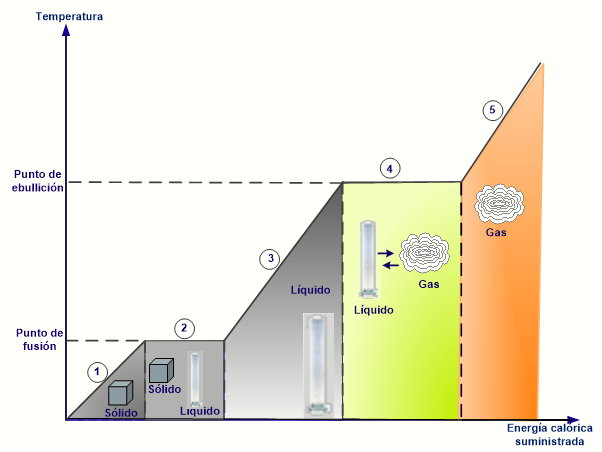
Algunos sólidos se convierten en gas directamente sin pasar por el estado líquido, siendo este un proceso endotérmico (es decir, requiere que se aplique calor al sistema), y se llama sublimación.
Lo inverso a la sublimación es la deposición que corresponde a un proceso exotérmico (desprende o produce calor); en general las sustancias pasan del estado gaseoso al estado líquido y al sólido a medida que se elimina más calor y el proceso será lo contrario o se invierte si se añade más y más calor.

El laboratorio de química es el lugar donde se desarrollan prácticas para validar los conocimientos teóricos impartidos en aula de clase, así que, todos los principios, herramientas y técnicas de Química se desarrollan en el laboratorio.
La experiencia de observar un fenómeno químico y luego explicarlo no se puede ganar simplemente leyendo un libro de texto o escuchando una clase. Es en el laboratorio en donde se vive la química, es allí donde se desarrollan las técnicas, se registran e interpretan datos y se deducen teorías en contexto con el mundo real que permiten que éste sea mejor entendido.
En particular, las prácticas de laboratorio que se presentan en este manual, son el producto de la consulta y análisis detallado de las prácticas más usuales en diferentes Universidades e Institutos a nivel mundial, buscando con el material seleccionado dar la oportunidad de observar variados fenómenos de la Química bajo condiciones controladas y deducir de ellas los principios básicos que constituyen el fundamento de esta disciplina científica. Así, el laboratorio de Química debe ser un lugar de descubrimiento y aprendizaje para cada estudiante, por ello, éste debe llegar con la suficiente preparación previa, habiendo estudiado los pasos a seguir en cada ensayo, observando las reglas de seguridad pertinentes y conociendo cómo ha de elaborarse el informe de resultados.
Ello requiere que el estudiante se convierta en protagonista de su propio aprendizaje, que se implique de forma activa en todo el proceso.
El papel del profesor es principalmente el de crear situaciones que permitan al alumno intervenir activamente en su proceso de aprendizaje para que, lejos de limitarse a memorizar los conceptos, pueda integrarlos dentro de su propio sistema cognitivo, relacionándolos con los que previamente conoce.

Haz clic en la imagen de abajo para abrir el documento de prácticas de laboratorio.
 Ya antes se había respondido a la pregunta ¿qué es materia?, ahora se va a responderla misma pregunta de una manera más libre y cotidiana, por ello se hará referencia a la materia como todo aquello que ocupe un espacio y tenga masa.
Ya antes se había respondido a la pregunta ¿qué es materia?, ahora se va a responderla misma pregunta de una manera más libre y cotidiana, por ello se hará referencia a la materia como todo aquello que ocupe un espacio y tenga masa.
Así, por lo tanto, materia es todo lo que nos rodea, la silla en que las personas se sientan, los zapatos, la ropa, el tablero, las paredes con sus distintos colores, cuando se mira nuestro entorno, los vidrios de las ventanas, las paredes, los carros, etc. Se puede evidenciar la materia y darnos cuenta que ésta se presenta de distintas formas, alguna materia tendrá forma definida, a otra clase de materia no se le podrá definir exactamente su forma, será sólida, liquida o gaseosa, tendrá distintos colores; no solamente esto es materia, se puede percibir el calor y el frío, la luz, cuando se enciende la radio, se escucha la voz de las personas a través de éste mediante las ondas de radio, también están las ondas electromagnéticas, la luz que emite un bombillo, a ellas se les clasifica como diferentes formas de energía.
Así entonces, puede decirse que materia y energía son entonces los únicos componentes de nuestra realidad física, estos dos conceptos fueron relacionados por Albert Einstein, mediante su ecuación $E = mc^2$, es decir, la energía refleja la esencia misma de la materia: el movimiento, Así pues, la energía no es algo externo a la materia, implantada en ella desde el exterior, sino que es una cualidad inherente de la materia.
Cuando se observa nuestro entorno se puede notar que hay animales, árboles, ventanas, puertas, muros, ríos, cada uno de ellos es materia, qué clase de materia, sería la pregunta que se puede formular, para poder responderla pregunta será necesario clasificar la materia y para ello serán necesarias tres preguntas: ¿Qué es un elemento?, ¿Qué es un compuesto?, ¿Qué es una mezcla y cómo se clasifican?
En páginas anteriores, se hizo referencia a la definición de elemento, pero en este apartado la retomaremos nuevamente:
Las sustancias puras se dividen en dos grupos, los elementos y los compuestos.
Es toda aquella sustancia que no se puede descomponer en otras más simples mediante procesos químicos convencionales. Ejemplos de elementos son: cobre, oro, sodio, hidrógeno, oxígeno, nitrógeno, el flúor, el oro, el yodo, la plata, el sodio, el carbono, el mercurio, etc.
Un compuesto es una sustancia pura conformada por dos o más elementos, por lo tanto, se puede descomponer mediante distintos métodos químicos en dos o más sustancias simples, algunos ejemplos son: el agua(H2O), la sal de cocina (cloruro de sodio NaCl), el azúcar (Sacarosa, o sus sinónimos: beta-D-fructofuranosil-alfa-D-glucopiranosida, alfa-D-glucopiranosil-beta-D-fructofuranosida; el ácido acético (CH3COOH), el ácido sulfúrico (H2SO4).

La materia homogénea y heterogénea son diferentes entre sí por su aspecto.
Esta clase de materia es uniforme en sus propiedades y toda su composición se mantiene constante en cualquiera de sus partes. Por ejemplo la sal, el azúcar.
Esta es una clase de materia que no es uniforme en su composición ni en sus propiedades, está conformada por dos o más fases, distribuidas en forma irregular y físicamente diferentes, ejemplo: el agua con aceite, cuando estas dos sustancias o compuestos se mezclan ellos no se disuelven entre sí y finalmente terminarán por separarse. Otros ejemplos de mezclas heterogéneas son la tierra, la gasolina con el agua, el granito, el hormigón.Por ejemplo, el agua que se utiliza para beber, para el aseo diario, esta agua, contiene unas sustancias llamadas sales minerales, las que se encuentran disueltas en ella; por eso decimos que el agua potable es una mezcla de agua y sales minerales, por ello, podemos decir que las mezclas se dan al unir varias sustancias y pueden ser homogéneas y heterogéneas.
Una mezcla esta constituía por dos o más sustancias puras donde cada una mantiene su identidad y sus propiedades Así, la leche es una mezcla formada por agua y numerosos compuestos químicos, tales como, azúcares, grasas, proteínas y sales minerales-, mientras que el aire es una mezcla de gases, formada, fundamentalmente, por oxígeno y nitrógeno, donde, además existen otros gases como CO2 y pavor de agua.
También reciben el nombre de disolución, las mezclas homogéneas están formadas por una sola fase, es decir, no se pueden distinguir las partes que la conforman, presenta la misma composición en cualquiera de sus partes.
En una disolución el componente que está en mayor proporción y que generalmente es líquido se denomina disolvente, y el que está en menor proporción soluto.
Un ejemplo de una mezcla homogénea es el aire no contaminado, el agua con sal de cocina, agua y alcohol.
Tienen más de una fase, no tienen las mismas propiedades en toda la muestra.Se pueden distinguir las fases a simple vista o utilizando un microscopio. Las fases pueden estar en el mismo estado físico o en otro estado distinto. Por ejemplo: agua y aceite, arena y agua, hierro y azufre, el granito.

Es importante establecer una diferencia entre compuesto y mezcla: Los compuestos, análogamente a las mezclas, están constituidos por dos o más cuerpos diferentes, pero se diferencian esencialmente por:
Los elementos y compuestos por o general se encuentran en la naturaleza mezclados con otras sustancias. El aire por ejemplo, es una mezcla homogénea de varios gases: nitrógeno, oxígeno, argón, dióxido de carbono, vapor de agua y otros; la bauxita es una mezcla de dos óxidos: el férrico y el de aluminio.
En química, por lo general se trabaja con sustancias puras, por lo que es necesario separarlas de las mezclas y purificarlas. Existen diferentes técnicas de separación, las cuales pueden clasificarse según el tipo de mezcla que se posea, así:
Técnica que permite separar mezclas conformadas por partículas de diferentes tamaños. Se utilizan cedazos o tamices, los cuales se clasifican según el número de malla por unidad de superficie ( en centímetros cuadrados) y por el diámetro de los orificios de la malla. Esta técnica es muy utilizada en el estudio de la composición y características de los diferentes tipos de suelos.
Los tamices de laboratorio para análisis granulométrico son de 8", y están fabricados en tres partes: aro superior roscado, filtro tensable (tamiz) y aro inferior roscado. Para armar el tamiz, es necesario poner el filtro tensable en la parte media (como se ve en la ilustración), enroscar e ir tensando hasta dejar el tamiz completo en una unidad. Los aros están fabricados en nylon y el tamiz (intercambiable) en acero inoxidable.
La ventaja que este tamiz ofrece es el ahorro tanto económico al ser intercambiables, como el de espacio; y las medidas van desde 4 hasta 400 mesh. También contamos con la tapa de aluminio y la charola receptora en aluminio con recubrimiento anti-adherente.
La malla es de acero inoxidable y es un medio de filtración eficaz; es utilizada para separar, cribar o tamizar diferentes tipos de productos, y puede ser utilizada en cualquier industria.
Se producen diferentes tipos de tejidos de mallas, los cuales tienen características particulares, haciéndolas aptas para usos específicos. La medida que se usa en la tela metálica es "MESH" y quiere decir número de aberturas por pulgada lineal. Se cuenta empezando desde el centro de un alambre anotando el número de aberturas que hay hasta un punto a una pulgada de distancia.
Cuando la cuenta no llega a un número entero, es necesario indicar la parte fraccional o sobrante. Cuando la malla se especifica como parte fraccional de pulgada, ha de entenderse que ella representa la abertura o espacio libre entre los alambres.
Es una operación mecánica utilizada para separar un líquido de otra sustancia insoluble, la que puede ser un sólido para luego utilizar la filtración obtener el líquido completamente separado del sólido.

También se puede tener una mezcla de un líquido con un líquido los cuales no se mezclan, se utiliza el embudo de decantación o embudo de separación, para separar los dos líquidos.
Es un método físico que se utiliza para separar mezclas heterogéneas. En este tipo de mezclas uno de los componentes es una sustancia líquida y otra sólida, las que no son solubles. La mezcla se hace pasar por un material poroso donde el sólido queda atrapado.

La centrifugación es un método mecánico de separación de líquidos no miscibles, o de sólidos y líquidos por diferencia de densidad, con la aplicación de una fuerza centrífuga, el sólido se deposita en el fondo del tubo de ensayo utilizado para centrifugar por decantación y después se remueve el sólido.

La centrífuga se utiliza de la siguiente manera:
Note que debe apagar la centrífuga y esperar a que pare de girar. Repita el proceso hasta que logre la separación efectiva del precipitado y la solución.

Proceso que consiste en calentar un líquido hasta que sus componentes más volátiles pasan a la fase de vapor y, a continuación, enfriar el vapor para recuperar dichos componentes en forma líquida por medio de la condensación. El objetivo principal de la destilación es separar una mezcla de varios componentes aprovechando sus distintas volatilidades, o bien separar los materiales volátiles de los no volátiles.
En la evaporación y en el secado, normalmente el objetivo es obtener el componente menos volátil; el componente más volátil, casi siempre agua, se desecha. Sin embargo, la finalidad principal de la destilación es obtener el componente más volátil en forma pura. Por ejemplo, la eliminación del agua de la glicerina evaporando el agua, se llama evaporación, pero la eliminación del agua del alcohol evaporando el alcohol se llama destilación, aunque se usan mecanismos similares en ambos casos.
Si la diferencia en volatilidad (y por tanto en punto de ebullición) entre los dos componentes es grande, puede realizarse fácilmente la separación completa en una destilación simple. Si los puntos de ebullición de los componentes de una mezcla sólo difieren ligeramente, no se puede conseguir la separación total en una destilación individual. Un ejemplo importante es la separación de agua, que hierve a $100 °C$, y alcohol, que hierve a $78.5 °C$. Así por ejemplo, para obtener una disolución que contenga un 50% de alcohol (frecuente en el whisky), el destilado ha de destilarse una o dos veces más, y si se desea alcohol industrial (95%) son necesarias varias destilaciones.
Es la separación de un sólido soluble de la solución que lo contiene, en forma de cristales. Los cristales pueden formarse por fusión, por disolución, o por sublimación.
Para cristalizar una sustancia por fusión, como por ejemplo el azufre, éste se coloca en un crisol y se funde por calentamiento, se enfría y cuando se forma una costra en la superficie, rehace un agujero en ella y se invierte el crisol, vertiendo el líquido que queda dentro.
Consiste en saturar un líquido o disolvente por medio de un sólido o soluto y dejar que se evapore lentamente, hasta que se formen los cristales. También puede hacerse una.
solución concentrada al calor y dejarse enfriar. Si el enfriamiento es rápido, reobtendrán cristales pequeños, si el enfriamiento es lento, cristales grandes.
la sublimación es el paso directo de un sólido a gas, como sucede con el yodo y la naftalina al ser calentados, (la naftalina son las bolitas de matapolilla que se consiguen en las farmacias o con los vendedores ambulantes), estos al ser enfriados los gases originan la cristalización por enfriamiento rápido. El hielo seco, (gas carbónico congelado), al hacer contacto con el aire, pasa directamente a estado gaseoso, sin pasar por el estado líquido.
Otros métodos de separación son el magnetismo, el que se puede realizar se da cuando la mezcla esta formada por un elemento metálico y otro no metálico, los cuales se pueden separar mediante un imán. La propiedad de ser atraídas por los imanes que presentan estas sustancias se aprovecha para separarlas del resto de los componentes de una mezcla.
La cromatografía es otro método de separación, es una técnica de separación en la que hay dos fases (sólida, líquida o gas) una móvil y otra estacionaria, que se mueven una con respecto de la otra manteniendo un contacto íntimo. La muestra se introduce en la fase móvil y los componentes de la muestra se distribuyen entre la fase estacionaria y la móvil.
Los componentes de la mezcla a separar invierten un tiempo diferente en recorrer cada una de las fases, con lo que se produce la separación. Si un componente está la mayor parte del tiempo en la fase móvil el producto se mueve rápidamente, mientras que si se encuentra la mayor parte en la fase estacionaria, el producto queda retenido y su salida es mucho más lenta. Existen técnicas de cromatografía dependiendo del medio utilizado para separar las sustancias, ellas son: Cromatografía de papel, cromatografía de columna, cromatografía de capa delgada y cromatografía de gas.
Cromatografía de Papel: Un método que implica poner una gota de un líquido a ser investigado se pone cerca de un extremo de una tira del papel. Este extremo se sumerge en el solvente que viaja abajo del papel y distribuye los materiales presentes en la gota originalmente seleccionada. Comparación con sustancias conocidas hacen posible la identificación. Se coloca por medio de un capilar, una cantidad mínima de la solución que contiene las sustancias que se van a separar, por ejemplo, tinta, a continuación se coloca dentro de un solvente. El solvente es agua que al subir por el papel arrastra los componentes de la mezcla, pero como estos viajan a distinta velocidad a través del papel se van separando y originando las distintas manchas correspondientes a los componentes de la tinta. En la técnica de separación por cromatografía siempre es necesario efectuar la operación con diferentes solventes y aún con mezclas hasta encontrar el que mejor efectúe la separación. La cromatografía (crédito: GARCÍA R. Arcesio., AUBAD L. Auilino. ZAPATA P. Rubén. Química general. Corporación para investigaciones Biológicas. Impresiones Pluma de Oro. Segunda edición (p. 19).

"El agua se ha convertido en un recurso muy valioso. Hay algunos lugares en los que un barril de agua cuesta más que un barril de petróleo". (Lloyd Axworthy)"


"Para que medir tenga sentido, debe hacerse con un propósito concreto. Por lo general, mejorar nuestros resultados". Anónimo


Las Ciencias experimentales miden muchos fenómenos. Los aspectos medibles de un fenómeno se denominan magnitudes. La medida de cualquier magnitud se expresa mediante un número seguido de una unidad. Cuando medimos la cantidad de un líquido que hay e un recipiente, y encontramos que ésta es de $3$ litros, el volumen es la magnitud, expresarlo en litros ($L$) es unidades en que se mide dicho volumen y $30$ es la medida del volumen; por tanto, todas las propiedades medibles de la materia perteneces a una de dos categorías: sus propiedades intensivas o extensivas, donde el valor de una propiedad extensiva depende de la cantidad de materia considerada.
Medir una magnitud supone compararla con otras medidas. Todo valor obtenido en una medida viene condicionado por posibles errores experimentales (accidentales y sistemáticos) y por la sensibilidad del aparato utilizado. En las medidas Influyen el observador, las circunstancias en que mide y la calidad del aparato que utiliza. Toda observación está condicionada por la imperfección de los sentidos, y el error cometido en el proceso de medida tiene un significado distinto a "equivocación": El error es inherente a todo proceso de medida.
La medida de una magnitud física supone, en último extremo, la comparación del objeto que encarna dicha propiedad con otro de la misma naturaleza que se toma como referencia y que constituye el patrón.
En el proceso de medir se ha de conocer que es una magnitud y cuáles son los patrones básicos:
Magnitud es algo cuantificable, es decir, medible, ponderable, es aquello se pueden expresar con un número, (ya en el libro de la Sabiduría se dice: "Tú lo has regulado todo con medida, número y peso". Las magnitudes pueden ser directamente apreciables por nuestros sentidos, como los tamaños y pesos de las cosas, o más indirectas (aceleraciones y energías).
Medir implica realizar un experimento de cuantificación, normalmente con un instrumento especial (reloj, balanza, termómetro, probeta, pipeta, etc.).
 Cuando se consigue que la cuantificación sea objetiva (no dependa del observador y todos coincidan en la medida) se llama magnitud física (tiempos, longitudes, masas, temperaturas, aceleraciones, energías). Hay otras magnitudes que no resultan cuantificables universalmente: gustos, sabores, colores, ruidos, texturas, las propiedades que no dependen de la cantidad de materia, las propiedades físicas intensivas, puede existir alguna propiedad física relacionada, como la potencia sonora con el ruido, la longitud de onda de la luz con el color, etc.
Cuando se consigue que la cuantificación sea objetiva (no dependa del observador y todos coincidan en la medida) se llama magnitud física (tiempos, longitudes, masas, temperaturas, aceleraciones, energías). Hay otras magnitudes que no resultan cuantificables universalmente: gustos, sabores, colores, ruidos, texturas, las propiedades que no dependen de la cantidad de materia, las propiedades físicas intensivas, puede existir alguna propiedad física relacionada, como la potencia sonora con el ruido, la longitud de onda de la luz con el color, etc.
Se llaman unidades de medida, para especificar el valor de una magnitud hay que dar la unidad de medida y el número que relaciona ambos valores. De nada sirve decir que la altura de un árbol es de $5$ o decir que es de no sé cuantos metros. Aunque la relación del valor numérico con la unidad de medida es multiplicativa (ejemplo, $5$ veces un metro), la norma de escritura es separar con un espacio en blanco ambos términos. Por ejemplo, cuando se escribe $L = 1500 m$, que se lee "ele (longitud de…) igual a mil quinientos metros" se quiere decir que la longitud denominada $L$ mide aproximadamente $1500$ veces más que la longitud del metro patrón, que es lo mismo que decir $L = 1,5 km$, y que no tiene sentido si sólo se dice "$L = 1,5$".
 Las mediciones que suelen hacerse en esta ciencia experimental, a menudo son utilizadas para obtener otras cantidades relacionadas, los químicos utilizan distintos instrumentos de medida, como es el flexómetro, para medir longitudes, mientras que con el beacker, la bureta, la pipeta, la probeta, se mide el volumen, la balanza, mide la masa y con el termómetro la temperatura a la que ocurren los diferentes cambios de la materia. Los instrumentos de medida pueden ser tan sencillos como un nanómetro o tan sofisticado como un microscopio electrónico.
Las mediciones que suelen hacerse en esta ciencia experimental, a menudo son utilizadas para obtener otras cantidades relacionadas, los químicos utilizan distintos instrumentos de medida, como es el flexómetro, para medir longitudes, mientras que con el beacker, la bureta, la pipeta, la probeta, se mide el volumen, la balanza, mide la masa y con el termómetro la temperatura a la que ocurren los diferentes cambios de la materia. Los instrumentos de medida pueden ser tan sencillos como un nanómetro o tan sofisticado como un microscopio electrónico.
En química es importante medir:
La unidad de densidad en el Sistema Internacional es el $kg/m^3$; otra unidad de uso común es el $g/cm^3$.
a densidad es una propiedad de la materia que no depende de la masa, es decir, $1 kg$ de hierro tiene la misma densidad que $2 kg$ de hierro.
El Sistema Internacional de Unidades, abreviado SI, también denominado Sistema Internacional de Medidas, es el heredero del antiguo sistema métrico decimal, por lo que el SI también es conocido de forma genérica como sistema métrico.
Una de las principales características del Sistema Internacional de Medidas, es que sus unidades están basadas en fenómenos físicos fundamentales. La única excepción a esta regla es la definición de la unidad de la magnitud Masa, el kilogramo, que está definida como la masa de un prototipo internacional del kilogramo que está almacenado en la Oficina Internacional de Pesos y Medidas, en Sèvres, Francia La cromatografía (crédito: Ingemecánica. Sistema Internacional de Unidades de Medida. https://ingemecanica.com/tutoriales/unidadesdemedida.html).
Las unidades del SI son la referencia internacional de las indicaciones de todos los instrumentos de medida, y a las que están referidas a través de una cadena ininterrumpida de calibraciones o comparaciones.
El Sistema Internacional de Unidades consta de siete unidades básicas, también denominadas unidades fundamentales, que definen a las correspondientes magnitudes físicas fundamentales, que han sido elegidas por convención, y que permiten expresar cualquier magnitud física en términos o como combinación de ellas.
Las magnitudes físicas fundamentales se complementan con dos magnitudes físicas más, denominadas suplementarias.
Por combinación de las unidades básicas se obtienen las demás unidades, denominadas unidades derivadas del Sistema Internacional, y que permiten definir a cualquier magnitud física.
Este sistema se basa en siete unidades fundamentales, y unidades derivadas que se enumeran en la tabla siguiente:
El orden de magnitud de los múltiplos y submúltiplos se indican mediante prefijos que definen un valor fraccionario o un múltiplo de la unidad básica.
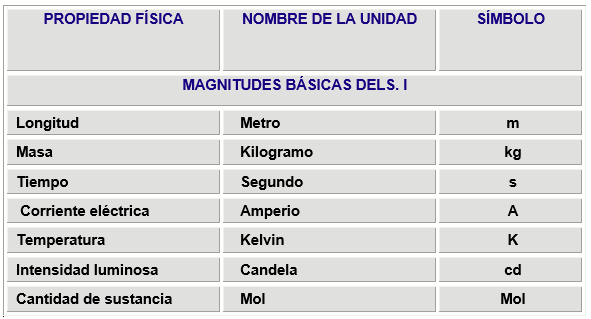
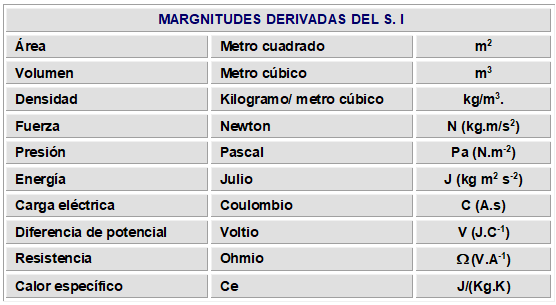
La 11ª Conferencia General de Pesas y Medidas, en sus sesiones de octubre de 1960 celebradas en París, cuna del Sistema Métrico Decimal, estableció definitivamente el Sistema Internacional de Medidas (SI), basado en 6 unidades fundamentales: metro, kilogramo, segundo, ampere, Kelvin, candela-, perfeccionado y completado posteriormente en las 12ª, 13ª y 14ª Conferencias, agregándose en 1971 la séptima unidad fundamental, la mole, que mide la cantidad de materia.
Los prefijos del SI son palabras empleadas para nombrar a los múltiplos y submúltiplos de cualquier unidad del Sistema Internacional, ya sean unidades básicas o derivadas.
Estos prefijos no pertenecen solamente al SI, muchos de ellos, así como la propia idea de emplearlos, son anteriores al establecimiento del Sistema Internacional en 1960; por lo tanto, se emplean a menudo en unidades que no pertenecen a este sistema. Los prefijos pertenecientes al SI los fija oficialmente la Oficina Internacional de Pesos y Medidas.
El S.I. establece y define 7 unidades fundamentales: metro (longitud), Kilogramo (masa), segundo (tiempo), ampere (intensidad de corriente eléctrica). Kelvin (temperatura termodinámica), candela (intensidad luminosa) y mol (cantidad de materia); y al menos 34 unidades derivadas.
Las unidades derivadas resultan en algunos casos de combinaciones de las unidades base con las que se relacionan matemáticamente con el valor $1$ (por ejemplo: $1 \; coulomb = 1 \; ampere x 1 \; segundo$), y en otros casos surgen de la combinación con otras unidades derivadas bajo el mismo tipo de relación (por ejemplo: $1 \; Pascal = 1 \; Newton/1 m^2$).
Las unidades fundamentales se definen en función de fenómenos físicos precisos y medibles, lo que confiere una máxima precisión y seguridad al sistema y permite no depender necesariamente de patrones de medida, con todas las inexactitudes de confección y duplicación que ello implica.
1. Los nombres de las unidades, así como de sus múltiplos y submúltiplos, se escriben con minúscula. El grado Celsius es una excepción.
2. Los símbolos que representan a las unidades se escriben con minúscula, excepto cuando proceden nombres propios. Se usa la letra mayúscula L para litro porque el 1 se confunde con l. Cuando un símbolo con dos letras procede de un nombre propio, la letra inicial es mayúscula. Por ejemplo $Pa$ (en honor a Blaise Pascal)
3. Los prefijos y submúltiplos se escriben con minúscula, excepto en el caso de mega y superiores.
4. Los símbolos nunca se escriben en plural, ni llevan punto final, salvo que estén al final de una frase.
5. Entre el número y el símbolo debe dejarse un espacio salvo en las medidas angulares.
6. Los productos de unidades se expresan o bien dejando un espacio entre los símbolos o bien dejando un espacio entre ellos.
Los prefijos SI representan estrictamente potencias de $10$. No deben utilizarse para expresar potencias de $2$ (por ejemplo, un kilobit representa $1000$ bits y no $1024$ bits). Los nombres y símbolos de los prefijos correspondientes a $210, 220, 230, 240, 250$ y $260$ son, respectivamente, $kibi, Ki$; $mebi, Mi$; $gibi, Gi$; $tebi, Ti$; $pebi, Pi$; y $exbi, Ei$. Así, por ejemplo, un kibibyte se escribe: $1 KiB = 210 B = 1024 B$, donde $B$ representa al byte. Aunque estos prefijos no pertenecen al SI, deben emplearse en el campo de la tecnología de la información a fin de evitar un uso incorrecto de los prefijos SI. Ver .
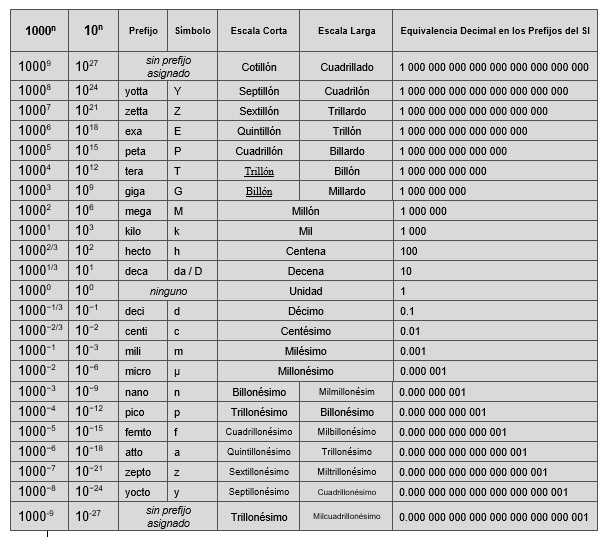
Se utiliza la notación científica cuando se trata con números muy grandes o muy pequeños. En la notación científica el número se expresa como el producto de dos números, el primero, está comprendido entre $1$ y $10$ y el otro es una potencia de diez con exponente entero y positivo cuando el punto decimal se corre a la izquierda y negativo cuando el punto decimal se corre a la derecha.

Si se tiene el número $0.00056 = 5.6 × 10^{- 4}$
Si se tiene el número $56000 = 5.6 × 10^4$
Al utilizar números escritos en notación científica para realizar operaciones matemáticas, es necesario tener en cuenta las siguientes reglas, ye que es necesario conocer cuántas cifras significativas tendrá el resultado:
1. En la multiplicación y la división el resultado tendrá el número de cifras significativas correspondiente al término con menor número de éstas que intervenga en la operación aritmética.
2. En la suma y la resta el resultado debe tener tantas cifras decimales como correspondan al menor número de cifras que contengan los sumandos, el minuendo o sustraendo de acuerdo a la operación que se esté efectuando.

1. Multiplicar $4.5$ por $1.21 = 5.445$, aplicando la regla, la respuesta correcta debe ser $5.4$.
2. Realizar la siguiente operación:
$$\frac{1.5 × 4.51}{5.141} = \frac{6.765}{5.141} = 1.3$$Realizar la sumas siguientes:
$$1.331 + 2.11 - 2.3 = 1.1$$Se considera que las cifras significativas de una medida son aquellos dígitos que tienen significado real o aportan alguna información. Las cifras no significativas aparecen como resultado de los cálculos y no tienen significado alguno. Las cifras significativas de un número vienen determinadas por su error.
Por ejemplo, consideremos una medida de longitud que arroja un valor de $5432,4764 m$ con un error de $0,8 m$. El error es por tanto del orden de décimas de metro. Es evidente que todas las cifras del número que ocupan una posición menor que las décimas no aportan ninguna información. En efecto, ¿qué sentido tiene dar el número con precisión de diezmilésimas si afirmamos que el error es de casi $1$ metro? Las cifras significativas en el número serán por tanto las que ocupan la posición de las décimas, unidades, decenas, etc., pero no las centésimas, milésimas y diezmilésimas.
Cuando se expresa un número debe evitarse siempre la utilización de cifras no significativas, es decir, siempre se deben tener en cuenta los dígitos confiables que se reportan al realizar la medición.
Para determinar el número de cifras significativas es conveniente tener en cuenta varias reglas que suelen ser de gran utilidad.
• Reglas para determinar el número de cifras significatiavas
1. Todos los dígitos distintos de cero son cifras significativas:
Ejemplo:
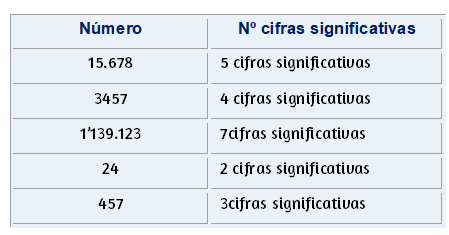
2. Los ceros que se encuentran antes o después del punto decimal, pero antes de dígitos distintos de cero NO son cifras significativas:
Ejemplo:
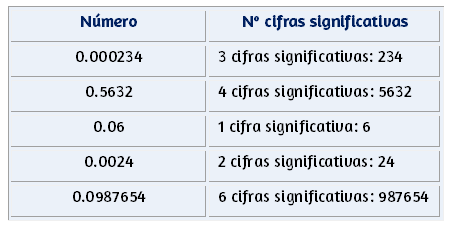
3. Los ceros son significativos cuando se encuentran:
a. Después del punto decimal y al final de un número.
b. Entre dígitos distintos de cero.
c. Al final de números enteros si la incertidumbre lo indica
d. Para número sin punto decimal, números enteros, $200 cm$, $40 m$, pueden tener una cifra significativa, el digito $2$, o el dígito $4$ respectivamente, no es posible saber cual es la cantidad correcta si no se tiene más información; sin embargo utilizando la notación científica se evita esta ambigüedad.
Ejemplo:
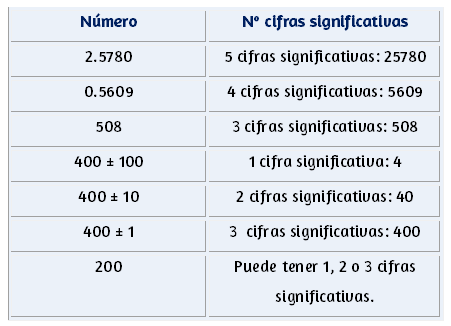
Puesto que en algún caso puede haber algo de confusión, los números deben redondearse de forma que contengan sólo cifras significativas. Se llama redondeo al proceso de eliminación de cifras no significativas de un número.
• Las reglas que emplearemos en el redondeo de números son las siguientes:
Redondear los siguientes números, aplicando las reglas respectivas:
Cuando se analizan mediciones y cifras significativas es conveniente distinguir entre exactitud y precisión. En términos de las medidas experimentales existe una distinción importante entre ellas. La EXACTITUD se refiere a cuán cercano está el valor medido al valor aceptado, de otra forma, puede expresarse como cuán cercana está una medición del valor real de la cantidad medida. La PRECISIÓN significa cuán cercanas están las medidas realizadas una de las otras, o lo que es lo mismo, cuanto concuerdan dos o mas mediciones de una misma cantidad. A mayor precisión, más cercanas son las medidas unas de las otras al repetirlas. Sin embargo, la precisión no implica exactitud.
Veamos la diferencia entre ambos conceptos en las figuras A, B y C. En ellas puede observarse que en la figura A, hay buena precisión y buena exactitud, en la figura B, puede observarse que el tirador cuenta con poca exactitud, ya que está muy alejado del punto central, pero sus tiros son muy cercanos unos de otros por lo que tiene buena precisión, En la C, se tienen tiradas que llegan al tablero muy alejadas unas de otras, por lo que este tirador cuenta con mala precisión y mala exactitud, como puede observarse en la siguiente figura Exactitud y precisión (crédito: Sepúlveda, E. (2016, mayo). Fricción. Recuperado de Física en Línea: http://www.fisicaenlinea.com/02medicion/medicion06-errorespersonales.html:
La precisión de una medición a menudo se expresa mediante la desviación promedio. Es decir, se calcula la diferencia entre cada resultado experimental y el resultado promedio. Se obtiene un promedio de estas diferencias expresando a cada una como cantidad positiva y los resultados del experimento se reportan como el valor promedio más o menos la desviación promedio.

• ¿Quién determina lo “aceptable?
Para saber si un resultado es exacto? En el caso de la masa, por ejemplo, los laboratorios nacionales de varios países tienen un kilogramo masa estándar. En Estados Unidos, el laboratorio es el del Instituto nacional de normas y tecnología (Nacional Institute for Standard and technology, NIST).
Los tamaños de las unidades básicas no siempre son los más útiles, si tratamos de medir una cancha de fútbol con un micrómetro tendríamos bastante trabajo, es por ello que requerimos de implementos de medida mayores, tal vez un decámetro. Al medir el diámetro de un cabello requerimos de un implemento de medida más fina tal vez hasta las centésimas de milímetro (mm).
Se cuenta con prefijos utilizando la palabra metro lo cual nos indica un factor de multiplicación si el prefijo defiende un exponente positivo o de división si el prefijo define un exponente negativo.
Para convertir magnitudes a unidades relacionadas por factores de escala se plantean equivalencias y su transformación obedece a un análisis dimensional donde se coloca en el numerador los datos de unidades en las cuales deseamos convertir y en el denominador las unidades que deseamos eliminar.
¡Evite transformar mediante reglas de tres! Esto no habla bien de un futuro ingeniero.
Es muy probable haber escuchado de niños esta vieja expresión: “No es posible sumar naranjas con bananos, ni huevos con yuca”, siempre se ha escuchado tengo 2 naranjas, tengo 4 bananos, compré 30 de huevos, es decir, siempre se está haciendo referencia a la misma unidad. Por lo que es necesario aprender la manera de convertir tanto las piñas como los mangos en una sola expresión, como, por ejemplo, compré tantas frutas y así resolver correctamente los problemas que incluyen diferentes unidades métricas.
Por lo general, los químicos y otras ciencias utilizan el análisis dimensional para llevar a cabo estas conversiones. Este método se basa en el desarrollo de una relación entre diferentes unidades que expresan la misma dimensión física. Por ejemplo, suponga que decide hacer guacamole para su almuerzo, va a la tienda más cercana y se entera que los aguacates cuestan $\$800$ cada uno, si únicamente cuenta con $\$1600$. ¿Cuántos aguacates puede comprar para preparar el guacamole?
Intuitivamente, con lo que usted ya sabe de matemática, responderá que podrá comprar dos aguacates (ya que ha dividido 1600 entre 800), pero aplicando el método de análisis dimensional para resolver el problema. Podemos expresar la relación entre pesos y el número de aguacates así:
$\$800 = 1 \textsf{aguacate}$
Si dividimos la ecuación entre $\$800$, tenemos:
$\dfrac{1 \textsf{ aguacate}}{\$800}$, esta expresión se llamará factor $A$
Ahora si se divide la ecuación, entre un aguacate, se tiene:
$\dfrac{\$800}{1 \textsf{ aguacate}}$, esta expresión se llamará factor $B$
Se podrá utilizar uno de estos factores $A$ o $B$ para resolver el problema. Pero, ¿Cuál se debe utilizar? Puesto que estamos buscando una respuesta en términos del número de aguacates, se requiere multiplicar la cantidad determinada ($\$1600$) por un factor tal que se cancele el signo $\$$. Así que el factor correcto es el factor $A$, que contiene los aguacates en el numerador y los pesos en el denominador, por lo tanto:
$1600 × \textsf{ factor } A =$ número de aguacates
$\$1600 × \dfrac{1 \textsf{ aguacate}}{\$800} = 2 \textsf{ aguacates}$
Ojo: si por error se hubiera elegido el factor $B$, el resultado habría realizado la siguiente operación:
$$\$1600 × \frac{\$800}{1 \textsf{ aguacate}} = \frac{\$1280000}{1 \textsf{ aguacate}},$$expresión que no corresponde a la pregunta original y da como resultado unidades sin sentido.
• Siempre que sea posible de aquí en adelante se utilizará el análisis dimensional para la solución de problemas, según el planteamiento de los siguientes seis pasos:
1. Lea primero el problema con mucha atención para determinar lo que realmente se pide.
2. Organice los datos asegurándose de incluir tanto las unidades de la cantidad determinada como las unidades de la cantidad desconocida.
3. Escriba las unidades de la cantidad determinada en el lado izquierdo de una línea. Escriba las unidades de la cantidad desconocida en el lado derecho de la línea.
4. Aplique el principio de análisis dimensional para desarrollar los factores, de manera que estos factores, utilizados adecuadamente, den las unidades correctas en la cantidad desconocida.
5. Verifique su respuesta para comprobar que sí es razonable, revisando tanto las operaciones matemáticas como las unidades.
6. por último, verifique el número de cifras significativas.

Convertir $3.85 m$ a milímetros.
Solución:
$3.85 m × \textsf{ un factor} = \textsf{milímetros}$
Se sabe que $1m = 1000 mm$, por tanto, los factores que se analizarán son los siguientes:
Un factor $A$ y un factor $B$, para así decidir cuál es el correcto en este caso:
Para obtener la respuesta correcta (milímetros), se debe utilizar el factor $A$, observe como las unidades del denominador del factor $A$ deben cancelarse con las unidades de la cantidad determinada (metros para este caso).
$\dfrac{1000 mm}{1 m}$, factor $A$ y $\dfrac{1m}{1000 mm}$, factor $B$.
El factor correcto a utilizar es el factor $A$:
$$3.85 m × \frac{1000 mm}{1m} = 3850 mm$$La respuesta debe ser expresada con tres cifras significativas, y $3.85$ tiene tres cifras significativas, que pueden expresarse con notación científica de la siguiente forma: $38.5 × 10^2 mm$.

Convertir 0.0055 litros a microlitros.
Solución:
Se sabe que $1L = 1000000$, $μL$, es decir: $(10^6) μL$, por lo tanto:
El factor a utilizar en este caso es: $\dfrac{1000000 μL}{1L}$,
entonces: $0.0055 L × \dfrac{1000000 μL}{1L} = 5500 μL$, o lo que es lo mismo, $5.5 10^3 × μL$

Expresar 5.6 días a microsegundos.
Solución:
Se sabe que un microsegundo, $(μs) = 10^{-6}$ segundos.
En este ejercicio se requieren varios factores de conversión, ya que es necesario convertir días a horas, horas a minutos, minutos a segundos y por último segundos a microsegundos, $μs$.
El factor para convertir días a horas: se sabe que un $\textsf{día} = 24 \textsf{ horas}$, por lo tanto el factor es: $\dfrac{24 \textsf{ horas}}{1 \textsf{ día}}$
El factor para convertir horas a minutos: se sabe que $1 \textsf{ hora} = 60 \textsf{ minutos}$, por lo tanto el factor es: $\dfrac{60 \textsf{ min}}{1 \textsf{ hora}}$
Para convertir minutos a segundos: se sabe que $1 \textsf{ min} = 60 \textsf{ segundos}$, por lo tanto el factor es: $\dfrac{60 \textsf{ s}}{1 \textsf{ min}}$
ahora solo falta convertir los segundos a microsegundos, utilizando el factor: $\dfrac{1 μs}{0.0000001}$
Así entonces la conversión de horas a microsegundos es:
$$5.6 \cancel{\textsf{ días}} × \frac{24 \cancel{\textsf{ h}}}{1 \cancel{\textsf{ día}}} × \frac{60 \cancel{\textsf{ min}}}{1 \cancel{\textsf{ h}}} × \frac{60 \cancel{\textsf{ s}}}{1 \cancel{\textsf{ min}}} × \frac{1μs}{0.0000001 \cancel{\textsf{ s}}} = 4.8 × 10^{12} μs$$
"El futuro está girando hacia la energía renovable porque se trata de un recurso ilimitado". Vivek Wadhwa.
Desde la Antigüedad se sabe que la materia está formada por partículas pequeñas llamadas átomos y moléculas, que dependiendo del estado en que se encuentre la materia, sus átomos o moléculas se hallan en mayor o menor grado de libertad. El grado de libertad depende de las fuerzas que existan entre los átomos o moléculas; si las moléculas se mueven es porque poseen energía bien sea potencial o cinética. De la misma manera que todas las personas que se encuentran alrededor de una fogata no experimentan el mismo grado de calor, tampoco todas las moléculas de un cuerpo tienen la misma energía; unas se mueven más rápido que otras, de tal manera que si queremos expresar de alguna forma la energía del cuerpo, tenemos que hacerlo mediante un valor que corresponda a la energía promedio de sus moléculas. Pues bien, el concepto que se puede deducir del ejemplo anterior es el de temperatura. La temperatura de un cuerpo se define como una magnitud que mide la energía promedio de las moléculas que constituyen ese cuerpo. La temperatura de un cuerpo es independiente de su masa, porque solo depende de la velocidad y la masa de cada una de sus moléculas. De otra parte, el concepto de calor corresponde a la medida de la energía que se transfiere de un cuerpo a otro debido a la diferencia de temperatura que existe entre ellos.
Aunque la energía es un concepto familiar, es difícil definirlo de manera precisa.
Para propósitos de este libro se definirá la energía como la habilidad para realizar trabajo o transferir calor. Enseguida se definirán estos términos.La energía puede clasificarse como potencial o cinética.
Es la energía que mide la capacidad que tiene dicho sistema para realizar un trabajo en función exclusivamente de su posición o configuración.
Puede pensarse como la energía almacenada en el sistema, o como una medida del trabajo que un sistema puede entregar.
Por ejemplo, el agua detrás de una presa tiene energía potencial que puede convertirse en trabajo cuando el agua fluye a través de las turbinas creando electricidad. Las fuerzas de atracción y repulsión también conducen a la energía potencial. La energía liberada cuando se quema la gasolina resulta de las diferencias en las fuerzas de atracción entre el núcleo y los electrones en los reactivos y productos.
La $Ec$ de un objeto es la energía debida al movimiento del objeto y depende de su masa $m$ y de su velocidad, y el cálculo de ésta se efectúa mediante la expresión:
$$Ec = \frac{1}{2} m \cdot v^2$$Podemos observar que cuando la $V = 0$, esta condición sirve como referencia real para el valor cero de la energía cinética.
La cantidad de trabajo que un cuerpo en movimiento puede realizar depende de la masa y de la velocidad que posee, por ejemplo dos cuerpos de igual masa y diferente velocidad al chocar contra otro producen distintos efectos, es decir, hay trabajo.
Una bala en su trayectoria, un viento fuerte, el agua al fluir, una persona cuando está desplazándose, son ejemplos de cuerpos que poseen energía cinética.
Una de las características más importantes de la energía radica en que se conserva.
La ley de conservación de la energía enuncia que la energía puede convertirse de una forma en otra pero no puede ser creada ni destruida. Es decir, la energía del universo es constante.
Tradicionalmente, los cambios de energía que acompañan las reacciones químicas se han expresado en calorías, una unidad que no pertenece al SI.
Una caloría, originalmente se definió como la cantidad de calor necesario para que la temperatura de $1g$ de H2O se incremente $1°C$, entre $14.5°C$ y $15.5°C$ (el calor específico del H2O en ese intervalo de temperatura es igual a $1$).
Hoy día se lo define en términos del Joule: una caloría es $4,184$ Joules o (Julios)
$1kcal$ $4,184 kJ$
$1cal$ $4, $184 J$
$1kcal = 1.103 cal = 4, 184.10^3 J$
De aquí, que un Joule expresado en calorías, pueda requiera la siguiente conversión:
$$1J = \frac{1}{4,184} cal = 0,239 cal$$Experimentalmente se ha demostrado, que siempre que una cantidad definida de cualquier forma de energía se convierte en calor, se produce un número definido de calorías. Esto se conoce como Equivalente Mecánico del Calor, y establece que cuando un joule de energía se transforma en calor, siempre se produce $0,239 cal$.
Principio de Conservación de la Energía: experimentalmente se comprobó que la energía involucrada en todo proceso químico, después de ocurrido el cambio, aparece de alguna forma.
Este principio expresa que la energía no puede crearse ni destruirse en una reacción química o proceso físico, solo puede convertirse de una forma a otra (Primera Ley de la Termodinámica).
Podemos decir que la cantidad combinada de materia y energía en el universo, es una constante.
Ahora bien, si nos remontamos a la época del inicio de la era nuclear 1914, cuando los científicos se dieron cuenta que la materia puede convertirse en energía, pues hay una equivalencia entre la energía y la masa de un sistema material, la que está dada por la ecuación de Einstein:
De esta expresión deducimos que la masa y la energía del objeto son proporcionales, y la constante de proporcionalidad es la velocidad de la luz, entonces, según el principio de equivalencia entre masa y energía de Einstein, tenemos que.
Hablando en términos de variaciones, lo que denotamos como $(Δ)$ tenemos $ΔE α Δm = \textsf{constante} \to \frac{ΔE}{Δm} = c^2$, así entonces, $ΔE = Δm × c^2$.
Por tener $c$ un valor tan elevado y estar además elevado al cuadrado en la expresión matemática, los pequeños cambios de masa, van acompañados de grandes cambios de energía.
Si en una reacción se libera cierta cantidad de energía, el sistema material pierde una cantidad de masa proporcional a la energía liberada. Esto significa, que si un sistema pierde masa, es porque el proceso es exotérmico. Por el contrario, si en una reacción se absorbe una determinada cantidad de energía, la masa del sistema aumenta en una cantidad equivalente a la energía absorbida.
En todo proceso endotérmico, el sistema gana masa. ¿Qué nombre recibe este tipo de reacción?, ¿qué se destruye cuando esta ocurre?
El calor es otra forma de energía, al igual que la energía cinética o la potencial, pero también puede considerarse como la manifestación a escala microscópica de la energía cinética y potencial de las moléculas.
En el desplazamiento de calor se presenta transmisión de energía, es decir, movimiento por choque entre las partículas. Cuando un cuerpo caliente choca con otro con menor cantidad de calor, este último gana velocidad en el movimiento de sus partículas a tiempo que reduce la velocidad de movimiento de las partículas del cuerpo caliente de, esto explica por qué el calor se transmite de un cuerpo más caliente a uno de menor calor esto explica por qué el calor se transmite de un cuerpo más caliente a uno de menor calor hasta que ambos se encuentren a la misma temperatura.
Tradicionalmente la energía calórica se mide en calorías. pero recordemos que en el SI el patón de medida es el Joule, y para medir grandes cantidades de calor se emplea la kilocaloría o caloría grande, que es igual a $1000$ calorías.
Una propiedad de la materia es que requiere una cierta cantidad de calor para producir un cambio en la temperatura, por unidad de masa de una sustancia determinada. A esto se le denomina calor específico de una sustancia.
El calor específico se define como el número de joules requeridos para elevar la temperatura de $1.00 kg$ de una sustancia a $1.00 K$, o el número de calorías necesario para elevar la temperatura de $1.00 g$ de una sustancia en $1.00°C$.
$$\textsf{Calor específico} = \frac{\textsf{Joules}}{kg × K} \; \textsf{ o } \; \frac{\textsf{calorías}}{g × °C} \tag{4.3}$$La siguiente interactividad, muestra diferentes cambios y formas de energía.
Esta simulación ha sido diseñada por PHETtempFX, Universidad de Colorado. https://phet.colorado.edu/sims/html/energy-forms-and-changes/latest/energy-forms-and-changes_en.html OpenStax Chemistry
Simulación, diferentes cambios y formas de energía.

Calcule el número de joule necesarios para elevar la temperatura de $250g$ de aluminio sólido de $373$ a $473 K$.
Solución
Para iniciar la solución, es necesario conocer el calor específico del aluminio, dato que se encuentra tabulado, y es igual a $0.217 cal/g \cdot °C$ o $9.08 × 10^3 joule/kg \cdot K$.
$$\frac{9.08 × 10^3 J}{1 \cancel{kg} \cdot K} × \frac{1 \cancel{kg}}{1000 \cancel{g}} × 250 \cancel{g} × (473 - 373)K = 227 × 10^3 J$$La siguiente ecuación, sirve para calcular el calor cedido o absorbido por un cuerpo :
$$Q = m × c_e × T = m × c_e × (T_f - T_i) \tag{4.4}$$
Un recipiente de aluminio de $2,5 Kg$ contiene $5 Kg$ de agua a la temperatura de $28 °C$. Qué cantidad de calor se requiere para elevarles la temperatura hasta $80 °C$.
Solución
Aluminio
$m_1 = 2,5kg = 2500g$
$T_1 = 28°C$
$T_f = 80°C$
$c_e = 0.21 \frac{cal}{g \cdot °C}$
$Q_1 = m_1 × c_e × (T_f - T_1)$
$Q_1 = 525 × (52) \textsf{calorías}$
$Q_1 = 27.300 \textsf{calorías}$
Agua
$m_2 = 5kg = 5000g$
$T_1 = 28°C$
$T_f = 80°C$
$c_e = 1 \frac{cal}{g \cdot °C}$
$Q_2 = m_2 × c_e × (T_f - T_1)$
$Q_2 = 5000g × \frac{1 cal}{g \cdot °C}$
$× (80°C - 28°C)$

"La suprema realidad de nuestro tiempo es la vulnerabilidad de nuestro planeta" John F. Kennedy.

“Un objeto no resulta de la pluralidad de los átomos, sino de la combinación de los átomos deviene cada objeto.” [Fuente: Simplicio, Comentarios a Aristóteles.] Demócrito


Antes de 1800, se pensaba que la materia era continua, es decir que podía ser dividida en infinitas partes más pequeñas sin cambiar la naturaleza del elemento. Sin embargo, cerca de 1803 ganó aceptación la teoría de un científico inglés llamado John Dalton, hacia 1766-1844.
Al dividir una muestra de cobre en trozos cada vez más pequeños, finalmente se encuentra una unidad básica que no puede ser dividida sin cambiar la naturaleza del elemento. Esta unidad básica se llama Átomo. Un átomo es la partícula más pequeña que puede existir de un elemento conservando las propiedades de dicho elemento.
Seguidamente, haremos referencia a los diferentes modelos atómicos, iniciando con la visión de Demócrito:
Demócrito, hacia el año 400 a. C., sugirió que toda la materia estaba formada por partículas minúsculas, indivisibles, a las cuales les dio el nombre de átomos. Sus ideas fueron rechazadas durante 2000 años, pero a finales del siglo dieciocho se retoma su teoría y de le da una luz de aceptación.
Hacia 1808, el maestro de escuela inglés, John Dalton, publicó las primeras ideas modernas acerca de la existencia y naturaleza de los átomos. Resumió y amplió los vagos conceptos de antiguos filósofos y científicos. Esas ideas forman la base de la Teoría Atómica de Dalton, con la que logró revolucionar la química con su hipótesis de que el comportamiento de la materia podría explicarse, utilizando la teoría atómica, siendo publicada por primera vez en 1807, sus hipótesis de sobre las características microscópicas de la materia, las que siguen siendo válidas en la teoría atómica moderna.
Estos son los postulados de la teoría atómica de Dalton:
1. La materia está compuesta de partículas extremadamente pequeñas llamadas átomos. Un átomo es la unidad más pequeña de un elemento que puede participar en un cambio químico.
2. Un elemento consta de un solo tipo de átomo, que tiene una masa que es característica del elemento y es el lo mismo para todos los átomos de ese elemento (). Una muestra macroscópica de un elemento contiene un increíblemente gran número de átomos, todos los cuales tienen propiedades químicas idénticas.
3. Los átomos de un elemento difieren en las propiedades de los átomos de todos los demás elementos.
4. Un compuesto consiste en átomos de dos o más elementos combinados en una pequeña proporción de números enteros. En un compuesto dado, la cantidad de átomos de cada uno de sus elementos están siempre presentes en la misma proporción. ()

5. En las reacciones químicas los átomos se separan o se unen; pero ningún átomo se crea ni se destruye, y ningún átomo de un elemento se convierte en átomo de otro elemento

La teoría atómica de Dalton explica la ley de la conservación de la masa, al establecer, que durante una combinación química, los átomos de los elementos no se crean ni se destruyen. Es así que los átomos que forman los reactivos será el mismo de los productos.
Como Dalton conocía los experimentos del químico francés Joseph Proust, quien demostró que todas las muestras de un compuesto puro contienen los mismos elementos en la misma proporción en masa.lo que se conoce como la ley de la definición o proporción constante. Esto sugiere que los números de átomos de los elementos en un determinado compuesto siempre existe en la misma proporción. Por ejemplo es, cuando diferentes muestras de isooctano (un componente de la gasolina y uno de los estándares utilizados en el sistema de clasificación de octano) se analizan, se encuentra que tienen una relación de masa de carbono a hidrógeno de $5.33:1$, como se muestra en la .

Vale la pena señalar que aunque todas las muestras de un compuesto particular tienen la misma relación de masa, pero las muestras que tienen la misma relación de masa no son necesariamente la misma sustancia. Por ejemplo, hay muchos otros compuestos además del isooctano que también tienen una relación de masa de carbono a hidrógeno de $5.33:1.00$.
Dalton también usó datos de Proust, así como los resultados de sus propios experimentos, para formular otra ley interesante. La ley de las proporciones múltiples, la que establece que cuando dos elementos reaccionan para formar más de un compuesto, una masa fija de un elemento reaccionará con las masas del otro elemento en una proporción de números enteros pequeños. Por ejemplo, cobre y el cloro puede formar un sólido verde y cristalino con una relación de masa de $0.558 g$ de cloro a $1 g$ de cobre, así como un sólido marrón cristalino con una relación de masa de $1.116 g$ de cloro por $1 g$ de cobre. Estas razones por sí mismas pueden no parecer particularmente interesantes o informativas; sin embargo, si tomamos una proporción de estas relaciones, obtenemos una información útil y posiblemente un resultado sorprendente: una pequeña proporción de números enteros.
Otro ejemplo serían el CO y CO2, según los postulados de Dalton, en el CO2 existen dos veces más átomos de oxígeno por átomo de carbono que en el CO. El monóxido de carbono tiene un átomo de oxígeno por cada átomo de carbono, mientras que el CO2 tiene dos átomos de oxígeno por cada átomo de carbono. Según las matemáticas, se puede afirmar que la relación de átomos de oxígeno del CO con respecto al CO2 es $1:2$, que representan números enteros sencillos.
Esta relación de $2$ a $1$ significa que el compuesto marrón tiene el doble de cloro por cantidad de cobre que el compuesto verde, de la
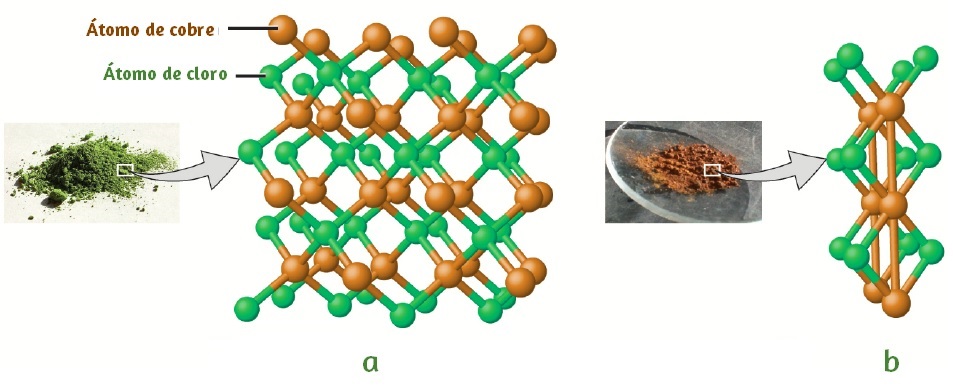
En ese tiempo algunos de sus postulados no pudieron verificarse experimentalmente, ya que se basaron en limitadas observaciones experimentales de su época.
Aún con sus limitaciones, los postulados de Dalton constituyen un marco de referencia que posteriormente los científicos pudieron modificar o ampliar. Por esta razón se considera aDalton como el padre de la Teoría Atómica Moderna.
En 1803, Dalton publicó su primera lista de pesos atómicos relativos para cierta cantidad de sustancias. Esto, unido a su rudimentario material, hizo que su tabla fuese poco precisa. Por ejemplo, creía que los átomos de oxígeno eran $5,5$ veces más pesados que los átomos de hidrógeno, porque en el agua midió $5,5$ gramos de oxígeno por cada gramo de hidrógeno y creía que la fórmula del agua, en estado gaseoso, era HO (en realidad, un átomo de oxígeno es $16$ veces más pesado que un átomo de hidrógeno).
Su propuesta, que incluía 36 elementos, consistía en círculos que contenían símbolos (como una cruz para el sulfuro) o letras (la "C" para el cobre).

El video presenta el desarrollo de la teoría atómica de Dalton.
En 1898, el ingles Joseph John Thomson propuso un modelo para la estructura del átomo al que llamaron “budín de pasas”. Thomson estableció la hipótesis, de que los átomos estaban formados por una esfera de carga eléctrica positiva distribuida de manera uniforme, en cuyo interior se encontraban los electrones en movimiento en cantidad de igual al número de las cargas positivas para que el átomo fuera neutro.
Posteriormente, el descubrimiento de nuevas partículas y los experimentos llevados a cabo por Rutherford demostraron la inexactitud de tales ideas.

Pero antes de ello, en 1897, se creía que los átomos eran la división más pequeña de la materia, cuando J.J Thomson descubrió el electrón mediante su experimento con el tubo de rayos catódicos. El tubo de rayos catódicos que usó Thomson era un recipiente cerrado de vidrio, en el cual los dos electrodos estaban separados por un vacío. Cuando se aplica una diferencia de tensión a los electrodos, se generan rayos catódicos, que crean un resplandor fosforescente cuando chocan con el extremo opuesto del tubo de cristal. Mediante la experimentación, Thomson descubrió que los rayos se desviaban al aplicar un campo eléctrico (además de desviarse con los campos magnéticos, cosa que ya se sabía). Afirmó que estos rayos, más que ondas, estaban compuestos por partículas cargadas negativamente a las que llamó "corpúsculos" (más tarde, otros científicos las llamaron electrones).
Thomson creía que los corpúsculos surgían de los átomos del electrodo. De esta forma, estipuló que los átomos eran divisibles, y que los corpúsculos eran sus componentes. Para explicar la carga neutra del átomo, propuso que los corpúsculos se distribuían en estructuras anilladas dentro de una nube positiva uniforme; éste era el modelo atómico de Thomson o "modelo del plum cake"
El modelo atómico de Thomson fue refutado por Ernest Rutherford, quien descubrió que la mayor parte de la masa y de la carga positiva de un átomo estaba concentrada en una fracción muy pequeña de su volumen, que suponía que estaba en el mismo centroDescubrimiento del núcleo (crédito: Núñez González, Claudia. (s.f). Recuperado en: https://upload.wikimedia.org/wikipedia/commons/6/62/LIBRO_TEXTO_IPP_QUIMICA.pdf.
En su experimento, Geiger y Marsden bombardearon partículas alfa a través de una fina lámina de oro (que chocarían con una pantalla fluorescente que habían colocado rodeando la lámina). Dada la mínima como masa de los electrones, la elevada masa y momento de las partículas alfa y la distribución uniforme de la carga positiva del modelo de Thomson, estos científicos esperaban que todas las partículas alfa atravesasen la lámina de oro sin desviarse, o por el contrario, que fuesen absorbidas. Para su asombro, una pequeña fracción de las partículas alfa sufrió una fuerte desviación. Esto indujo a Rutherford a proponer el modelo planetario del átomo, en el que los electrones orbitaban en el espacio alrededor de un gran núcleo compacto, a semejanza de los planetas y el Sol.
E. Rutherford realiza en 1911 un experimento crucial con el que trataba de comprobar la validez del modelo atómico de Thomson, ya que mantiene que el átomo se compone de una parte positiva y una negativa, pero la diferencia es que postula que la parte positiva se concentra en un núcleo, el cual también contiene virtualmente toda la masa del átomo, mientras que los electrones se ubican en una corteza orbitando al núcleo en órbitas circulares o elípticas con un espacio vacío entre ellos.
Rutherford predijo la existencia del neutrón en el año 1920, por esa razón en el modelo de Thomson no se menciona éste.
Sin embargo, el modelo atómico de Rutherford presentaba varias incongruencias, ya que contradecía las leyes del electromagnetismo de James Clerk Maxwell, las cuales estaban comprobadas mediante datos experimentales. Según las leyes de Maxwell, una carga eléctrica en movimiento (en este caso el electrón) debería emitir energía constantemente en forma de radiación y llegaría un momento en que el electrón caería sobre el núcleo y la materia se destruiría. Todo ocurriría muy brevemente. No explicaba los espectros atómicos.
El experimento de Rutherford, también llamado "experimento de la lámina de oro", fue realizado por Hans Geiger y Ernest Marsden en 1909, bajo la dirección de Ernest Rutherford en los Laboratorios de Física de la Universidad de Manchester. Los resultados obtenidos y el posterior análisis tuvieron como consecuencia la rectificación del modelo atómico de Thomson y la propuesta de un modelo nuclear para el átomo.
El experimento, Consistían básicamente en bombardear una lámina metálica delgada, aproximadamente de un grosor de $1 µm$, con unas partículas que el propio Rutherford había identificado en la década anterior, cuando realizaba diversos experimentos para determinar la naturaleza de estas partículas, hallando que el ratio carga - masa es es idéntico al de los átomos de helio doblemente ionizados. pero, sí estaba claro que tenía carga y que era muy pequeña. Para el experimento se consiguió un haz de partículas $α$ a partir de la desintegración del radio. Colocando este elemento radiactivo en una caja de plomo (el plomo detiene todas las partículas $α$) con un diminuto orificio practicado en la caja por el que salían las partículas se consiguió que el haz fuera muy fino.
Perpendicular a la trayectoria del haz se interponía el blanco seguida de una pantalla móvil cubierta con sulfuro de zinc. Cada vez que una partícula $α$ choca con la pantalla se producen pequeños destellos, los cuales eran visibles mediante un microscopio colocado en la parte trasera de la pantalla.
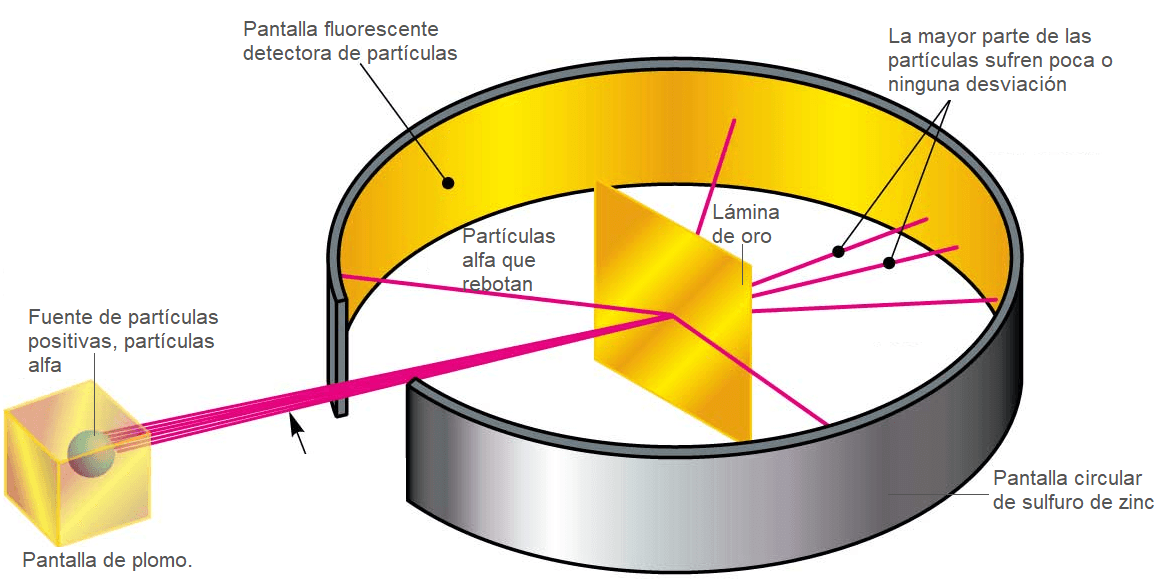
Todo el aparato estaba colocado dentro de una cámara en vacío para evitar que las partículas $α$ se vieran dispersadas por el aire.
Según el modelo atómico de Thomson, cada partícula debería atravesar la lámina metálica tras múltiples interacciones con los átomos por efecto de la fuerza de Coulomb, cada una de las cuales no desviaría apreciablemente su trayectoria, ya que la carga positiva y los electrones del átomo se encontrarían dispersos de forma homogénea en todo el volumen del átomo en todo el volumen del átomo, teniendo en cuenta que el ángulo máximo $θ_{\textsf{max}}$ que se puede desviar una partícula α por la interacción con un electrón es $θ_{\textsf{max}} ≈ 5 x 10^{-5} rad$, mientras que por la interacción con la carga positiva, que da un resultado de $θ_{\textsf{max}} ≈ 10^{-4}$.
Aquí se toma a $R$ como el radio atómico (típicamente, $10^{-10} m$), $v$ la velocidad de la partícula $α$ (usualmente $2 × 10^7 ms^{-1}$) y $m_α$.
Sin embargo, estos experimento mostraron que aunque un alto porcentaje de partículas atravesaban la lámina sin sufrir una desviación significativa, un reducido número de ellas era desviado incluso a ángulos de difusión de $180$ grados (aproximadamente una de cada 8000 se desvía hacia la fuente radiactiva para una lámina de platino). Parafraseando a Rutherford, "es como si le disparas balas de cañón a un pañuelo y rebotasen hacia ti"Teoría atómica de Rutherford.(crédito: Álvarez Alonso, Pablo. (2014, mayo). Capítulo 1.La teoría atómica de E. Rutherford. Recuperado en: https://www.researchgate.net/publication/216849222_La_teoria_atomica_de_Ernest_Rutherford.
Rutherford se dio cuenta de que se podía explicar de manera cualitativa la existencia de partículas rebotadas en sentido opuesto al que se emiten si se asume una disminución de varios órdenes de magnitud del tamaño de la distribución de las cargas positivas, lo que llevó a Rutherford a proponer su modelo atómico.
Este modelo se basa en la existencia de un núcleo atómico en el que se localiza la carga positiva, y por tanto la casi totalidad de la masa atómica, y una corteza formada por los electrones, en cantidad suficiente para que el átomo sea eléctricamente neutro. Para evitar que la atracción entre el núcleo y los electrones produjera el colapso del átomo (y por ello volvería a ser de tipo Thompson). Rutherfor propuso que los electrones se encontraban girando alrededor del núcleo en órbitas circulares con radios del orden del tamaño atómico. La fuerza central en este modelo sería de tipo coulombiano, y tendría el mismo papel que la fuerza gravitatoria en el caso de los planetas y el sol, de ahí que este modelo sea conocido como modelo planetario. Al igual que en el Sistema Solar, la mayor parte de este átomo estaría vacía, por lo que los electrones no tendrían ningún obstáculo a su paso, ni tampoco las partículas $α$. Teoría atómica de Rutherford.(crédito: Álvarez Alonso, Pablo. (2014, mayo). Capítulo 1.La teoría atómica de E. Rutherford. Recuperado en: https://www.researchgate.net/publication/216849222_La_teoria_atomica_de_Ernest_Rutherford
El electrón del átomo de Rurherford modificaba su dirección lineal continuamente, ya que seguía una trayectoria circular. Por lo tanto, debería emitir radiación electromagnética y esta radiación causaría la disminución de la energía del electrón, que en consecuencia debería describir una trayectoria en espiral hasta caer en el núcleo. El modelo de Rutherford fue sustituido por el de Bohr unos años más tarde.
Con las informaciones que disponía y de las obtenidas de su experiencia, Lord Rutherford propuso en el 1911 este modelo de átomo:
a. El átomo está constituido por una zona central, a la que se le llama núcleo, en la que se encuentra concentrada toda la carga positiva y casi toda la masa del núcleo.
b. Hay otra zona exterior del átomo, la corteza, en la que se encuentra toda la carga negativa y cuya masa es muy pequeña en comparación con la del átomo. La corteza.
c. Está formada por los electrones que tenga el átomo.
d. Los electrones se están moviendo a gran velocidad en torno al núcleo.
e. El tamaño del núcleo es muy pequeño en comparación con el del átomo (unas 100.000 veces menor)
f. El neutrón fue propuesto también por Rutherford en 1920, siendo identificado por J. Chadwick en 1932 como producto de la reacción nuclear producida al bombardear núcleos de berilio con partículas alfa.
 James Clerk Maxwell, (1831 -1879), apoyándose en trabajos anteriores de Oersted, Faraday y Ampere, que relacionaban electricidad y magnetismo, dio forma matemática a la teoría electromagnética durante la década de 1860. Dicha teoría predecía la existencia de ondas electromagnéticas.
James Clerk Maxwell, (1831 -1879), apoyándose en trabajos anteriores de Oersted, Faraday y Ampere, que relacionaban electricidad y magnetismo, dio forma matemática a la teoría electromagnética durante la década de 1860. Dicha teoría predecía la existencia de ondas electromagnéticas.
El hecho de que las ondas electromagnéticas se propagaran con idéntica velocidad que la luz llevó a la consideración de que la luz misma no es más que una onda electromagnética. La teoría de Maxwell unificaba así óptica y electromagnetismo.
Existen una gran variedad de ondas electromagnéticas que van desde los rayos gamma, muy energéticos y fuertemente ionizantes (son capaces de arrancar electrones de los átomos produciendo iones), hasta las ondas de radio en el extremo opuesto del espectro.
Hertz confirmó en 1888 la predicción de Maxwell al generar y recibir ondas electromagnéticas en el laboratorio.
El modelo de átomo planetario propuesto por Rutherford mostró pronto algunos inconvenientes teóricos que lo hacían inviable:
Un electrón al girar en círculos alrededor del núcleo debería emitir, por tanto, ondas electromagnéticas. Dicha emisión provocaría una pérdida de energía que haría que el electrón describiera órbitas de radio decreciente hasta caer sobre el núcleo. El modelo atómico de Rutherford era, por tanto, inviable desde el punto de vista de la física clásica.
Pronto se concluyó que la emisión de luz podría deberse a que los electrones absorbían energía de la corriente eléctrica y saltaban a órbitas superiores para, a continuación, volver a caer a las órbitas más próximas al núcleo emitiendo el exceso de energía en forma de energía luminosa.
Esta interpretación conducía, sin embargo, a afirmar que los espectros deberían de ser continuos, ya que al existir órbitas de cualquier radio (y energía) todos los saltos son posibles. La experiencia, por el contrario, mostraba que los espectros de los átomos son discontinuos. Constan de rayas de diversos colores sobre un fondo negro.Modelo atómico de Bohr-Sommerfeld. FisQuiweb(12/01/2020). Recuperado en: https://fisquiweb.es/Apuntes/Apuntes2Qui/Bohr_Sommerfeld.pdf
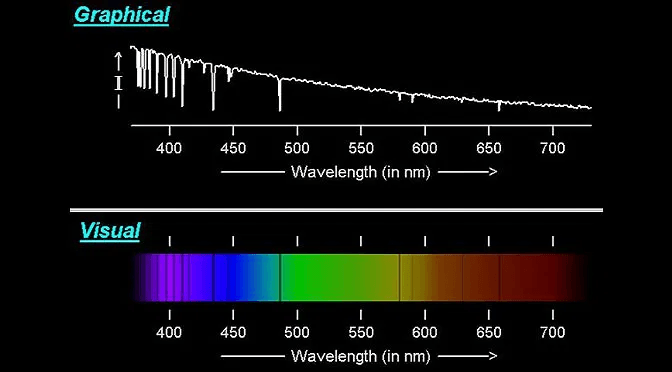
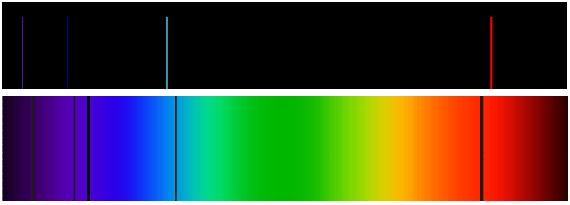
En 1886, Goldstein utilizó un tubo de rayos catódicos con un cátodo perforado y observó unos rayos que iban en sentido opuesto a los rayos catódicos, es decir, salían del ánodo ($+$) y se movían hacia el electrodo negativo o cátodo.
Estos rayos positivos eran desviados por campos eléctricos y magnéticos, lo que demuestra su naturaleza eléctrica, aunque de signo contrario a la de los rayos catódicos.
La relación carga/masa de las partículas positivas sí depende del tipo de gas encerrado en el tubo.
Si el gas era hidrógeno cada partícula positiva tenía una masa 2000 veces mayor que la del electrón y por tanto prácticamente igual a la del átomo de H. Su carga ($+$) igual a la del electrón.
La partícula ($+$) se identificó con el ión H$+$ y Ernest Rutherford le llamó protón y en 1919 a través de reacciones como: 7N14 + partícula $α →$ 8O16 + 1H1
Siempre aparecía el núcleo de Hidrógeno (H$+$).
Independiente de si era Nitrógeno (N) u otro núcleo, por ejemplo, oro, Flúor, Neón, Sodio…, se concluyó que el núcleo de Hidrógeno era uno de los componentes fundamentales de todos los núcleos: el protón.
Con el descubrimiento del protón, surgió la pregunta: ¿cuál es la estructura del núcleo? ¿cómo pueden permanecer los protones, siendo cargas del mismo signo, en un espacio tan reducido?
En 1920, Rutherford sugirió la existencia de otra partícula sin carga a la que llamó neutrón. Entre protones y neutrones existirían fuerzas atractivas de una nueva naturaleza (fuerzas nucleares) que superaban a las fuerzas de repulsión eléctricas.
J. Chadwick, 1932, bombardeó berilio con partículas α y detectó por primera vez a los neutrones ya predichos en 1920 por Rutherford.
Las partículas fundamentales constituyentes del átomo descubiertas hasta ese momento se presentan en la :
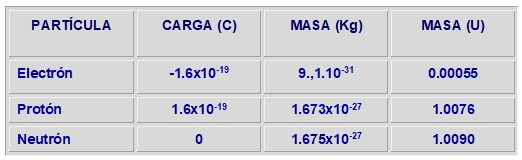
Corresponde número de protones que tiene un átomo y se representa con Z. Como los átomos son neutros, Z nos indica en cierto modo el número de electrones.
Se representa con N al número de neutrones que tiene un átomo.
La suma del número de protones y neutrones se denomina número másico (A).
Según este modelo, en valor absoluto la carga del protón y la del electrón coincide. Al número de protones en el núcleo se le denominó "número atómico" (Z), el cual coincide con el número de electrones en el caso de un átomo eléctricamente neutro, es decir, en el caso de que el átomo no sea un ión; ya que se denomina ión al átomo cargado eléctricamente como consecuencia de la pérdida o ganancia de uno o varios electrones.
No se debe olvidar, que:
El número atómico es el número de protones que tiene un átomo y se representa con Z. Como los átomos son neutros, Z nos indica en cierto modo el número de electrones.
Por tanto:
$$\textsf{Número de protones} = \textsf{Número de electrones}$$Se representa con N al número de neutrones que tiene un átomo. La suma del número de protones y neutrones se denomina Número Másico (A). La suma del número de protones y neutrones se denomina Número Másico (A).

Simbólicamente para cada núcleo de un determinado elemento el número atómico y el número de protones se representaría así:
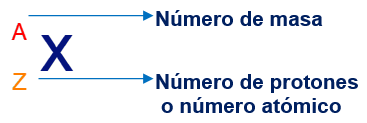
Cada elemento químico se caracteriza porque tiene un Z (número atómico) diferente, es decir, un número de protones diferentes. Si nos fijamos en la tabla periódica, los elementos químicos están ordenados según su número atómico, Z. Al ir sumando un protón vamos pasando de un elemento a otro.
• ¡NO debes olvidar!
Que el átomo posee un núcleo, donde se localizan los protones y los neutrones que son las partículas subatómicas de mayor masa. En el núcleo se concentra prácticamente toda la masa del átomo. El núcleo de un átomo tiene un diámetro de aproximadamente $1.10-14 m$, esto es, un tamaño aproximadamente $10.000$ veces menor que el tamaño atómico. Los electrones se encuentran en la parte exterior del átomo, rodeando al núcleo, y se mueven en regiones definidas del espacio llamadas orbitales; los electrones son 1838 veces más livianos que los protones.
• Además, No debes olvidar que Z determina el elemento químico del que se está hablando. Así, un átomo que tenga número atómico 3, es decir, será siempre Litio.
Pero podría suceder que haya varios átomos diferentes, pero todos ellos con un protón en su núcleo, a ello, nos preguntaríamos: ¿Qué elemento sería? La respuesta es que todos serían Hidrógeno, ya que como se ha dicho, el número atómico determina el elemento que se trata, ahora, es importante tener en cuenta que, quizá la diferencia entre dichos átomos estribe en el número de neutrones. Cada una de estas especies, que son diferentes, pero que todas son el elemento hidrógeno, se llaman isótopos .
• El número Z se puede leer directamente de tu tabla periódica y el número A se puede estimar con el número atómico $+$ el número de neutrones. El valor de N se tendrá que calcular.
Por ejemplo, para el caso del oro (Au), de la tabla periódica sabemos que $Z = 79$ y que la masa atómica es de $196,967$; por lo tanto: $A = 197$ y $n = 118$.
Átomos de un mismo elemento que poseen el mismo número atómico (igual número de protones), pero distinto número másico; es decir diferente número de neutrones en su núcleo. Por ejemplo, el hidrógeno normal tiene un protón en el núcleo con un electrón girando alrededor se le conoce por ese motivo como protio, existe otro isótopo del hidrógeno el deuterio, que tiene un neutrón por lo tanto, si tiene un protón y un neutrón su número másico es 2, pero su número atómico sigue siendo 1, hay otro isótopo del hidrógeno, el tritio, que tiene número másico 3: posee dos neutrones y un protón.
• Usos de los isótopos
Ellos son utilizados en: Vacunas. Se han elaborado radio vacunas para combatir enfermedades parasitarias del ganado y que afectan la producción pecuaria en general.
a. Medicina Nuclear. Se ha extendido el uso de radiaciones y de radioisótopos en medicina como agentes terapéuticos y de diagnóstico. En el diagnóstico se utilizan radiofármacos para diversos estudios como: Tiroides, Hígado, Riñón, Metabolismo, Circulación sanguínea, Corazón, Pulmón. En Terapia médica con técnicas nucleares se pueden combatir ciertos tipos de cáncer. Con frecuencia se utilizan tratamientos en base a irradiaciones con rayos gamma provenientes de fuentes de Cobalto-60.
b. Radioinmunoanálisis. Es un método de gran sensibilidad utilizado para realizar mediciones de hormonas, enzimas, virus de la hepatitis.
c. Radiofármacos. Se administra al paciente un cierto tipo de fármaco radioactivo que permite estudiar mediante imágenes bidimensionales o tridimensionales (tomografía) el estado de diversos órganos del cuerpo humano.

Para cada uno de los átomos indicados, identifique el número de protones, ($p+$), electrones, ($e-$) y neutrones, (N). Identifique también a qué elemento pertenecen:
a) $_{30}^{60} X$
b) $_{13}^{27} X$
c) $_{20}^{40} X$
d) $_{19}^{39} X$
• Solución
Según la notación, en la parte superior izquierda está el número de masa, A; en la parte inferior izquierda está el número atómico, Z, que identifica al elemento, ya que es igual al número de protones y el $\textsf{número de protones} = \textsf{número de electrones}$, y así se va a identificar cada elemento:
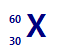
a. Se conoce que $Z = 30$, $\textsf{número de protones} = \textsf{número de electrones} = 30$, en la tabla periódica, se busca el elemento correspondiente, este es el Zn (Zinc),
$\textsf{Número de neutrones } (N) = \textsf{Número de masa } – \textsf{ Número de protones } N = A – Z$, por lo tanto, $N = 60 – 30 = 30 \textsf{ neutrones}$.
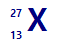
b. Igual que en el ejemplo anterior, $Z = \textsf{número atómico } = \textsf{ número de protones } = \textsf{ al número de electrones } = 13$, de la tabla periódica, se identifica el elemento, siendo este el aluminio (Al).
$\textsf{Número de neutrones } (N) = A – Z$, por lo tanto: $N = 27 – 13 = 14 \textsf{ neutrones}$.
• Realizar el numeral $c$ y $d$.
• Carga y tamaño del núcleo
La carga del núcleo determina su posición en el sistema periódico. Rutherford demostró que la mayor parte de la masa del átomo y su carga positiva están localizadas en una pequeña región central del átomo que llamó núcleo, cuyo radio estimó del orden de $10^{-14} m$ a través del estudio de dispersión de partículas alfa al incidir en núcleos de átomos metálicos.
El radio nuclear ha sido calculado posteriormente, siendo del orden de $10^{-15m}$, y resultando ser proporcional al número másico A:
$$R = r_o \cdot A^{\frac{1}{3}}$$$r_o$ es un valor constante para todos los núcleos y es igual a $1.3 × 10^{-15} m$.
Por tanto, el volumen de un núcleo si se considera su forma esférica, es proporcional al número A de nucleones, y la densidad nuclear es un valor constante, $10^{15}$ veces mayor que la densidad de la materia macroscópica, lo que da una idea de la gran compacidad de los nucleones dentro de un núcleo. Así mismo, demuestra que la materia macroscópica está esencialmente vacía, ya que la mayor parte de la masa está concentrada en los núcleos.
El tamaño del núcleo es tan pequeño, comparado con el resto del átomo, que si el átomo fuera una esfera de $1$ kilómetro de diámetro, su núcleo tendría apenas el tamaño de una canica de 1 cm y los electrones se verían apenas como puntos a los que difícilmente se les podría medir sus dimensiones. De hecho, el núcleo contiene casi toda la masa del átomo, y en muchos casos es aproximadamente $4 000$ veces más pesado que los electrones periféricos, pero tiene dimensiones muy pequeñas.
Por ser precisamente la parte fundamental del núcleo, a los protones y neutrones se les llama nucleones. A pesar de su pequeñez, el núcleo del átomo es muy pesado: si se pudiera juntar materia nuclear en un volumen de $1 cm^3$, su peso sería de doscientos millones de toneladas.
Uno de los grandes defectos del modelo nuclear de Rutherford era que no coincidía con los principios de la física contemporánea. La física proponía que en cualquier momento una partícula cargada eléctricamente, como un electrón experimentara una aceleración, debería emitir energía radiante. Además, un objeto que describe una orbita circular experimentará una aceleración hacia el centro del círculo. Entonces, podía concluirse que un electrón planetario, como lo propuso Rutherford, debía irradiar energía y, al perderla, descendería acercándose al núcleo. Un átomo así destruiría en unos pocos segundos.
Además, hay otro hecho que estuvo en contra del modelo de Rutherford: la discontinuidad de los espectros de emisión de los gases incandescentes. Si el electrón emitiera energía radiante a la vez que se acerque al núcleo (y en consecuencia, aumentara su velocidad) hasta caer en él, la frecuencia de la radiación emitida iría aumentando continuamente con el tiempo, ya que al transcurrir éste, aumenta la velocidad y por tanto la frecuencia de giro, igual a la de la rotación; en consecuencia, los espectros atómicos serían continuos, lo que estaría en contradicción con la realidad, pues dichos espectros están constituidos por diferentes líneas definidas, correspondientes a radiaciones de frecuencias distintas.
La primera solución importante que rompía con toda la tradición de la física clásica fue propuesta en 1913 por el físico danés Niels Bohr. Su modelo se basó en los postulados de Rutherford, y en los estudios de otros investigadores entre los que sobresalían Max Planck y los de Albert Einstein.
La existencia de los espectros de líneas de sustancias incandescentes suministraron un mayor apoyo experimental para que Bohr propusiera un modelo atómico basado en innumerables espectros de muchas sustancias incandescentes obtenidos por espectroscopías a finales del siglo XIX y comienzos del XX.
Para hacerlo comenzó a analizar el espectro de emisión del hidrógeno. Después de todo era elemento más simple, ya que solo posee un electrón, y por consiguiente, una sola carga positiva. Observó que los átomos originaban espectros diferentes, por tanto, poseían diferentes energías y, en consecuencia, debían poseer diferentes niveles de energía.
Lo anterior le permitió afirmar que el átomo era como un sistema planetario con órbitas circulares concéntricas en las cuales podía localizarse un electrón siempre y cuando hubiera absorbido la cantidad de energía cuantificada suficiente para colocarse, así fuera temporalmente, en una de dichas órbitas.
Había que tener en cuenta dos condiciones extremas una, que el electrón estuviera en condiciones de mínima energía, lo que podría llamarse su órbita base, y otra, es la que el electrón se encontrara infinitamente lejos del núcleo, es decir, en la que el núcleo estuviera solo. Entre estas dos condiciones extremas estarían todas las órbitas posibles, cuya energía correspondería a las líneas espectrales encontradas en las diferentes regiones del espectro, que para este caso se extendía (en la época de Bohr) desde el de los rayos X hasta el del infrarrojo. Todas estas observaciones le permitieron a Bohr crea un modelo para el átomo de hidrógeno.
Atendiendo a las características estructurales del átomo las propiedades de este varían. Así por ejemplo los átomos de que tienen el mismo número de electrones de valencia que poseen distintos números atómicos poseen características similares.
Los átomos están formados por un núcleo que posee una serie de partículas subatómicas. Alrededor del núcleo se hallan en diferentes órbitas los electrones.
Las partículas subatómicas de las que se compone el núcleo son los protones y los neutrones. Los átomos son eléctricamente neutros. Luego, si contienen electrones, cargados negativamente, deben contener también otras partículas con carga positiva que corresponden a la carga de aquellos. Estas partículas estables con signo positivo se las llamó protón.
Con estas dos partículas, se intentó construir todos los átomos conocidos, pero no pudo ser así porque faltaba unas de las partículas elementales del núcleo que fue descubierto por J. Chadwick en 1932 y que se llamó neutrón. Esta partícula era de carga nula y su masa es ligerísimamente superior a la del protón ($1,67482 × 10^{-27} kg$.)
Situados en órbitas alrededor del núcleo se hallan los electrones, partículas estables de carga eléctrica negativa y con una masa igual a $9.1110^{-31} kg$. El modelo de Bohr explica el espectro del átomo de hidrógeno, pero no los de átomos mayores.
La teoría atómica de Niels Bohr, generó un gran avance, ésta solo podía aplicarse a átomos muy sencillos, y aunque dedujo el valor de algunas constantes, que prácticamente coincidían con los valores experimentales sencillos, el modelo no fue capaz de explicar los numerosos saltos electrónicos, responsables de las líneas que aparecen en los espectros de los átomos que poseen más de un electrón. Al modelo de Bohr se le fueron introduciendo mejoras, pero la idea de un átomo compuesto por orbitas alrededor de un núcleo central, puede considerarse demasiado sencilla, no fue posible interpretar satisfactoriamente el espectro de otros átomos con más de un electrón ni mucho menos la capacidad de los átomos para formar enlaces químicos.
El neutrón es descubierto por James Chadwick, el descubrimiento de esta tercera partícula fundamental no fue descubierta hasta el 1932, la dificultad de su descubrimiento debía a que ésta partícula carecía de carga eléctrica. Así que su descubrimiento hasta ahora ha resuelto el problema de la radiación alfa y una mejora del modelo atómico de Rutherford, que quedó completado en los siguientes términos:

"Lo que embellece al desierto es que en alguna parte esconde un pozo de agua" Antoine De Saint Exupéry.


La mecánica cuántica es la ciencia que estudia las características y el comportamiento de las partículas atómicas y subatómicas.


La mecánica cuántica moderna surge hacia 1925 como resultado del conjunto de trabajos realizados por Heisenberg, Schrödinger, Born, Dirac, y es capaz de explicar de forma satisfactoria no sólo, la constitución atómica, sino otros fenómenos fisicoquímicos, además, de predecir una serie de sucesos que posteriormente se comprobarán experimentalmente, basándose en la teoría de Planck, y tomó como punto de partida la dualidad onda-corpúsculo de Louis De Broglie y el principio de incertidumbre de Heisenberg.
En 1923, Louis de Broglie sugirió que, del mismo modo que la radiación puede presentar un comportamiento corpuscular (en el estudio del efecto fotoeléctrico, por ejemplo), la materia podría presentar características ondulatorias. Esta sugerencia era muy atrevida ya que, desde luego, las propiedades ondulatorias de la materia no se observan a simple vista. No se quedó en el planteamiento cualitativo, extraordinariamente atrevido, sino que lo reflejó en la expresión en la que asignó una frecuencia y una longitud de onda (magnitudes típicamente ondulatorias) a las partículas. Las relaciones asignadas fueron las siguientes: Hipótesis de De Broglie. Recuperado en: http://agrega.juntadeandalucia.es/repositorio/23062017/91/es-an_2017062312_9121137/2_hiptesis_de_de_broglie.html
Siendo:
$λ =$ la longitud de onda en $m$
$h =$ (contante de plank): $h = 6.62 × 10^{-34} J \cdot s$
$m =$ la masa del corpúsculo (partícula) en $m/s$
$v = m \cdot v$ es la cantidad del movimiento o momento lineal del corpúsculo, (partícula), en $Kg \cdot m/s$
En 1924 en su tesis doctoral, inspirada en experimentos sobre la difracción de electrones, propuso la existencia de ondas de materia, es decir, que toda materia tenía una onda asociada a ella. Esta idea revolucionaria, fundada en la analogía con que la radiación tenía una partícula asociada, propiedad ya demostrada entonces, no despertó gran interés, pese a lo acertado de sus planteamientos, no tenía evidencias de producirse.
Como toda teoría física, esta idea, conocida por Hipótesis de De Broglie, carece de valor si no se confirma experimentalmente, y llegó en 1927 de la mano de los físicos americanos Davisson y Germer, los cuales demostraron la naturaleza ondulatoria de los electrones obteniendo unas figuras de difracción (fenómeno típico ondulatorio) al hacer incidir un chorro de electrones contra una superficie de níquel. Los electrones procedían de un filamento caliente y, después de ser acelerados, se dirigían a la superficie de un cristal de níquel.
Sin embargo, Einstein reconoció su importancia y cinco años después, en 1929, De Broglie recibió el Nobel en Física por su trabajo.Hipótesis de De Broglie. Recuperado en: http://agrega.juntadeandalucia.es/repositorio/10092010/5d/es-an_2010091013_9190014/ODE-4dfaa7d1-5453-3766-ab8d-22fad765353c/31_hiptesis_de_de_broglie.html
Puede decirse entonces, que en 1.924 Louis De Broglie extendió el carácter dual de la luz a los electrones, protones, neutrones, átomos y moléculas, y en general a todas las partículas materiales, basándose en consideraciones relativistas y en la teoría cuántica, pensó que si la luz se comportaba como onda y como partícula la materia debería poseer este carácter dual.
El movimiento de una partícula puede considerarse como el movimiento de un paquete de ondas, algo así como la superposición de varias ondas de longitudes de onda poco diferentes, cuyas oscilaciones se intensifican al máximo en el punto del espacio ocupado por la partícula.
No hay nada de imaginario en estas ondas de materia, son tan reales como las ondas luminosas y las del sonido, aunque no sean observables en todos los casos, como ocurre con las ondas electromagnéticas, los aspectos ondulatorios y de partículas de los cuerpos en movimiento nunca se pueden observar al mismo tiempo.
En ciertas situaciones una partícula en movimiento presenta propiedades ondulatorias y en otras situaciones presenta propiedades de partícula.Constitución del átomo: incidencia de los modelos atómicos en el avance de la Química. recuperado en: https://thales.cica.es/rd/Recursos/rd99/ed99-0280-01/ejem3-parte1.html
El Principio de Incertidumbre, o Principio de Indeterminación fue formulado por una de las más importantes figuras de la física cuántica: Werner Heisenberg.
Según esta teoría, si queremos observar una partícula y medir sus propiedades, es necesario "observarla" mediante un rayo de luz para que interaccione con ella y nos devuelva algún tipo de información al respecto. Pero, a escalas tan pequeñas, incluso propia la luz empuja nuestra partícula, alterando su dirección. Es decir que, aunque podamos saber dónde estaba la partícula en el instante justo en el que la luz impacta contra ella (en la siguiente imagen), no sabremos dónde estaba hace un momento ni dónde estará después, así que no podremos calcular su velocidad.
Heisenberg enunció su principio de incertidumbre, según el cual es imposible medir de manera exacta y simultánea la posición y la velocidad de una partícula ya que el producto de la incertidumbre en la posición por la incertidumbre en el momento lineal es siempre mayor que $h/4π$:
$$Δx \cdot Δp ≥ \frac{h}{4 \cdot π}$$De esta manera, si se aumenta la precisión en la medida de la posición empeora la medida simultánea del momento línea.
$$ΔE \cdot ΔT ≥ \frac{h}{4 \cdot π}$$La principal diferencia de la Física cuántica con la Física clásica es que esta es determinista, es decir, las ecuaciones de la física clásica permiten conocer la posición, velocidad, energía de cada partícula en cualquier instante.
El paradigma cambia completamente en la mecánica cuántica, ya que los mismos principios que rigen el universo a nivel macroscópico no funcionan cuando intentamos aplicarlos a escalas subatómicas. Para ello es necesario el tratamiento estadístico.
A esas escalas, nada tiene sentido: las partículas aparecen y desaparecen sin causa o las cosas pueden estar en dos sitios a la vez.
Así, puede decirse que uno de los aspectos más importantes de la mecánica cuántica es que no es posible determinar simultáneamente, de un modo preciso, la posición y la cantidad de movimiento de una partícula. Esta limitación se conoce con el nombre de principio de incertidumbre o de indeterminación de Heisenberg.
El principio de incertidumbre es una consecuencia de la dualidad onda-partícula de la radiación y de la materia.
Todos los objetos, independientemente de su tamaño, están regidos por el principio de incertidumbre, lo que significa que su posición y movimiento se pueden expresar solamente como probabilidades, pero este principio sólo es significativo para dimensiones tan pequeñas como las que presentan las partículas elementales de la materia. Descripción del modelo mecano-cuántico del átomo. La ecuación de onda de Schrödinger, publicada en 1926.
En 1926, el físico austriaco Erwin Schrödinger (1887-1961) propuso una ecuación, ahora conocida como ecuación de onda de Schrödinger, que incorpora los comportamientos tanto ondulatorio como de partícula del electrón. Los trabajos de Schrödinger indujeron a una nueva forma de tratar las partículas subatómicas conocida como mecánica cuántica o mecánica ondulatoria.
La aplicación de la ecuación de Schrödinger requiere cálculo avanzado, y no nos ocuparemos de los detalles de este enfoque. Lo que haremos será considerar cualitativamente los resultados que obtuvo, pues ofrecen una nueva y potente forma de visualizar la estructura electrónica. Comencemos por examinar la estructura electrónica del átomo más simple, el del hidrógeno.
La resolución de la ecuación de Schrödinger da lugar a una serie de funciones matemáticas llamadas funciones de onda que describen la onda de materia del electrón. Estas funciones por lo regular se representan con la letra griega psi, Ψ. aunque la función de onda en sí no tiene un significado físico directo, su cuadrado, $Ψ^2$, proporciona información acerca de la ubicación de un electrón cuando está en un estado de energía permitido.
En el caso del átomo de hidrógeno, las energías permitidas son las mismas que predice el modelo de Bohr. Sin embargo, el modelo de Bohr supone que el electrón está en una órbita circular con cierto radio alrededor del núcleo. En el modelo de la mecánica cuántica, la ubicación del electrón no se puede describir con tanta sencillez. El principio de incertidumbre sugiere que si conocemos la trayectoria (momentum) del electrón con gran exactitud, nuestro conocimiento simultáneo de su posición es muy incierto.
Por tanto, no es realista querer especificar la ubicación de un electrón individual en la cercanía del núcleo. Más bien, debemos contentarnos con una especie de conocimiento estadístico.
Así, en el modelo de la mecánica cuántica hablamos de la probabilidad de que el electrón esté en cierta región del espacio en un instante dado. De hecho, el cuadrado de la función de onda, $Ψ^2$, en un punto dado del espacio representa la probabilidad de encontrar un electrón en una región dada alrededor del núcleo de un átomo. Las funciones de probabilidad son llamadas orbitales.
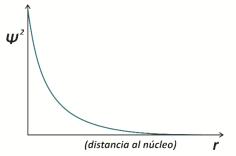
Es de observar en la , que a medida la distancia al núcleo disminuye, el valor de $Ψ^2$ aumenta. Esto sugiere que el electrón con menor nivel energético del átomo de hidrógeno se puede encontrar, lo más probable, más cerca del núcleo.
Esta densidad de probabilidad se puede visualizar imaginando que el electrón es un punto y cambia su posición cada segundo por un periodo largo de tiempo, como se observa en la la mayor densidad de puntos se halla más cerca del núcleo. Esta es la región de mayor densidad electrónica; es decir, la región de mayor probabilidad para encontrar un electrón.
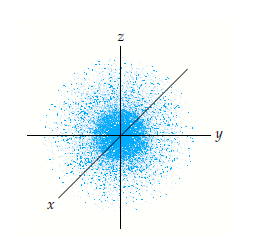
Para describir la distribución de los electrones en el hidrógeno y los demás átomos, la mecánica cuántica precisa de los números cuánticos: el número cuántico principal, el número cuántico del momento angular, el número cuántico magnético, el número cuántico de spin . Estos números se derivan de la solución matemática de la ecuación de Schrodinger para el átomo de hidrógeno, la que produce un conjunto de funciones de onda con sus correspondientes energías. Estas funciones de onda se denominan orbitales.
Los orbitales son regiones de espacio con alta probabilidad de encontrar un electrón y pueden ser caracterizados y descritos mediante los denominados números cuánticos:
$n$: número cuántico principal.
$l$: número cuántico orbital o de momento angular.
$ml$: número cuántico magnético.
$ms$: número cuántico de spin.
El número cuántico principal ($n$) solo puede tomar valores naturales $1, 2, 3, 4$, etc. Para poner un ejemplo sobre el número cuántico principal, si disponemos de un elemento químico donde su último nivel o capa es el $4s$, el valor de $N$ o número cuántico principal es de $4.$
Cada valor designa un nivel, el cual está relacionado con el tamaño y la energía del orbital. A mayor valor de $n$, mayor es la distancia promedio del electrón respecto al núcleo.
Al aumentar $n$, el orbital se hace más grande, y el electrón pasa más tiempo lejos del núcleo. Un aumento en $n$ también implica que el electrón tiene mayor energía, y por tanto, está unido menos firmemente al núcleo.
Determina la forma del orbital, es decir, la región donde el electrón se mueve. Los posibles valores de $ℓ$ dependen de $n$, de modo que, para cada valor de $n$, $ℓ$ puede tomar todos los valores comprendidos entre $0$ y $n - 1$. Por ejemplo, si $n = 4$, el número $ℓ$ puede tomar los valores $0, 1, 2$ y $3$. Se acostumbra simbolizar con letras los valores numéricos que puede tomar el número cuántico $ℓ$, como se observa en la :

Si $n = 1$ hay un solo valor posible para $ℓ$:
$ℓ = 0$ ya que $(n – 1)$ es $(1 –1) = 0$.
Si $n = 2$ entonces: $ℓ = 0$ y $1$.
Si $n = 3$: $ℓ = 0, 1$ y $2$.
Entonces: si $ℓ = 0$ tiene un orbital $s$, si $ℓ = 1$ tiene un orbital $p$ y así sucesivamente.
Al conjunto de orbitales con el mismo valor de n a menudo se le da el nombre de nivel o capa electrónica. Uno o más orbitales con los mismos valores de $n$ y $ℓ$ se le conocen como subnivel o subcapa, y, un orbital atómico es una región del espacio, en torno al núcleo, donde la probabilidad de encontrar el electrón con una determinada energía es muy grande.
Ejemplo: la capa con $n = 2$ está formada por dos subcapas $ℓ = 0$ y $1$ (los valores permitidos para $n = 2$), estos subniveles son los subniveles $2s$ y $2p$, donde $2$ expresa el valor de $n$ y $s$ y $p$ expresan los valores de $ℓ$.
Sus valores dependen del valor de $ℓ$, de manera que puede tomar todos los valores enteros comprendidos entre $−1$ y $+1$, incluido el cero. Está relacionado con la orientación del orbital en el espacio. así entonces,
Si $ℓ = 0$, entonces $m = 0$, es decir $1$ solo tipo de orbital $s$.
Si $ℓ = 1$, entonces $m = -1, 0, + 1$, es decir 3 tipos de suborbitales $p (px, py y pz)$
Si $ℓ = 2$, entonces $m = -2, -1, 0, + 1, +2$, es decir 5 tipos de suborbitales $d (du, dv, dx, dy, dz)$
Si $ℓ = 3$, entonces $m = -3, -2, -1, 0, +1, +2, +3$ es decir 7 tipos de suborbitales $f (fs, ft, fu, fv, fx, fy y fz)$
Corresponde al giro del electrón sobre su propio eje. Indica la cantidad de electrones presentes en un orbital y el tipo de giro que tienen de los electrones. Puede tener dos sentidos: en la dirección de los punteros del reloj y en el sentido inverso. Este número cuántico puede tomar sólo los valores $+1/2$ o $-1/2$. En cada tipo de suborbital cabe máximo 2 electrones y estos deben tener spines o giros opuestos. Cada orbital atómico es definido por tres números cuánticos: $n$ $l$ $ml$. Los electrones son definidos por cuatro números cuánticos: $n$, $ℓ$, $mℓ$, $s$. Los tres primeros definen el orbital en que se encuentra el electrón y $s$ define el giro.
Un orbital puede albergar como máximo dos electrones. Dichos electrones se diferencian entre sí por el sentido de giro sobre su eje. Cuando dos electrones ocupan el mismo orbital, sus sentidos de giro son opuestos. Como sólo son posibles dos sentidos de giro, el número cuántico $m_s$ entonces puede tomarlos valores ya mencionados, y también se simbolizan con flechas contrarias, como indica la figura:

La presenta un resumen de lo que se ha tratado hasta ahora con respecto a los números cuánticos:
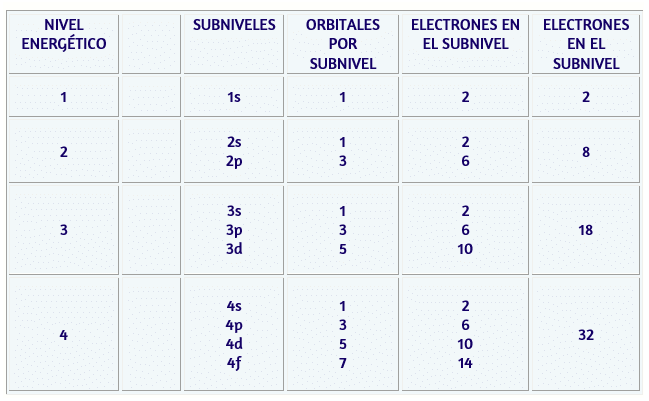
En 1925 el físico de origen austriaco Wolfgang Pauli, descubrió el principio que gobierna la disposición de los electrones en los átomos de muchos electrones. El principio de exclusión de Pauli dice que en un átomo no puede haber dos electrones que tengan el mismo conjunto de los cuatro números cuánticos $n$, $ℓ$, $m_ℓ$ y $m_s$.
Para un orbital dado los valores de $n$, $ℓ$ y $m_ℓ$ están fijos, por lo tanto si queremos colocar más de un electrón en un orbital y satisfacer el principio de exclusión de Pauli, nuestra única opción es asignar diferentes valores de ms a los electrones. Dado que solo hay dos de estos valores, concluimos que un orbital puede contener un máximo de dos electrones, los cuales deben tener espines opuestos.
Si representamos con líneas o casillas a los orbitales y con flechas a los electrones y consideramos al átomo de helio el cual solo tiene dos electrones, estos deben estar localizados en el primer nivel, es decir $n = 1, 1 = 0$ solo tiene un orbital, donde se deben colocar los electrones, de esta forma hay tres maneras posibles para realizarlo:
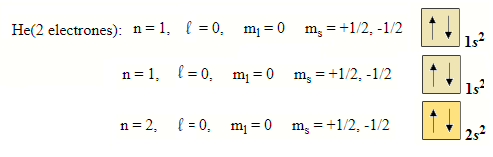
Aunque en principio un electrón se puede encontrar en cualquier lugar, se sabe que la mayor parte del tiempo está muy cerca del núcleo. Así, entonces, un orbital atómico puede considerarse como la función de onda del electrón de un átomo. Cuando se dice que un electrón está en cierto orbital, significa que la distribución de la densidad electrónica o la probabilidad de encontrar el electrón en ese espacio.
Orbitales $s$: Aunque es difícil describir la forma que tiene un orbital, es conveniente pensar en los orbitales en función de formas específicas.
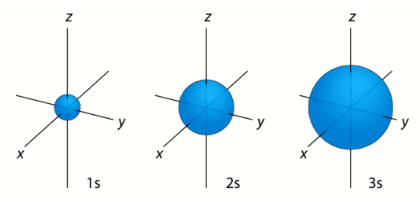
Se puede representar un orbital s dibujando un diagrama de contorno de superficie que englobe aproximadamente el 90% de la densidad electrónica total de un orbital, entonces un orbital s representado de esta forma es prácticamente una esfera. La representación del tamaño del orbital varía según el nivel de este: así:
Orbitales $p$: debemos aclarar que los orbitales $p$ comienzan con el número cuántico principal $n = 2$, ya que si $n = 1$, el valor para el número cuántico $ℓ$ solo puede ser cero, en consecuencia solo hay un orbital $1s$. Si se comienza con $n = 2$ y $ℓ = 1$, se tienen tres orbitales $2p$: $2px, 2py y 2pz$, la letra del subíndice indica el eje a lo largo del cual se orientan los orbitales. Estos tres orbitales p son idénticos en tamaño, forma y energía y solo difieren en su orientación. Observe, sin embargo que no hay una relación simple entre los valores de $mℓ$ y las direcciones $x, y$ y $z$.
En los diagramas de contorno de superficie de los orbitales $p$ se puede ver que cada orbital p puede ser imaginado como dos lóbulos a los lados opuestos del núcleo. Al igual que los orbitales $s$, los orbitales $p$ aumentan de tamaño desde $2p$ a $3p$ $s$ $4p$ y así sucesivamente.
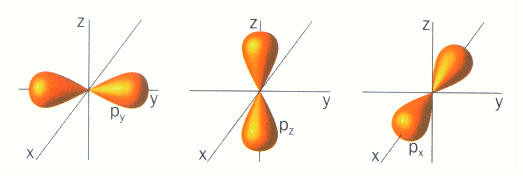
Orbitales $d$ y otros orbitales de mayor energía, orbital $f$: Cuando $ℓ = 2$, existen cinco valores de $mℓ$, que corresponden a cinco orbitales $d$. El valor mínimo de $n$ para un orbital $d$ es $3$. Como $ℓ$ nunca puede ser mayor que $n – 1$, cuando $n = 3$ y $ℓ = 2$, se tienen cinco orbitales $3d$, $3dxy, 3dyz, 3dxz, 3dx2-y2$ y $3dx2$. Como en el caso de los orbitales $p$ las diferentes orientaciones de los orbitales $d$ corresponden a los diferentes valores de $mℓ$, pero no hay correspondencia entre una orientación dada y los diferentes valores de $mℓ$. Todos los orbitales $3d$ de un átomo tienen energía idéntica.
Los orbitales $d$ tienen formas diversas formadas por cuatro grupos de cuatro lóbulos cada uno, y un último formado por una pareja de lóbulos rodeada por un anillo.
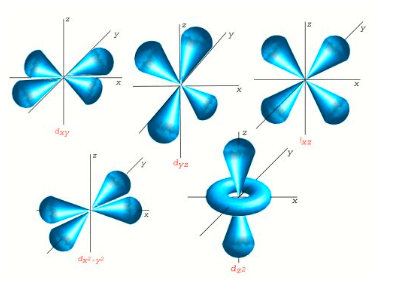
Cada uno de los 5 suborbitales d puede contener 2 electrones. Por lo tanto, el orbital $d$ puede contener un máximo de 10 electrones.
Los orbitales de más energía que los orbitales de se representan con $f, g$ y así sucesivamente. Los orbitales $f$ son importantes para explicar el comportamiento de los elementos con número atómico mayor de 57, aunque es difícil representar su forma.
Cuando $n$ es $4$ o mayor, hay siete orbitales $f$ equivalentes (para los cuales $ℓ = 3$, $mℓ = -3, -2, -1, 0, +1, +2, +3$). Las formas de los orbitales $f$ son aún más complicadas que las de los orbitales $d$, y no las presentaremos aquí. Sin embargo, como veremos en la siguiente sección, no debemos olvidar la existencia de estos orbitales al considerar la estructura electrónica de los átomos de la parte inferior de la tabla periódica.
La configuración electrónica indica la manera en la cual los electrones se estructuran o se modifican en un átomo de acuerdo con el modelo de capas electrónicas, es decir, La forma en que los electrones se distribuyen entre los diferentes orbitales de un átomo. La configuración electrónica es importante porque determina las propiedades de combinación química de los átomos y por tanto su posición en la tabla periódica, además, Una gran parte de las propiedades físicas y todas las propiedades químicas de un elemento dependen de la corteza electrónica de los átomos que lo componen.
La configuración electrónica más estable, o basal, de un átomo es aquella en la que los electrones están en los estados de energía más bajos posibles.
Con el propósito de describir cómo están dispuestos los electrones en la periferia del núcleo atómico, deben tenerse en cuenta los siguientes principios:
El principio de Aufbau contiene una serie de instrucciones relacionadas a la ubicación de electrones en los orbitales de un átomo. Establece que el electrón que distingue a un elemento del elemento precedente se ubica en el orbital atómico de menor energía disponible ($s$ o $p$), y, es complemento del principio de ordenamiento:
Al ordenar los elementos de manera creciente de números atómicos, cada átomo de un elemento tendrá un electrón más que el del elemento que le precede. Por ejemplo, cada átomo de carbono ($Z = 6$) tendrá un electrón más que cada átomo de boro ($Z = 5$).
Un orbital no puede contener más de dos electrones, y los espines de dichos electrones deben tener valores opuestos.
La regla de Hund hace referencia a que ningún orbital puede tener dos orientaciones del giro del electrón sin antes de que los restantes números cuánticos magnéticos de la misma subcapa tengan al menos uno. Se comienza con el orbital de menor energía. Primero debe llenarse el orbital 1s (hasta un máximo de dos electrones), esto de acuerdo con el número cuántico $ℓ$. Seguido se llena el orbital $2s$ (también con dos electrones como máximo). La subcapa $2p$ tiene tres orbitales degenerados en energía denominados, según su posición tridimensional, $2px, 2py, 2pz$. Así, los tres orbitales $2p$ puede llenarse hasta con seis electrones, dos en cada uno. De nuevo, de acuerdo con la regla de Hund, deben tener todos por lo menos un electrón antes de que alguno llegue a tener dos, y así, sucesivamente, como se puede observar seguidamente:
A través de esta regla, se define un orden en el llenado de los orbitales, los que se rigen por los tres números cuánticos $n$, $ℓ$ y $mℓ$.
Este método fue desarrollado como regla nemotécnica de tal manera que se pueda expresar la configuración electrónica de un átomo en función del principio de Aufbau. Esto implica que los electrones son integrados en un orden especial uno a uno a cada orbital disponible tomando como referencia sus niveles de energía.
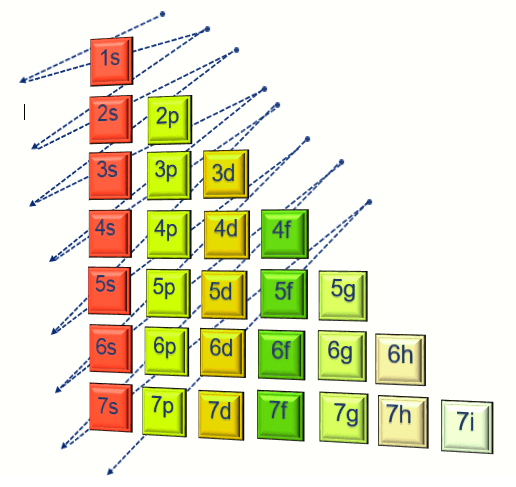
De esa forma, los primeros orbitales están conectados con los electrones de menor energía y los últimos orbitales se asocian con los electrones de mayor energía presentes en el átomo.
Cómo hacerlo: En primer lugar hay que determinar al número atómico $Z$ del elemento a estudiar, el cual está asociado al número de electrones que se encuentran en un átomo neutro. Luego, se determina el llenado de los electrones en los orbitales a través del trazo de líneas diagonales apuntando hacia abajo, de izquierda a derecha.
Seguidamente, se establece el llenado desde el orbital $1s$ en adelante, siguiendo el orden presente en el diagrama. Cabe destacar que, para el caso de los orbitales "$s$" se alojan 2 electrones; del mismo modo, para los orbitales "$p$" se alojan 6 electrones y 10 electrones para los orbitales "$d$", respectivamente. Ahora bien, la importancia de este diagrama radica en que es una forma fácil y sencilla de explicar y calcular las configuraciones electrónicas del átomo con base a la Regla de Madelung. Esto permitió la masificación de la química como ciencia de estudio y fue punta de lanza para los desarrollos tecnológicos que se dieron en épocas posteriores.
La escena anterior fue creada por Juan Guillermo Rivera Berrío.

Según la regla de Hund, debido a la repulsión entre electrones, estos tienden a posicionarse en posiciones lo más alejadas posibles y con spines paralelos, es decir, los electrones deben estar tan desapareados como sea posible. Por ejemplo, en la distribución electrónica de los elementos químicos como el nitrógeno cuyo número atómico es $Z = 7$, tendremos los orbitales $2p3$ que contendrán los 3 electrones totalmente desapareados.
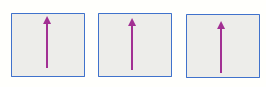
Sin embargo, en la configuración electrónica del átomo de oxígeno existe un conjunto de orbitales $2p^4$ por lo que ya no podrán estar completamente desapareados, por lo tanto la configuración electrónica del oxígeno en ese conjunto mencionado es:
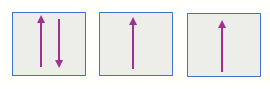
Los subniveles llenos y semiocupados confieren al átomo una estabilidad adicional y en ocasiones se producen promociones de electrones más bajos de energía hacia niveles superiores para conformar estas configuraciones electrónicas de los elementos químicos más estables.
Existen 3 formas de notación para las distribuciones electrónicas el ya visto diagrama de orbitales, la notación $spdf$ condensada $(1s^2 2s^2 2p^2)$ y la notación $spdf$ expandida $( 1s^2 2s^2 2px^1 2py^1).$
Para determinar que orbitales tienen más energía se sigue la regla $n + l$; dados dos orbitales tendrá mayor energía aquel cuya suma de valores de números cuánticos $n$ y $l$ sea mayor, y a igualdad tendrá mayor energía el que tenga mayor número cuántico principal $n$.
También, tenga en cuenta que la configuración electrónica de los elementos químicos está basada en su número atómico, cuyo símbolo es $Z$. El número atómico es el número de electrones que hay en un átomo. Es lo mismo que el número de protones, dado que se compensan las cargas negativas con las cargas positivas.
1) El litio (Li) tiene tres electrones: dos en el primer nivel de energía y un tercer electrón que debe estar en el subnivel $s$ del segundo nivel de energía. La configuración electrónica del litio Li es $1s^2 2s^1$. En el caso del ion litio Li$+$, simplemente se quita el único electrón de valencia de $2s$ y se escribe $1s^2$.
2) Cromo, $Z = 17$, su configuración es $1s^2 2s^2 2p^6 3s^2 3p^5$.
3) Plata, $Z = 47$, su configuración es $1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5^2 4d^9$.
4) Sodio, $Z = 11$, su configuración es $1s^2 2s^2 2p^6 3s^1$.
5) Cloro, $Z = 17$, su configuración es $1s^2 2s^2 2p^6 3s^2 3p^5$.
6) Cromo, $Z = 24$, su configuración es $1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^4$.
7) Aluminio, $Z = 13$, su configuración es $1s^2 2s^2 2p^6 3s^2 3p^1$.


El mundo es un lugar peligroso. No por causa de los que hacen el mal, sino por aquellos que no hacen nada por evitarlo. Albert Einstein.

"Los maestros, como las lámparas de la educación local debe cumplir con todos los conocimientos más recientes y los requerimientos de su especialidad". Dmitri Mendeléyev


Para simplificar y racionalizar el estudio de la química de los elementos químicos, hubo múltiples intentos de clasificarlos en función de sus propiedades y pesos atómicos a lo largo del siglo XIX. Son emblemáticas las triadas del alemán Johann Wolfgang Döbereiner, que clasificó en 1829 los elementos, por propiedades químicas similares, en grupos de tres (como calcio, estroncio y bario) y advirtió que, en cada triada, el peso atómico de uno era la media aritmética de los otros dos aproximadamente. El geólogo francés Alexandre Émile Béguyer de Chancourtois, en 1862, colocó los elementos conocidos (y algunos compuestos) por orden creciente de peso atómico, sobre una curva helicoidal inscrita alrededor de un cilindro vertical con una circunferencia de 16 unidades (peso atómico del oxígeno), en la que los elementos que caían en la misma vertical tenían propiedades semejantes. Sugirió una ordenación que denominó vis tellurique (tornillo telúrico), por estar el telurio en el centro de la gráfica. Para Scerri, aunque Chancourtois recibió poca atención en su tiempo, fue quien realmente descubrió la periodicidad química.
A finales de la década de los 1860, aparecieron dos trabajos publicados con diferentes enfoques sobre la repetición periódica de los elementos y regular de sus propiedades, el del químico alemán Julius L. von Meyer y el del científico ruso Dimitri Ivanovich Mendeléiev.
Pero Mendeléiev y Meyer, en 1869, aprovecharon los conocimientos existentes sobre la clasificación de los elementos químicos según sus propiedades y encontraron que si estos se ordenaban de acuerdo aumentaba la masa atómica, cada.
cierto número de elementos repetían las propiedades químicas y físicas o variaban de forma sistemática y regular.Esto los condujo a realizar una clasificación de los elementos en orden creciente de su masa atómica, de tal manera, que las columnas relacionaran los elementos de propiedades semejantes. Así, es que fue establecida la primera ley periódica, la cual manifiesta: las propiedades físicas y químicas de los elementos químicos son funciones periódicas de sus masas atómicas.
Se dispusieron los 63 elementos que se conocían en líneas, una debajo de la otra, de forma que los que tenían igual valencia se hallaban ubicados en una misma fila. A este ordenamiento se le llamó Tabla periódica de los elementos.
Mendeléiev observó que en su clasificación debía dejar algunos “huecos” vacíos, ya que no conocía los elementos que tenían las propiedades de esa posición; introduciendo de esta manera el sistema de períodos largos, ver .
Gracias a la tabla periódica de Mendeléiev, se pudieron relacionar las propiedades de los elementos y sus compuestos con otros de comportamiento similar, lo que sirvió de impulso para la racionalización de la química. Su tabla supuso un verdadero renacimiento de esta ciencia y se considera que varios descubrimientos posteriores tienen su base en la búsqueda de las causas de las irregularidades que señaló.
En 1870, Meyer estudió los elementos químicos en forma gráfica, representando el volumen de cada átomo en función de su masa y obtuvo una gráfica en picos cada vez mayores. En 1871, ambos propusieron una nueva tabla que se conformaba por siete filas y, ocho columnas, a causa, de que los elementos poseían propiedades semejantes.
Los descubrimientos del galio en 1875, en 1879 el escandio y en 1886 del germanio, y la comprobación de las propiedades previstas por Mendeléiev para los elementos descubiertos confirmaron brillantemente la validez de la clasificación periódica propuesta por este científico.

Mendeléiev cambió el orden de colocación de algunos pares de elementos cuando las propiedades químicas lo hacían aconsejable, en otros casos fue preciso revisar los valores del peso atómico: berilio, indio y uranio.
Esta tabla periódica, además, de la necesidad de cambiar el orden de la colocación de algunas parejas de elementos, presentaban algunas dificultades: No hay un grupo definido para el hidrógeno, podría colocarse en el grupo de los halógenos o de los metales alcalinos.
La tabla periódica se presenta como una herramienta gráfica en la que figuran todos los elementos químicos conocidos por la humanidad, organizados conforme al número de protones de sus átomos, también llamado número atómico, y tomando en cuenta también la configuración de sus electrones y las propiedades químicas específicas que presentan.
De esa manera, los elementos que se comportan de manera semejante ocupan renglones cercanos, y se identifican en grupos (columnas, dieciocho en total) y períodos (filas, siete en total). En principio, toda la materia conocida del universo está compuesta por diversas combinaciones de los elementos que se encuentran en esta tabla: hasta ahora se conocen 118 elementos, pero hay que tener presente que en 1952, el científico costarricense Gil Chaverri (1921-2005) presentó una nueva versión basada en la estructura electrónica de los elementos, la cual permite colocar las series lantánidos y los actínidos en una secuencia lógica de acuerdo con su número atómico, de esa manera, los elementos que se comportan de manera semejante ocupan renglones cercanos, y se identifican en grupos (columnas, dieciocho en total) y períodos (filas, siete en total). En principio, toda la materia conocida del universo está compuesta por diversas combinaciones de los elementos que se encuentran en esta tabla: hasta ahora se conocen 118 elementos.
La tabla periódica actual es un sistema donde se clasifican los elementos conocidos hasta la fecha. Se colocan de izquierda a derecha y de arriba a abajo en orden creciente de sus números atómicos. Los elementos están ordenados en siete hileras horizontales llamadas periodos, y en 18 columnas verticales llamadas grupos o familias. Hacia abajo y a la izquierda aumenta el radio atómico y el radio iónico. Hacia arriba y a la derecha aumenta la energía de ionización, la afinidad electrónica y la electronegatividad.
A las columnas verticales de la tabla periódica se les conoce como grupos o familias. Hay 18 grupos en la tabla periódica estándar, de los cuales diez son grupos cortos y los ocho restantes largos, que muchos de estos grupos correspondan a conocidas familias de elementos químicos: la tabla periódica se ideó para ordenar estas familias de una forma coherente y fácil de ver.
Todos los elementos que pertenecen a un grupo tienen la misma valencia atómica, entendido como el número de electrones en la última capa, y por ello, tienen propiedades similares entre sí. La explicación moderna del ordenamiento en la tabla periódica es que los elementos de un grupo poseen configuraciones electrónicas similares y la misma valencia atómica, o número de electrones en la última capa. Dado que las propiedades químicas dependen profundamente de las interacciones de los electrones que están ubicados en los niveles más externos, los elementos de un mismo grupo tienen propiedades químicas similares. Por ejemplo, los elementos en el grupo 1 tienen una configuración electrónica $ns^1$ y una valencia de 1 (un electrón externo).
Todos tienden a perder ese electrón al enlazarse como iones positivos de $+1$. Los elementos en el último grupo de la derecha son los gases nobles, los cuales tienen lleno su último nivel de energía (regla del octeto) y, por ello, son excepcionalmente no reactivos y son también llamados gases inertes.
Numerados de izquierda a derecha utilizando números arábigos, según la última recomendación de la IUPAC La Unión Internacional de Química Pura y Aplicada, más conocida por sus siglas en inglés IUPAC (International Union of Pure and Applied Chemistry), es un grupo de trabajo que tiene como miembros a las sociedades nacionales de química. Es la autoridad reconocida en el desarrollo de estándares para denominación de compuestos químicos, mediante su Comité Interdivisional de Nomenclatura y Símbolos (Interdivisional Committee on Nomenclature and Symbols). Es miembro del Consejo Internacional para la Ciencia (ICSU). Recuperado en: https://es.wikipedia.org/wiki/Tabla_peri%C3%B3dica_de_los_elementos (según la antigua propuesta de la IUPAC) de 1988 y entre paréntesis según el sistema estadounidense, los grupos de la tabla periódica son:
Las filas horizontales de la tabla periódica son llamadas períodos. El número de niveles energéticos de un átomo determina el período al que pertenece. Cada nivel está dividido en distintos subniveles, que conforme aumenta su número atómico se van llenando en este orden.
Siguiendo esa norma, cada elemento se coloca según su configuración electrónica y da forma a la tabla periódica.
Los electrones situados en niveles más externos determinan en gran medida las propiedades químicas, por lo que éstas tienden a ser similares dentro de un mismo grupo, sin embargo la masa atómica varía considerablemente incluso entre elementos adyacentes.
Al contrario, dos elementos adyacentes de mismo periodo tienen una masa similar, pero propiedades químicas diferentes.
La tabla periódica consta de 7 períodos:
La tabla periódica se puede también dividir en bloques de elementos según el orbital que estén ocupando los electrones más externos, de acuerdo al principio de Aufbau. Los bloques o regiones se denominan según la letra que hace referencia al orbital más externo: $s, p, d$ y $f$. Podría haber más elementos que llenarían otros orbitales, pero no se han sintetizado o descubierto; en este caso se continúa con el orden alfabético para nombrarlos.
Esta notación se tiene en cuenta, pues las propiedades físicas y químicas de los elementos se explican con base en sus configuraciones electrónicas y en la tabla periódica se resume gran parte del comportamiento químico de las sustancias elementales, a continuación se da una explicación a partir de las notaciones espectrales.
En la , se ilustra cada uno de los cuatro bloques de elementos de la tabla periódica, lo que tienen en cuenta los electrones más externos:
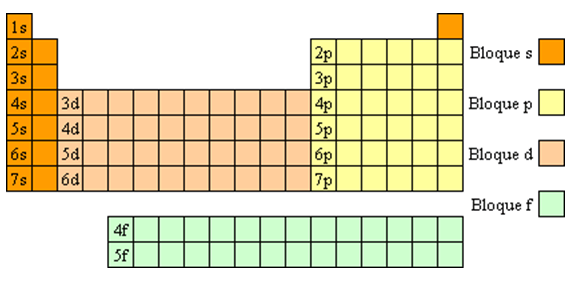
Las notaciones espectrales para los elementos del grupo VIIIA, con números atómicos 2, 10, 18, 36, 54 y 86, que corresponden los elementos helio, neón, argón, criptón, xenón y radón, se muestran en la .

En este grupo, se ha de tener en cuenta, a excepción del Helio, He, tienen en su nivel externo o nivel de valencia ocho electrones: $ns^2 np^6$. EL Helio posee dos electrones, que corresponde a la cantidad máxima de electrones del subnivel 1S y al igual que los demás elementos de este grupo, es químicamente poco reactivo, además, todos los elementos de este grupo, a temperatura ambiente, son gaseosos y tienen poca actividad química, por lo cual se les conoce como gases nobles.
Cabe notar que a este grupo , también pertenece el elemento más pesado de la tabla periódica, el ununoctio, Uuo, nombre que recibió cuando fue creado en laboratorio, por lo tanto, es un elemento sintético, hoy día, es conocido bajo el nombre de oganesón, Og, siendo anunciada su creación, por la IUPAC, el 30 de diciembre de 2015. Su nombre, se debe en honor al trabajo del químico ruso Yuri Oganessian, que descubrió elementos superpesados y quien encontró evidencias experimentales.
Todos los metales alcalinos son metales plateados brillantes a excepción del cesio, que es de un color dorado. Como metales son muy buenos conductores térmicos y eléctricos, pero sus otras características hacen saltar la alarma de cualquier persona que piense en la palabra metal. Todos ellos son muy blandos, más blandos conforme bajamos por el grupo: el litio se puede cortar con un cuchillo sin mucho esfuerzo, el potasio ya directamente se corta como si fuera mantequilla. Además, sus puntos de fusión son bajos, mas bajos conforme más abajo se encuentra el elemento que miremos.
Estos metales, pertenecen al grupo 1, el que esta mas hacia la izquierda, de la tabla periódica (excepto el Hidrógeno que es un gas). Está compuesto por Li, Na, K, Rb, Cs, Fr, en su orden sus nombres son litio, sodio, potasio, rubidio, cesio, y francio, la notación espectral para estos elementos se referencia en la .
Son metales blandos, químicamente muy activos, se les encuentra generalmente en forma de sales, no existen en la naturaleza en forma libre. Todos los metales alcalinos poseen un solo electrón en su nivel más externo.
Tienen tendencia a perder este electrón y a reaccionar fácilmente con los no metales, esto es debido a que tienen poca afinidad electrónica, y baja energía de ionización.
La Configuración electrónica del grupo es $ns^1$. Por ello se dice que se encuentran en la zona "$s$" de la tabla.

Los Halógenos son un grupo de elementos conocido como Grupo VIIA o Grupo 17 en la Tabla Periódica de los Elementos. Etimológicamente la palabra "halógeno" proviene del griego "formador de sales" en referencia a la facilidad que tienen estos elementos para unirse con el sodio (Na) y formar sales como el cloruro de sodio (NaCl).
Las notaciones espectrales para los elementos cuyos números atómicos son: 9, 17, 35, 53 y 85 que corresponden a los elementos flúor, cloro, bromo, yodo y ástato, se aprecian en la .
La Configuración electrónica del grupo es $ns^1$. Por ello se dice que se encuentran en la zona "$s$" de la tabla.

Los derivados del flúor tienen una notable importancia en el ámbito de la industria. Entre ellos destacan los hidrocarburos fluorados, como el anticongelante freón y la resina teflón, lubricante de notables propiedades mecánicas. Los fluoruros son útiles como insecticidas. Además, pequeñísimas cantidades de flúor añadidas al agua potable previenen la caries dental, razón por la que además suele incluirse en la composición de los dentífricos.
El cloro encuentra su principal aplicación como agente de blanqueo en las industrias papelera y textil. Así mismo, se emplea en la esterilización del agua potable y de las piscinas, y en las industrias de colorantes, medicamentos y desinfectantes.
El nombre de "transición" proviene de una característica que presentan estos elementos de poder ser estables por si mismos sin necesidad de una reacción con otro elemento. Cuando a su última capa de valencia le faltan electrones para estar completa, los extrae de capas internas.
Con eso es estable, pero le faltarían electrones en la capa donde los extrajo, así que los completa con otros electrones propios de otra capa. Y así sucesivamente; este fenómeno se le llama Transición electrónica.
Esto también tiene que ver con que estos elementos sean tan estables y difíciles de hacer reaccionar con otros. La definición más amplia es la que tradicionalmente se ha utilizado. Sin embargo, muchas propiedades interesantes de los elementos de transición como grupo son el resultado de su subcapa d parcialmente completa.
El zinc, cadmio, y mercurio están excluidos de los metales de transición, ya que tienen una configuración d10.
• Sus propiedades físicas más características son:
Sólidos, con puntos de fusión altos(Excepto el Hg); en general son dúctiles y maleables, poseen brillo plateado o son de color gris (Excepto Cu y Au), son buenos conductores de calor y de la electricidad, forma aleaciones fácilmente.
En cuanto a su notación espectral, es importante destacar que tienen llenos o semillenos los orbitales $d$; están formados por 8 grupos y se hallan ubicados en el centro de la tabla periódica.
Estos metales de transición son los cuarenta elementos químicos, del 21 al 30, del 39 al 48, del 71 al 80 y del 103 al 112.
Al estudiar la tabla periódica, se puede observar que las configuraciones electrónicas de los elementos muestran una variación periódica al aumentar el número atómico. En consecuencia, los elementos también presentan variaciones periódicas en cuanto a su comportamiento fisicoquímico. Son muchas las propiedades de los elementos que muestran periodicidad respecto a su número atómico, sin embargo, algunas de ellas son más importantes que otras cuando se quiere explicar o predecir la conducta química de los elementos. Entre estas últimas podemos citar el radio atómico, la energía de ionización, la energía de afinidad electrónica, la electronegatividad, y el carácter metálico de los elementos.
Factores de los que dependen las propiedades periódicas:
Es la carga real que mantiene unido un $e–$ al núcleo. Depende de dos factores contrapuestos:
- Carga nuclear ($Z$). Se trata de la carga positiva del núcleo del átomo. A mayor $Z$ mayor $Z*$, pues habrá mayor atracción por parte del núcleo al haber más protones.
- Apantallamiento o efecto pantalla:
Las propiedades periódicas dependen de la capa de valencia. Las capas internas del átomo, provocan una repulsión de los $e–$ interiores sobre los situados en la capa de valencia, que hace disminuir el efecto de la carga nuclear. Se llama "apantallamiento o efecto pantalla". A mayor apantallamiento menor "$Z*$".
Cuanto mayor es la distancia de la capa de valencia, menor es la atracción por parte de núcleo a los electrones de esta capa periférica.
En la práctica suele manejarse el término carga nuclear efectiva.
La carga nuclear efectiva es la carga que debiera tener el núcleo para que, en ausencia de otros electrones, la atracción del núcleo sobre el electrón considerado fuera la misma que la atracción neta que experimenta el electrón en el átomo real.
La carga nuclear efectiva puede calcularse a partir de la expresión siguiente:
$Z* = Z - a$, donde:
$Z* =$ carga nuclear efectiva.
$Z =$ carga nuclear.
$a =$ apantallamiento.
Así, la carga nuclear efectiva del helio sobre sus dos electrones es menor que $+2$.
El apantallamiento de los electrones depende principalmente del orbital que ocupan, y su cálculo no se incluye en la materia de este curso; no obstante, en general podemos resumirlo así:
Veamos como varía la carga nuclear efectiva a lo largo de los períodos y de los grupos.
A lo largo de un período, la carga nuclear efectiva sobre el electrón más externo aumenta conforme lo hace el número atómica.
A lo largo de un grupo, la carga nuclear efectiva sobre el electrón más externo es la misma, independientemente del número atómico.
En este caso, todos los elementos del mismo grupo poseen configuraciones electrónicas de valencia iguales, y se diferencian en la configuración electrónica más profunda o de gas noble.
Como los electrones que forman la estructura interna apantallan con el valor 1, y todos los elementos tienen la misma configuración electrónica de valencia, la carga nuclear efectiva sobre el electrón más externo no varía al aumentar el número atómico.Química: Propiedades periódicas de los elementos. Recuperado en: https://es.scribd.com/document/380078833/Guia-2-Sistema-Periodico-de-Los-Elementos-y-Enlace-Quimico
- Varía poco al aumentar $Z$ en los $e–$ de valencia de un mismo grupo, pues aunque hay una mayor carga nuclear también hay un mayor apantallamiento. Consideraremos que en la práctica cada $e–$ de capa interior es capaz de contrarrestar el efecto de un protón.
Crece hacia la derecha en los elementos de un mismo período debido a la mayor “$Z$”, pues el apantallamiento de los $e–$ de última capa es el mismo.
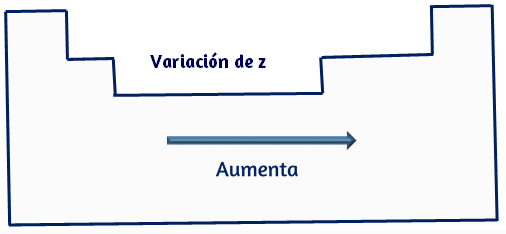
El tamaño de un átomo no es invariable sino que depende del entorno inmediato en el que se encuentre, de su interacción con los átomos vecinos. Estimar el tamaño de los átomos es un poco complicado debido a la naturaleza difusa de la nube electrónica que rodea al núcleo y que varía según los factores ambientales. Se realizan las medidas sobre muestras de elementos puros no combinados químicamente y los datos así obtenidos son los tamaños relativos de los átomos.
El radio atómico identifica la distancia que existe entre el núcleo y el orbital (con electrones) más externo de un átomo; es la mitad de la distancia entre los núcleos de dos átomos iguales enlazados. Está relacionado con el volumen del átomo. A mayor radio atómico corresponde mayor volumen.

En un período, al aumentar el número atómico, disminuye el radio atómico.
Al aumentar el número atómico de los elementos de un mismo período, se incrementa la carga nuclear efectiva sobre el electrón más externo y el número de niveles ocupados no varía. En consecuencia, aumenta la intensidad de la atracción entre el electrón y el núcleo, por lo que disminuye la distancia entre ellos.
En un grupo, al aumentar el número atómico, aumenta el radio atómico. Al aumentar el número atómico de los elementos de un grupo, se incrementa el número de niveles ocupados, mientras que la carga nuclear efectiva sobre el electrón más externo es la misma. En consecuencia, aumenta el radio atómico.
En el caso de los elementos de transición, las variaciones no son tan obvias ya que los electrones se añaden a una capa interior, pero todos ellos tienen radios atómicos inferiores a los de los elementos de los grupos precedentes IA y IIA. Los volúmenes atómicos van disminuyendo hasta que llega un momento en el que hay tantos electrones en la nueva capa que los apantallamientos mutuos y las repulsiones se hacen importantes, observándose un crecimiento paulatino tras llegar a un mínimo.
La estructura y la estabilidad de los sólidos iónicos depende de manera crucial del tamaño de los iones. Éste determina tanto la energía de red del sólido como la forma en que los iones se empacan en el sólido. Además el tamaño iónico influye en las propiedades de los iones en disolución.
Su variación en la tabla periódica es equivalente al de los radios atómicos. Un anión, al ganar electrones presenta un aumento en la repulsión entre los electrones, lo que hace que el radio aniónico sea mayor que el atómico.
Un catión, al perder electrones presenta una disminución de la repulsión entre los electrones, lo que hace que el radio del catión sea menor que el atómico.
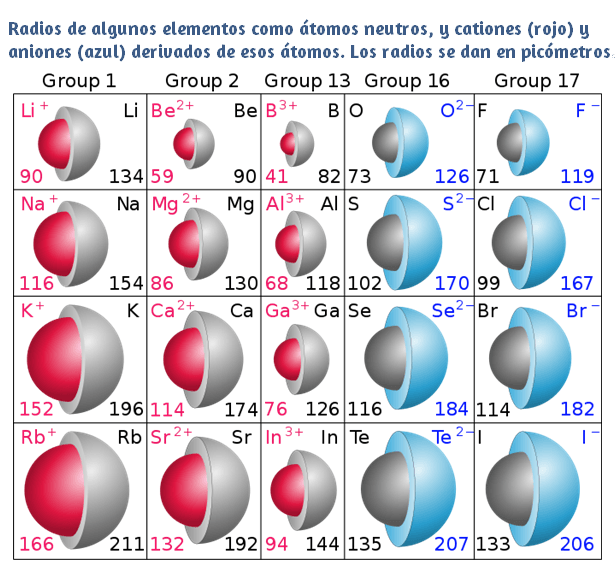
Esta propiedad es importante cuando se estudian compuestos iónicos, ya que la estructura tridimensional de éstos depende exclusivamente del tamaño de los iones involucrados.
En general, se puede decir que:
Este hecho también se explica fácilmente al estudiar la carga nuclear efectiva sobre el electrón más externo.
Es la mínima energía necesaria para extraer un $e –$ (el más externo y por tanto más débilmente unido a él) de su capa de valencia a un átomo neutro en estado gaseoso y fundamental para formar un catión. Siempre se les asigna un valor positivo, por tratarse de una reacción endotérmica (absorbe energía).
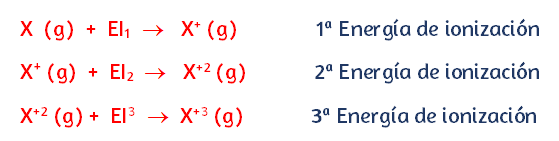
Podemos hablar de 1ª, 2ª, 3ª…. energía de ionización, que corresponde a la energía necesaria para que el átomo ceda el 1er, 2°, 3 electrón, respectivamente.
En un grupo la energía de ionización aumenta hacia arriba: Al descender en el grupo se intensifica el efecto pantalla, al elevarse el número de capas entre el núcleo y la capa de valencia, por lo que la energía de ionización disminuirá.
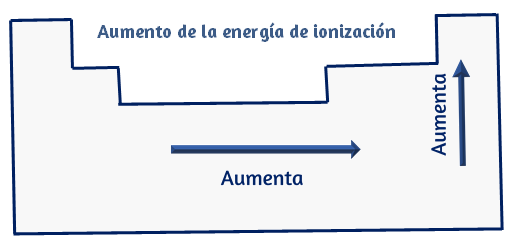
La energía de ionización de los gases nobles es muy grande, porque se debe extraer un $e –$ a átomos con configuración electrónica muy estable.
En teoría existen tantas energía de ionización como electrones tenga el átomo en su capa de valencia, son las energías de ionización sucesivas. En general, son cada vez mayores, ya que a medida que desaparecen los $e –$ hay un exceso de carga positiva en el núcleo que atraerá con más fuerza a los electrones restantes.
En los períodos influye la configuración electrónica de la capa de valencia. Se pueden observar saltos muy importantes en la energía de ionización si al perder un $e –$ se pierde una estructura de capa cerrada o semicapa cerrada ($ns^2 np^6, ns^2 o np^3 ⇒$ corresponde con gases nobles, alcalinotérreos y nitrogenoideos), por lo que la diferencia con las energías de ionización anteriores será muy alta.
Energía desprendida en un proceso en el que un determinado átomo neutro gaseoso en estado fundamental capta un electrón para dar un ión mononegativo gaseoso en estado fundamental. Con muy pocas excepciones, este proceso de captación de electrones es favorable (la atracción nuclear compensa la repulsión electrónica). Las segundas, terceras, ... afinidades electrónicas son siempre energéticamente desfavorables. La energía total puesta en juego para pasar de un átomo neutro en estado fundamental y gaseoso a un ion negativo con n cargas es la suma de las afinidades electrónicas.
A partir de los valores de la afinidad electrónica, se observan algunas regularidades que, al igual que la energía de ionización, encuentran explicación en la configuración electrónica:
Los elementos halógenos son los que forman aniones $X^-$ con mayor facilidad. Todos ellos tienen una estructura electrónica de valencia $ns^2$, $np^5$ y, por lo tanto, al aceptar el electrón, alcanzan estructura electrónica externa de gas noble, $ns^2$, $np^6$ que es especialmente estable.
Los elementos alcalinotérreos y los del grupo 15 presentan una mínima tendencia a aceptar un electrón. Esto es debido a que sus estructuras electrónicas externas son $ns^2$ y $ns^2 np^3$ respectivamente, que confieren estabilidad adicional al sistema.
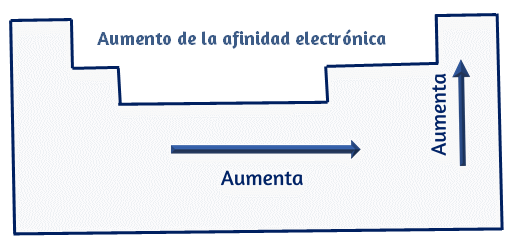
La afinidad electrónica de cualquier anión es positiva, es decir, los aniones no presentan tendencia a aceptar electrones, lo que no significa que los aniones con más de una carga negativa sean inestables; la estabilidad de un ion, catión o anión, depende sobre todo de los enlaces químicos en los que participa.
La variación de afinidad electrónica dentro del sistema periódico es similar a la variación del potencial de ionización, aunque es mucho menos periódica. A partir de estas dos propiedades se puede analizar hasta qué punto un átomo neutro está satisfecho con su número de electrones. A mayor potencial de ionización y electroafinidad, mayor es la apetencia electrónica (electronegatividad) de la especie.
Los elementos con las afinidades electrónicas más altas son los situados cerca del oxígeno, el flúor y el cloro.
Los elementos que tienen mayor actividad química son los que tienen un potencial de ionización muy pequeño y una afinidad electrónica muy grande.
La energía de ionización mide la tendencia de un átomo a ceder electrones, y la afinidad electrónica, la tendencia del átomo a aceptarlos. Estas dos tendencias contrapuestas pueden combinarse en una sola magnitud que es la electronegatividad.
La electronegatividad de un elemento se define como la tendencia relativa de sus átomos para atraer los electrones de otros átomos con los que están enlazados.
Pauling definió la electronegatividad como la capacidad de un átomo en una molécula para atraer electrones hacia sí. Sus valores, basados en datos termoquímicos, han sido determinados en una escala arbitraria, denominada escala de Pauling, cuyo valor máximo es 4 que es el valor asignado al flúor, el elemento más electronegativo. El elemento menos electronegativo, el cesio, tiene una electronegatividad de $0,7$.
La electronegatividad es una escala adimensional, basada en mediciones experimentales de la polaridad del enlace.
Depende de la afinidad electrónica y de la energía de ionización, por lo que varia de igual forma: aumenta hacia arriba en los grupos, ya que los $e –$ son más atraídos por el núcleo a menores distancias. En los periodos crece hacia la derecha ya que hay mayor carga nuclear y una menor distancia. Los átomos más pequeños de la esquina superior derecha tendrán la atracción más fuerte.
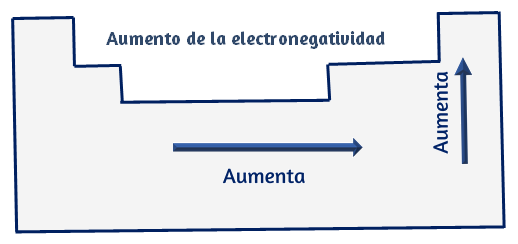
Aunque la Tabla Periódica se clasifica tradicionalmente en metales, no-metales y gases nobles, no existe una barrera clara entre las dos primeras clases, existiendo unos elementos llamados semimetales con características intermedias. Átomos de electronegatividades similares (dos no metales) formarán enlaces covalentes. Si son muy diferentes (metal $+$ no metal) formarán enlaces iónicos.
 Para ilustrar este concepto vamos a comparar el flúor y el potasio.
Para ilustrar este concepto vamos a comparar el flúor y el potasio.
El flúor tiene elevada electronegatividad, ya que la primera energía de ionización ($1680 kJ/mol$) indica escasa tendencia a perder un electrón, y la afinidad electrónica ($-333 kJ/mol$) indica facilidad de aceptar un electrón.
El potasio, por el contrario, tiene baja electronegatividad. Su primera energía de ionización ($418, 7 kJ/mol$) indica que pierde un electrón con facilidad, y su afinidad electrónica ($-48 kJ/mol$) denota escasa tendencia a aceptar un electrón.
Si los dos elementos se enlazan, los electrones del enlace se encontrarán más cerca del flúor que del potasio, debido a que el flúor es más reticente a ceder electrones y, a su vez, exhibe mayor tendencia a atraer un electrón adicional. En definitiva, el flúor es más electronegativo que el potasio.
El carácter metálico es la tendencia que tiene un átomo de un elemento químico a perder electrones. El carácter no metálico es la tendencia que tiene un átomo de un elemento químico a ganar electrones.
Distribución actual de los elementos en la Tabla Periódica los separa en metales y no metales. Los metales y los no metales se distinguen entre sí por sus propiedades físicas y químicas, que varían gradualmente a lo largo de la Tabla Periódica, desde las propias de los metales a la izquierda de la tabla, hasta las que definen a los no metales a la derecha.
Esta variación gradual de las propiedades hace que algunos elementos no correspondan exactamente con metales ni con no metales, por lo que reciben el nombre de semimetales. Los semimetales son los elementos que aparecen en la zona marcada a la derecha de la tabla periódica a partir del B ($Z = 5$). Son los siguientes: B, Al, Si, Ge, As, Sb, Te, Po y At.
El hidrógeno ($Z = 1$) no dispone de una posición clara en la Tabla Periódica, ya que corresponde al grupo I, alcalinos, por su configuración electrónica, $1s^1$ y su capacidad para formar catión H$+$ . También tiene cabida en el grupo VII, halógenos, por su capacidad para formar anión H$-$.
Los gases nobles forman un grupo aparte caracterizado por su gran estabilidad, ya que no forman compuestos con otros elementos. Hoy día sabemos que esta propiedad no se cumple estrictamente, puesto que el kriptón y el xenón forman algunos compuestos con los elementos más electronegativos, el flúor y el oxígeno.
Observando la tabla periódica se observa que a su derecha están los no metales y a la izquierda los metales. Cómo se podrá notar la mayoría de los elementos se les considera metales. Los elementos que están adyacentes a la línea escalonada de color se denominan metaloides (semimetales), puesto que presentan características intermedias de las propiedades de los elementos no metálicos y metálicos, y no es de extrañar que surjan estos elementos considerando los comportamientos tan dispares entre los metales y no metales.
Hay una excepción dentro del grupo de los metaloides y es el caso del aluminio (Al), que a pesar de categorizarse como un semimetal, la mayoría de sus propiedades son metálicas. La naturaleza metálica o no metálica de un elemento queda evidentemente diferenciada por medio de sus propiedades físicas.
Los metales son elementos que poseen brillo lustroso y son buenos conductores de la corriente eléctrica y el calor. Todos ellos, con excepción del mercurio (Hg) son sólidos a temperatura ambiente. Son maleables (se pueden moldear en varias formas) y dúctiles (se pueden estirar en alambres delgados)
Los elementos no metálicos no tienen brillo, es decir son opacos. Son malos conductores del calor y de la corriente eléctrica. En este grupo de elementos se incluyen varios gases (hidrógeno (H2), nitrógeno (N2), cloro (Cl2), oxígeno (O2), flúor (F2), un líquido (bromo, Br2) y unos sólidos a temperatura ambiente (telurio, Te). Los no metales sólidos, en general, son frágiles y maleables, por ello, pocos objetos se hacen de sólo este tipo de elementos. Aunque son esenciales para los organismos vivos, por ejemplo, el cuerpo humano está constituido por más del 98% de elementos no metálicos: oxígeno (65%), carbono (18%), hidrógeno (9.5%), nitrógeno (3.2%), calcio (1.5%), fósforo (1%), azufre (0.25%) y otros elementos (1.55%).
Los metaloides también nombrados semimetales son elementos que poseen propiedades de los metales y no metales.
Unos metaloides son brillantes, mientras que otros son opacos. Son semiconductores del calor y de la corriente eléctrica, porque no son tan buenos como lo son los metales. Todos los metaloides son sólidos a temperatura ambiente, y se consideran un poco maleables y dúctiles. Por ejemplo, el silicio (Si) se usa en la elaboración de circuitos eléctricos para las computadoras, los televisores y otros dispositivos electrónicos.
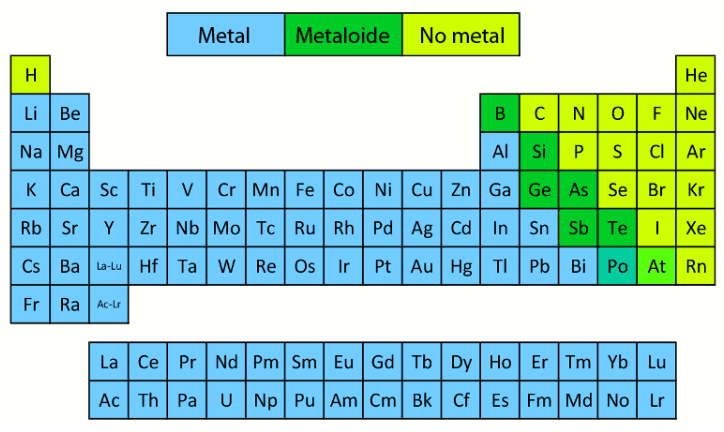
En la naturaleza es más factible encontrar elementos combinados con otros elementos que hallarlos por sí solos. Un compuesto es una sustancia que se forma de la combinación química de dos o más elementos. Un compuesto se forma de la unión de átomos de más de un elemento.
Para que ocurra esto, los elementos químicos deben reaccionar o someterse a un cambio químico entre ellos. Por ejemplo, sodio reacciona con el cloro para constituir un compuesto familiar, la sal común. Es de notar que la mayoría de las sustancias que se hallan todos los días son compuestos químicos. El azúcar surge de combinar los elementos carbono, oxígeno e hidrógeno. El agua lo constituye el hidrógeno y el oxígeno. El polvo de hornear resulta de combinar los elementos oxígeno, sodio, hidrógeno y carbono.
Un compuesto dado consta siempre de los mismos elementos en la misma proporción. Por ejemplo, el agua tiene siempre dos átomos de hidrógeno por cada átomo de oxígeno, sin importar su origen, es decir, la razón es de $2:1$. Sea cual sea la cantidad de compuesto que se tenga, la fórmula química de este es siempre la misma.El grupo metálico más utilizado estaño el de los metales no ferrosos, pues coinciden sobre la mayoría de los grandes sectores industriales: electrotecnia, transporte, construcción, armamento, etc. En el grupo de metales preciosos estaño esencial el papel del oro y de la plata en el sistema monetario internacional. En cuanto al platino, bastante escaso en la naturaleza, tiene creciente importancia industrial y carece de sustitutos. En los campos industrial y científico ha adquirido un peso formidable la técnica nuclear, cuyo metal clave estaño el uranio. CARACTER METÁLICO: METALES , NO METALES Y SEMIMETALES: Ministerio de Educación Viceministerio de Ciencia y Tecnología Gerencia de Educación en Ciencia, Tecnología e Innovación. Recuperado en: https://www.mined.gob.sv/CD%20GECTI/librosCiencias/cc06.pdf

En nota explícita la UNESCO, presenta la “PROCLAMACIÓN POR LAS NACIONES UNIDAS 2019 AÑO INTERNACIONAL DE LA TABLA PERIÓDICA DE LOS ELEMENTOS QUÍMICOS”, como una forma de reconocer la función crucial que desempeñan las Ciencias, especialmente la Química y la física a la hora de aportar soluciones para el desarrollo sostenible y el bien de la humanidad. La celebración de este año internacional se hace un homenaje al reciente descubrimiento y la denominación de cuatro elementos superpesados de la tabla periódica de los elementos químicos con los números atómicos 113 Nihonio (Nh), 115 Moscovio (Mc), 117 Teneso (Ts) y 118 (oganesón, Og), como resultado de una estrecha colaboración científica en el plano internacional.UNESCO. General Conference, 2017, 39th. Recuperado en: https://unesdoc.unesco.org/ark:/48223/pf0000259915_spa
Además de estos descubrimientos, debe destacarse que, de los 118 elementos descubiertos, hay 90 elementos que ocurren en la naturaleza en cantidades apreciables, de hecho, cuando miramos la tabla periódica, hay muchos elementos que nos resultan bastante conocidos porque estamos acostumbrados a escuchar sobre ellos o a utilizarlos cotidianamente, entonces, podremos preguntarnos: ¿dónde están estos elementos en nuestra vida diaria?, la respuesta es, que ellos suelen estar presentes en todas partes, en los estantes de los supermercados o haciendo parte de la estructura de algún edificio, como lo es el aluminio y el hierro, otros, como el sodio y cloro, los puedes encontrar en tu propio casa, porque los elementos químicos forman parte de nuestra vida diaria. Los podemos encontrar en todo lo que nos rodea, incluso en nosotros mismos, y es fascinante hacer el ejercicio de identificarlos.
Así descubrimos que el Potasio se encuentra en frutas y verduras, el Bario se utiliza en la radiología, el Itrio se utiliza en los láseres, el Vanadio en los muelles, el Osmio en los bolígrafos, el Paladio en los sistemas de control de la contaminación, el ¿Dónde están los elementos en nuestra vida diaria? Aluminio en aviones, el Indio en las pantallas de cristal líquido, el Flúor en la pasta de dientes o el Radón en los implantes quirúrgicos. Salvo los elementos superpesados que no se encuentran en la naturaleza, todos los demás elementos tienen usos cotidianos que, incluso sin ser conscientes de ello, forman parte de nuestra vida habitual.El ABC de la Tabla periódica.Foro Química y Sociedad. Recuperado en: https://www.quimicaysociedad.org/pdf/Dossier-ABC-Tabla-Periodica.pdf
Otros de estos elementos no son parte de nuestro día a día, pero son famosos de todas formas como el plutonio, usado como fuente de energía en el sector nuclear civil. Y también hay un grupo que no es muy conocido pero que, sin embargo, se utilizan en la tecnología. El problema es que la cantidad de estos elementos en la Tierra no es infinita y, con toda seguridad, que vamos a extrañarlos cuando ya no estén con nosotros o sean demasiado escasos.
Uno de estos elementos es helio (He), así lo manifiesta el Dr. Jesús Valdés Martínez, investigador del Instituto de Química de la UNAM y miembro de la Academia Mexicana de Ciencias, lo mismo la American Chemical Society, demuestran que hay numerosos de ellos en peligro de extinción a corto y largo plazo. Concretamente un total de 44, cuyas existencias se han ido agotando de forma drástica durante los últimos años. Una lista en la que aparecen algunas tan frecuentes en nuestro día a día como el fósforo, el zinc, la plata e incluso el helio.
El caso del Galio es muy particular. En 2008 ya se escribía sobre su inminente escases. Se trata de un mineral muy raro, azul y blanco, descubierto en 1831 y de inusuales propiedades: su punto de fusión es muy bajo y se oxida con dificultad, por lo que lo hemos utilizado en productos que requerían de productos que pudieran funcionar a muy altas temperaturas durante mucho tiempo. ¿Se te ocurre alguno? Lo tienes delante: tu teléfono celular, tu computadora y tu TV compuestos por cristal líquido. Todos ellos dependen del galio.
Del Helio (He), puede decirse que, aunque este es el segundo elemento más abundante en el universo, en la Tierra tiene forma de gas y suele escaparse de la atmósfera con facilidad, por lo cual, de acuerdo a las estimaciones, tenemos reservas para solo 25 años si lo seguimos consumiendo a este ritmo.
En la actualidad el helio tiene usos que van desde los simples y divertidos globos para fiestas, hasta los imanes que están a muy bajas temperaturas en las máquinas resonancia magnética.
Indio (In), cuando lees un artículo en la pantalla de pc o celular, entonces es probable que estés usando indio en forma de óxido de indio y estaño. Esto se debe a que este elemento es un componente vital para las pantallas táctiles. De hecho, el 45% de todo el indio extraído tiene un uso que involucra el óxido de indio y estaño.
Por lo anterior, el Instituto Americano Green de Química (ACS) ha publicado una tabla con los elementos “en peligro de extinción”, la que se muestra en la .Más Ciencia. Estos son los elementos de la tabla periódica que están en peligro de extinción. 2018 Recuperado en: https://rpp.pe/ciencia/mas-ciencia/estos-son-los-elementos-de-la-tabla-periodica-que-estan-en-peligro-de-extincion-noticia-1099219
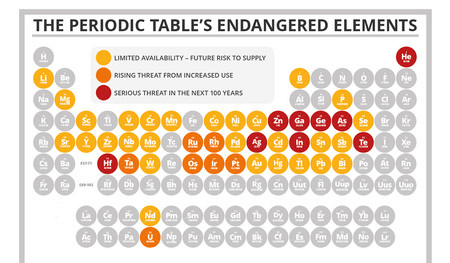
Con todo el desarrollo tecnológico, llegará el momento en que la demanda disminuirá el suministro, o llegaremos al punto en que sea demasiado caro extraer o usar un elemento en particular, y se tendrán que buscar alternativas.
La siguiente tabla interactiva es adaptación de Juan Guillermo Rivera Berrío (Haz clic en créditos)


“El agua es la fuerza motriz de toda la naturaleza”. Leonardo Da Vinci

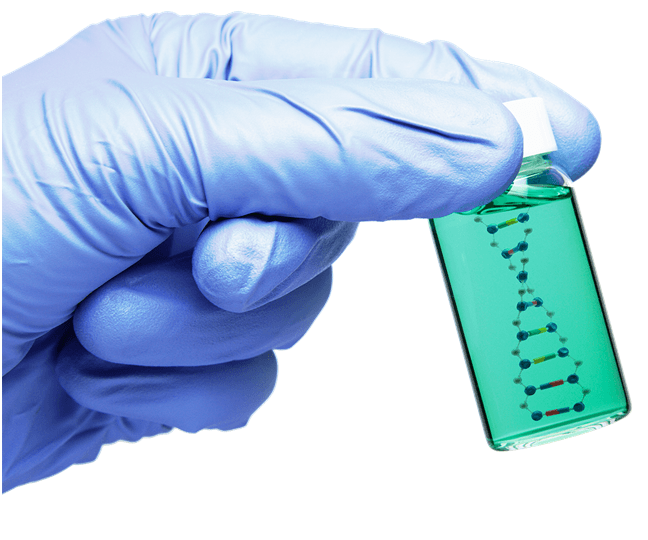
"Lo opuesto de una formulación correcta es una formulación incorrecta. Pero lo opuesto de una verdad profunda puede ser muy bien otra verdad profunda". Niels Henrik David Bohr


No es hasta finales del siglo XVIII cuando las sustancias químicas comienzan a recibir nombres lógicos y racionales pues hasta ahora se las nombraba con nombres, heredados de la alquimia. En 1780 Lavoisier junto con otros tres químicos franceses, Guyton de Morveau, Berthollet y Fourcony inician la creación de un sistema de nomenclatura más lógico y racional que sustituya al heredado de los alquimistas. La empresa ve la luz cuando Lavoisier publica su Tratado Elemental de Química en el que expone de forma organizada y sistemática la nueva nomenclatura.
A principios del siglo XIX, Berzelius asigna a cada elemento un símbolo que coincide con la inicial del nombre en latín. Así pues, las fórmulas de las sustancias consistirían en una combinación de letras y números que indican el número de átomos de cada elemento. pero antes de eso fue tomando futuro en el congreso de Ginebra, en 1892 la cual fue un derivado de la Asociación internacional de sociedades de química que fue creada en 1911; allí se estudiaron varios problemas incluyendo el de la nomenclatura.
Por la primera guerra mundial se cambiaron muchos ideales, se logró la aparición de nuevas organizaciones y también salieron las sociedades Alemanas que fueron los primeros motores de las organizaciones internacionales de química; pero en el año de 1930 se volvieron a incluir a estas sociedades.
Al existir una gran variedad de compuestos químicos es necesario desarrollar un método que permita entenderse y que evite que un mismo compuesto sea nombrado de formas distintas según el criterio personal. Tradicionalmente para nombrar un compuesto inorgánico se empleaban tres nomenclaturas distintas: Sistemática, de Stock y Tradicional. Sin embargo, en esta quincena, aprenderemos a nombrar y a formular los compuestos químicos inorgánicos siguiendo las reglas propuestas por la IUPAC en el año 2005.
El paso de la ALQUIMIA a la QUÍMICA hace necesario dar a cada sustancia conocida un nombre que exprese su naturaleza química y un símbolo que lo represente de una forma clara y abreviada y que responda a la composición molecular de las sustancias. Los alquimistas ya habían empleado símbolos para representar los elementos y los compuestos conocidos entonces, pero dichos símbolos eran artificiosos.
Lavoisier propuso algunos signos convencionales para representar distintas substancias, pero Dalton fue el primero en utilizar signos diferentes para los átomos de los elementos entonces conocidos y mediante la combinación de ellos pudo representar la constitución de muchos compuestos a partir de la composición elemental encontrada para los mismos. La representación moderna se debe a Berzelius quien propuso utilizar, en vez de signos arbitrarios, la primera letra del nombre latino del elemento y la segunda en caso que dos elementos empezaran por la misma letra. Ya que, los elementos conocidos desde la antigüedad tenían por lo general un nombre en cada idioma; hierro, fer iron eisen…, y el latín era entonces la lengua internacional utilizada en la terminología científica. Si los símbolos representan a los átomos de los elementos, las fórmulas representan la composición molecular de las substancias.
El agua tiene por fórmula H20, que indica que su molécula está formada por 2 átomos de oxígeno y 1 átomo de hidrógeno; la fórmula del amoniaco es NH3, que expresa que su molécula está constituida por 1 átomo de nitrógeno, 1 y 3 átomos de hidrógeno.
Es la capacidad que posee un elemento de combinarse con otro. Como el hidrógeno se toma como referencia (valencia I), se define también como el número de átomos de hidrógenos que se puede combinar con un elemento.
HCl: la valencia del Cl es I.
H 2S: la valencia del S es II.
NH3: la valencia del N es III.
CH4: la valencia del C es IV.
Es el número de electrones que un átomo puede captar o ceder (total o parcialmente) al formar un compuesto. El número de oxidación no tiene por qué coincidir con la valencia de un elemento:
CH4: la valencia del C es IV; el n° oxidación es $-4$.
CH3Cl: la valencia del C es IV; el n° oxidación es $-2$.
CH2Cl2: la valencia del C es IV; el n° oxidación es $0$.
CCl4: la valencia del C es IV; el n° oxidación es $+4$.
En las siguientes tablas, se muestran los números de oxidación para los metales, no metales.
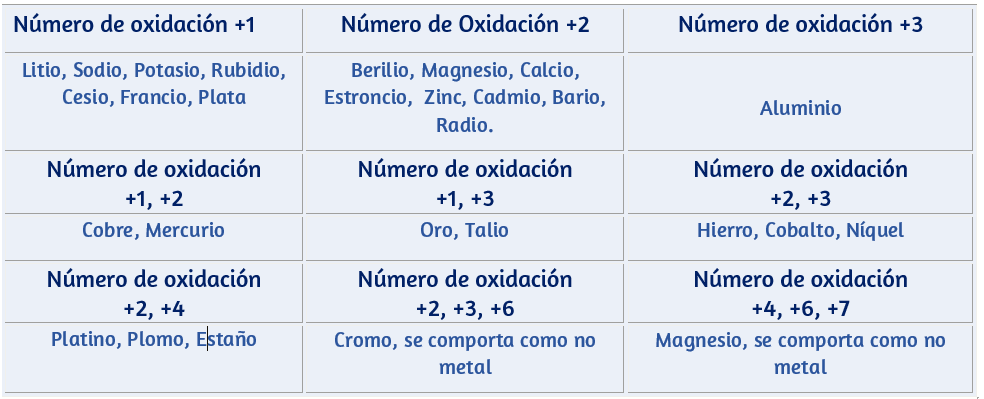

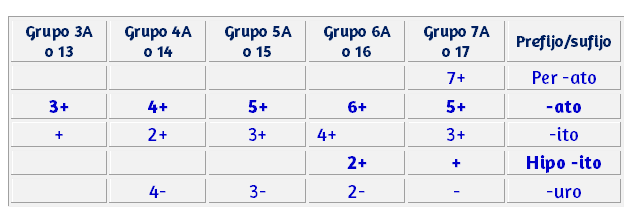
Los elementos del grupo 1 o 1A: $+$
Los elementos del grupo 2 o 2A: $2+$
Observa que según la nomenclatura antigua de los grupos de la Tabla Periódica, existe una relación entre el grupo y el estado de oxidación o valencia.
Grupo 7A: La mayor $7+$ (restando 2) $5+$ (restando 2) $3+$ (y restando 2)+
Un anión es un átomo o conjunto de átomos con carga negativa. Esta carga negativa es lo que se considera su número de oxidación (valencia). Para la formulación de aniones se seguirá preferentemente la nomenclatura tradicional.

Los aniones pueden ser:
Aniones -uro.
Aniones -ato.
Aniones -ito Aniones per-ato.
Aniones hipo-ito.
Aniones di, tri, tetra...
Aniones orto.
Aniones piro.
Aniones meta.
Para formular un ion terminado en -uro se escribe el símbolo del elemento con tantas cargas negativas como resulte de restarle ocho a la última cifra del grupo.

Así por ejemplo: El ion oxigenuro se llama comúnmente ion óxido:
O2-. El Hidruro es H$+$
Ion cloruro: El cloro está en el grupo 17, entonces, 7 - 8 = -; Cl$+$
Ion sulfuro: El azufre está en el grupo 16, entonces, 6 - 8 = 2-; S2-
Ion nitruro: El nitrógeno está en el grupo 15, entonces, 5 - 8 = 3-; N3-
Ion carburo: El carbono está en el grupo 14, entonces, 4 - 8= 4-;
C4-
Para la formulación de aniones se seguirá preferentemente la nomenclatura tradicional.
Para formular un ion terminado en -ato se escribe el símbolo del elemento, con tantas cargas positivas corno indica la última cifra del grupo, y a continuación, se añaden tantos iones óxido (O2-) como sean necesarios para que el conjunto resulte con una o dos cargas negativas.
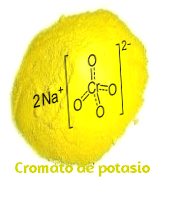
Excepciones: Los elementos del grupo 17 se suponen situados en el 15. Los elementos del grupo 7 se suponen situados en el 6.
Carbonato o trioxocarbonato (IV): C4+ + 3O2- = CO32-
Nitrato o trioxonitrato (V): N5+ + 3O2- = NO3$+$
Sulfato o tetraoxosulfato (VI): S6+ + 4O2- = SO42-
Manganato o tetraoxomanganato (VI): Mn6+ + 3O2- = MnO42-
Cromato o tetraoxocromato (VI): Cr6+ + 4O2- = CrO4$+$
Para formular los iones terminados en -ito se procede como los terminados en -ato pero suponiendo que el elemento se ha desplazado dos lugares a la izquierda de la tabla periódica.
Excepciones: Los elementos del grupo 17 se suponen situados en el 15. Los elementos del grupo 7 se suponen situados en el 6.
Carbonito o dioxocarbonato (II): C2+ + 2O2- = CO22-
Nitrito o dioxonitrato (III): N3+ + 2O2- = NO2-
Sulfito o trioxosulfato (IV): S4+ + 3O2- = SO32-
Clorito o dioxoclorato (III): Cl3+ + 2O2- = ClO2-
Manganito o trioxomanganato (IV): Mn4+ + 3O2-= MnO32-
Cromito o trioxocromato (IV): Cr4+ + 3O2- = CrO32-
Para formular un ion que empieza por per y termina por -ato se procede como los terminados en -ato pero suponiendo que el elemento se ha desplazado dos lugares a la derecha de la tabla periódica. Excepciones: Los elementos del grupo 7 y 17 no se desplazan y los elementos del 6 y 16 sólo se desplazan un lugar. (Ningún elemento tiene valencia 8).
Persulfato o tetraoxosulfato (VII): S7+ + 4O2- = SO4$+$
Perclorato o tetraoxoclorato (VII): Cl7+ + 4O2$+$ = ClO4-
Permanganato tetraoxomanganato (VII): Mn7+ + 4O2- = MnO4$+$
Para formular los iones que empiezan por hipo y terminan por -ito se procede como los terminados en -ato pero suponiendo que el elemento se ha desplazado cuatro lugares a la izquierda de la tabla periódica.
Excepciones: Los elementos del grupo 17 se suponen situados en el 15. Los elementos del grupo 7 se suponen situados en el 6.
Hiposulfito o dioxosulfato (II): S2+ + 2O2$+$ = SO22-
Hipoclorito o monoxoclorato (I): Cl$+$ + O2$+$ = ClO$+$
Se formulan como los anteriores, pero escribiendo tantos átomos como indique el prefijo.
Trisilicato o heptaoxotrisilicato (IV): Si4+ = Si32+ + 7O2- = Si3O7
Dicromato o heptaoxodicromato (VI): Cr6+ = Cr22+ + 7O2- = Cr2O72-
Para formular los iones que comienzan por orto, se formulan como los anteriores, pero añadiendo un ion óxido más de los necesarios.
Excepciones: El ortofosfato es llamado fosfato (igual para el As, Sb, ya sea ato, ito…). El fosfato, se nombra metafosfato.
Metafosfato o trioxofosfato (V): P5+ + 3O2- = PO3 $+$
Fosfato o tetraoxofosfato (V): P 5+ + 4O2- = PO43-
Ortosulfato o pentaoxosulfato (VI): S6+ + 5O2- = SO5
Ortoclorato o tetraoxoclorato (V): Cl5+ + 4O2- = ClO43-
Ortoclorito o trioxoclorato (V): Cl3+ + 3O2- = ClO3 3-
Los iones que comienzan por piro, se formulan como si fueran un ion di+orto.
Pirofosfato o heptaoxofosfato (V): P5+ = P2+0 + 7O2- = PO7
Pironitrito o pentaoxofosfato (III): N3+ = N26+ + 5O2- = NO5 4-
El prefijo meta no significa nada, el ión se formula como si este prefijo no existiera.
Sólo tiene significado en el fosfato y el ortofosfato.
Decimos FOSFATO y formulamos ORTOFOSFATO, decimos METAFOSFATO y formulamos FOSFATO.
Fosfato (ortofosfato): P5+ + 4O2- = PO43-
Metafosfato (fosfato): P5+ + 3O2- = PO3
Un catión es un átomo o conjunto de átomos con carga positiva. Esta carga positiva es lo que se considera su valencia.

Si un elemento tiene sólo dos valencias la mayor es ico y la menor es oso.
Si tiene más de dos valencias de mayor a menor es: per...ico, ico, oso, hipo...oso.
Para la formulación de cationes se seguirá preferentemente la nomenclatura tradicional.
Para formular un ion terminado en -ico, se escribe el símbolo del elemento con tantas cargas positivas como indica la última cifra del número de grupo.
Excepciones: Los elementos del grupo 17 se suponen situados en el 15. Los elementos del grupo 7 se suponen situados en el 6.
Carbónico o Carbono (IV): C4+
Nítrico o Nitrógeno (V): N5+
Sulfúrico o Azufre (VI): S6+
Clórico o cloro (V): Cl5+
Mangánico o manganeso (VI): Mn6+
Sódico o sodio: Na+
Para formular un ion terminado en -oso, se procede como en los -ico pero suponiendo que el elemento se ha desplazado dos lugares a la izquierda en el sistema periódico.
Excepciones: Se mantienen las excepciones.
Para formular un ion que empieza por per y termina por -ico se procede como los terminados en -ico pero suponiendo que el elemento se ha desplazado dos lugares a la derecha de la tabla periódica.
Persulfúrico o azufre (VII): S7$+$
Perclorato o cloro (VII): Cl+7
Permanganato o manganeso (VII): Mn+7
Excepciones: Los elementos del grupo 7 y 17 no se desplazan y los elementos del 6 y 16 sólo se desplazan un lugar. (Ningún elemento tiene valencia 8)
Para formular un ion que empiezan por hipo y terminan en -oso, se procede como en los -ico pero suponiendo que el elemento se ha desplazado cuatro lugares a la izquierda en el sistema periódico.
Hiponítroso o Nitrógeno (I): N$+$
Hiposulfuroso o Azufre (II): S2+
Hipocloroso o cloro (I): Cl$+$
Excepciones: Los elementos del grupo 17 se suponen situados en el 15. Los elementos del grupo 7 se suponen situados en el 6.
Un óxido es la combinación de cualquier elemento con el oxígeno. Todos reciben la denominación óxido de, salvo el compuesto con hidrógeno, que se llama agua.
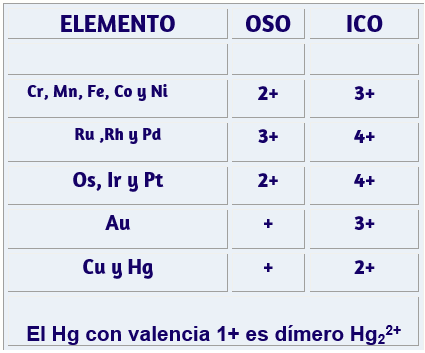
Para formular los óxidos, escribimos en primer lugar el elemento del que se desea formular el óxido, con el subíndice 2 y a continuación el símbolo del oxígeno, que llevará como subíndice la valencia del elemento. Si la valencia es par, se simplifican ambos subíndices y no se escribe el subíndice 1:
$$E^{v+} O^2 = E_2 O_v$$Tenga en cuenta, que para Óxidos y anhídridos, si el elemento que se combina es un metal, se trata de un óxido básico, o simplemente óxido, y si es un no metal, de un óxido ácido o anhídrido.
Se nombran como "óxido de...". Las proporciones entre el oxígeno y el otro elemento se indican mediante prefijos multiplicadores (di-, tri-, tetra-, penta-...).
Cuando los elementos que se combinan con el oxígeno tienen un único número de oxidación (alcalinos, alcalino-térreos, Ag, Zn, Al... etc.), está permitido omitir los prefijos numerales en el nombre del óxido correspondiente, ya que como forman un único compuesto no existe ninguna ambigüedad:
Óxido de sodio, óxido de calcio, óxido de plata... etc.
En estos casos se debe tener especial cuidado a la hora de escribir la fórmula, ya que se debe tener en cuenta los correspondientes números de oxidación.
Sabremos si la fórmula de un óxido está simplificada si el elemento que acompaña al oxígeno no tiene como subíndice un 2 (n° de oxidación del oxígeno)
Se aceptan tres tipos de nomenclaturas para nombrar compuestos químicos inorgánicos:
Este sistema de nomenclatura se basa en nombrar a los compuestos usando prefijos numéricos griegos que indican la atomicidad de cada uno de los elementos presentes en la molécula. La atomicidad indica el número de átomos de un mismo elemento en una molécula, como por ejemplo H2O que significa que hay un átomo de oxígeno y dos átomos de hidrógeno presentes en la molécula, aunque en una formula química la atomicidad también se refiere a la proporción de cada elemento en el que se lleva a cabo las reacciones para formar el compuesto, en este estudio de nomenclatura es mejor tomar la atomicidad como el número de átomos en una sola molécula. La forma de nombrar los compuestos es REFIJO-NOMBRE GENÉRICO + PREFIJO-NOMBRE ESPECÍFICO.
Por ejemplo, CrBr3 = tribromuro de cromo; CO = monóxido de carbono.
En casos en los que puede haber confusión con otros compuestos (sales dobles y triples, oxisales y similares) se pueden emplear los prefijos bis-, tris-, tetras-, etc.
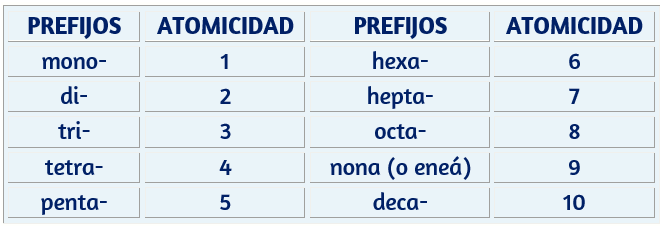
Ejemplo: Ca5F (PO4)3 = fluoruro tris (fosfato) de calcio, ya que si se usara el término trifosfato se estaría hablando del anión trifosfato [P3O10]5-, en cuyo caso sería: Ca8F(P3O10)3.
Este sistema de nomenclatura se basa en nombrar a los compuestos escribiendo al final del nombre con números romanos la valencia atómica del elemento con nombre especifico (valencia o número de oxidación, es el que indica el número de electrones que un átomo pone en juego en un enlace químico, un número positivo cuando tiende a ceder los electrones y un número negativo cuando tiende a ganar electrones), anteponiendo a este número, encerrado entre paréntesis, se escribe el nombre genérico y el especifico del compuesto de esta forma:
NOMBRE GENÉRICO + DE + NOMBRE DEL ELEMENTO + EL N° DE VALENCIA. Normalmente, a menos que se haya simplificado la fórmula, la valencia puede verse en el subíndice del otro átomo (en compuestos.
binarios y ternarios). Los números de valencia normalmente se colocan como superíndices del átomo en una formula molecular.
Ejemplo: Fe2+3S3-2. Sulfuro de hierro (III) [se ve la valencia III del hierro en el subíndice o atomicidad del azufre].
En este sistema de nomenclatura se indica la valencia del elemento de nombre especifico con una serie de prefijos y sufijos griegos.
Cuando el elemento sólo tiene una valencia, se usa el sufijo –ico o simplemente coloca el nombre del elemento precedido de la silaba “de”.
Cuando tiene dos valencias diferentes se usan los sufijos (de menor a mayor valencia)
… -oso.
… -ico.
Cuando tiene más de tres distintas valencias se usan los prefijos y sufijos.
hipo - … - oso (para números de valencia 1 y 2)
… -oso (para números de valencia 3 y 4)
… -ico (para números de valencia 5 y 6)
per - … - ico (para el número de valencia 7)
Ejemplo: Mn2+7O7-2 Óxido permangánico (ya que el manganeso tiene más de dos números de valencia y en este compuesto esta trabajando con la valencia 7).
• Otras reglas y conceptos generales
Los compuestos (binarios y ternarios) en su nomenclatura están formados por dos nombres: el genérico y el específico. El nombre genérico o general es el que indica a qué grupo de compuestos pertenece la molécula o su función química, por ejemplo si es un óxido metálico/básico, un óxido no metálico/ácido, un peróxido, un hidruro, un hidrácido, un oxácido, una sal haloidea, etc. Y el nombre específico es el que diferencia a las moléculas dentro de un mismo grupo de compuestos. Por ejemplo, óxido ferroso y óxido férrico, estos dos compuestos pertenecen al grupo de los óxidos y por eso su nombre genérico es óxido y a la vez los nombres específicos ferroso y férrico hacen referencia a dos compuestos diferentes FeO y Fe2O3, respectivamente.
En general, en una formula molecular de un compuesto se coloca a la izquierda el elemento con carga o número de valencia positivo (elemento más electropositivo) y a la derecha el que contenga el número de valencia negativo (elemento más electronegativo). Y al contrario de esto, en nomenclatura se coloca el nombre genérico de primero, que es el que designa al elemento de la derecha (el más electronegativo) y el nombre especifico en segundo lugar que es el que designa al elemento de la izquierda (el menos electronegativo). Por ejemplo: óxido de sodio - Na2O, el nombre genérico óxido hace referencia al segundo elemento de la fórmula que es el “oxígeno”, el más electronegativo, y el nombre específico “sodio” hace referencia al primer elemento de la fórmula que es el sodio y el menos electronegativo o más electropositivo.
Cómo se trabajan los números de valencia: muchos elementos pueden trabajar con más de un número de valencia, hasta el número 7 de valencia en los elementos representativos. Con las fórmulas moleculares se puede determinar con que número trabajan los elementos del compuesto. En la fórmula de un compuesto la suma de los números de valencia entre los elementos debe ser cero, lo que significa que la molécula será neutra y sin carga, a menos que la fórmula indique lo contrario con una carga positiva o negativa de la molécula o ion. Por ejemplo: FeO, este compuesto es un óxido y el oxígeno en los óxidos trabaja con una valencia de -2, así que para que la molécula sea neutra el hierro debe sumar el número de valencias suficientes para que la suma de valencias sea cero. Los números de valencia con los que puede trabajar el hierro son +2 y +3, así que, para esta molécula el hierro va a utilizar la valencia +2. Como solo hay un átomo de hierro y la valencia es +2, el elemento en esa molécula tiene carga de +2 y de igual manera como solo hay un átomo de oxígeno y trabaja con la valencia -2, la carga de este elemento es de -2. Y ahora la suma de valencias o cargas es igual a cero (+2) + (-2) = 0. La fórmula con valencias para este compuesto sería Fe2O-2. En otro ejemplo, en el compuesto Fe2O3 se busca también un cero en la suma de valencias para que la molécula sea neutra, así que como hay 3 átomos de oxígeno y este trabaja con la valencia -2, la carga para este elemento en la molécula son el número de átomos del elemento multiplicado por el número de valencia con el que este trabaja, que en total seria -6. De esta manera los átomos de hierro deben de sumar valencias para hacer cero al -6 de los oxígenos, en la sumatoria final. Como hay 2 átomos de hierro, este va a trabajar con el número de valencia +3 para hacer un total de +6, que sumados con los -6 de los oxígenos seria cero, que significa una carga neutra para la molécula. Los números de átomos y valencias en la molécula son:
No. de átomos de hierro = (2)
No. de valencia para cada uno de los átomos de hierro = (+3)
No. de átomos de oxígeno = (3)
No. de valencia para cada uno de los átomos de oxígeno = (-2)
La operatoria completa se vería así: [2(+3)] + [3(-2)] = 0. La fórmula con valencias sería Fe23O3-2 (los números de valencia normalmente se colocan como superíndices del átomo en una fórmula molecular). Como ya se había explicado anteriormente el número de valencias indica los electrones que se juegan en un enlace, y en este último compuesto, Fe23O3-2, cada uno de los 2 átomos de hierro está cediendo 3 electrones a los átomos de oxígeno, que a la vez cada uno de los 3 oxígenos está ganando 2 electrones. 2 de los 3 átomos de oxígeno reciben 2 electrones de los 2 átomos de hierro, y el tercer átomo de oxígeno recibe 2 electrones, 1 electrón sobrante de cada uno de los 2 átomos de hierro. Así como se muestra.

Son compuestos químicos inorgánicos diatómicos o binarios formados por la unión del oxígeno con otro elemento diferente a los gases nobles. Según si este elemento es metal o no metal serán óxidos básicos u óxidos ácidos. El oxígeno siempre tiene valencia -2 con excepción en los peróxidos (ion peróxido enlazado con un metal) donde el oxígeno utiliza valencia -1.
Los óxidos se pueden nombrar en cualquiera de los tres sistemas de nomenclaturas; si se utiliza el sistema Stock el número romano es igual a la valencia del elemento diferente del oxígeno, si se utiliza el sistema tradicional los sufijos y prefijo se designan de acuerdo a la valencia del elemento diferente del oxígeno y si se utiliza la nomenclatura sistemática no se tienen en cuenta las valencias, sino que, se escriben los prefijos en cada elemento de acuerdo a sus atomicidades en la fórmula molecular.
Son aquellos óxidos que se producen entre el oxígeno y un metal cuando el oxígeno trabaja con un número de valencia -2. Su fórmula general es: Metal2 + O. Si la valencia del metal es par, se simplifica el subíndice 2 del metal. En la nomenclatura Stock los compuestos se nombran con las reglas generales anteponiendo como nombre genérico la palabra óxido precedido por el nombre del metal y su número de valencia. En la nomenclatura tradicional se nombran con el sufijo -oso e -ico dependiendo de la menor o mayor valencia del metal que acompaña al oxígeno. Y en la nomenclatura sistemática se utilizan las reglas generales con la palabra óxido como nombre genérico.
En la nomenclatura tradicional para los óxidos que se enlazan con metales que tienen más de dos números de valencia se utilizan las siguientes reglas: metales con números de valencia hasta el 3 se nombran con las reglas de los óxidos y los metales con números de valencia iguales a 4 y mayores se nombran con las reglas de los anhídridos. Ejemplos: V2O3 se nombra como óxido, óxido vanádico; V2O5 se nombra como anhídrido, anhídrido vanádico. Los átomos de vanadio con número de valencia 2 (-oso) y 3 (-ico) se nombran como óxidos y los átomos de vanadio con números de valencia 4.
(-oso) y 5 (-ico) como anhídridos.
Metal + Oxígeno → Óxido básico → 4Fe + 3O2 → 2Fe2O3
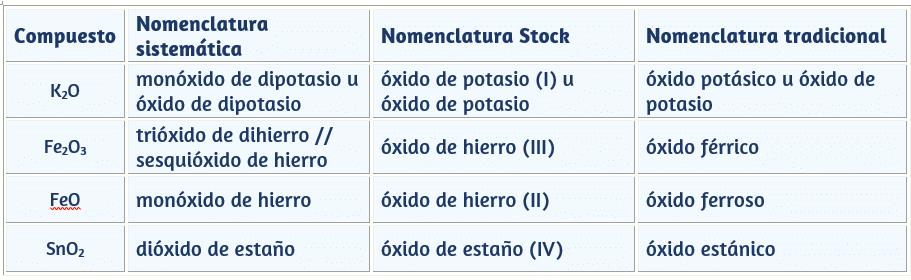
Cuando los no metales, nitrógeno y fosforo, trabajan con números de valencia 4 y 2 mientras se enlazan con el oxígeno se forman óxidos (ver la sección de anhídridos, penúltimo párrafo).
Son aquellos formados por la combinación del oxígeno con un no metal. Su fórmula general es No Metal2O. De ser posible, se simplifica. En este caso, la nomenclatura tradicional emplea la palabra anhídrido en lugar de óxido, a excepción de algunos óxidos de nitrógeno y fósforo. La nomenclatura sistemática y la Stock nombran a los compuestos con las mismas reglas que en los óxidos metálicos. En la nomenclatura tradicional se nombran con los siguientes sufijos y prefijos.
hipo - … - oso (para números de valencia 1 y 2)
… -oso (para números de valencia 3 y 4)
… -ico (para números de valencia 5 y 6)
per - … - ico (para el número de valencia 7)
No metal + Oxígeno → Anhídrido
2S + 3O2 → 2SO3

Cuando el flúor reacciona con el oxígeno se crea un compuesto diferente ya que el oxígeno deja de ser el elemento más electronegativo, distinto a como pasa con todos los óxidos donde el oxígeno es el elemento más electronegativo.
El único elemento más electronegativo que el oxígeno es el flúor con 4.0 mientras el oxígeno tiene 3.5. Así que el compuesto deja de llamarse óxido y se nombra como fluoruro de oxígeno para el sistema tradicional, fluoruro de oxígeno (II) para el sistema Stock y difluoruro de oxígeno para el sistemático. La formula es O2F2-1.Los óxidos de nitrógeno, al igual que los óxidos del azufre, son importantes por su participación en la lluvia ácida. Con el término óxido de nitrógeno se hace alusión a cualquiera de los siguientes:
• Óxido nítrico u Óxido de nitrógeno (II), de fórmula NO.
• Dióxido de nitrógeno, de fórmula NO2.
• Óxido nitroso o Monóxido de dinitrógeno, de fórmula N2O.
• Trióxido de dinitrógeno, de fórmula N2O3.
• Tetróxido de dinitrógeno, de fórmula N2O4.
• Pentóxido de dinitrógeno, de fórmula N2O5.
Entre las excepciones a las reglas de anhídridos para la nomenclatura tradicional están los óxidos de nitrógeno y óxidos de fósforo. Estos compuestos se nombran así:
• N21O-2 Anhídrido hiponitroso.
• N2O-2 Óxido hiponitroso
• N23O3-2 Anhídrido nitroso.
• N24O4-2 Óxido nitroso.
• N25O5-2 Anhídrido nítrico.
• P23O3-2 Anhídrido fosforoso.
Cuando los metales con más de dos números de valencia y que trabajan con los números de valencia iguales o mayores a 4 mientras se enlazan con el oxígeno, forman anhídridos (ver la sección de óxidos, segundo párrafo).
Los peróxidos son compuestos diatómicos en donde participan el grupo peróxido y un metal. En estos compuestos el grupo peróxido trabaja con dos oxígenos enlazados con una valencia de -1, la fórmula general de los peróxidos es Metal + (O-1) 2-2.En el sistema tradicional se utiliza el nombre peróxido en lugar de óxido y se agrega el nombre del metal con las reglas generales para los óxidos en esta nomenclatura. En las nomenclaturas Stock y sistemática se nombran los compuestos con las mismas reglas generales para los óxidos.
También llamados hiperóxidos, son compuestos binarios que contienen el grupo o anión superóxido, la fórmula general es Metal + (O 2)-1. Aparentemente, el oxígeno tiene valencia -1/2. Generalmente el grupo superóxido reacciona con los elementos alcalinos y alcalinotérreos.
Se nombran como los peróxidos tan sólo cambiando peróxido por superóxido o hiperóxido.
Metal + Grupo superóxido → Superóxido: Li+1 + (O2)-1 → LiO2
• KO2, superóxido o hiperóxido de potasio.
• CaO4 ó Ca (O2)2, superóxido de calcio.
• CdO4, superóxido de cadmio.
Son compuestos binarios formados por el grupo ozónido, que son 3 oxígenos enlazados con una valencia total de -1.
La fórmula general para los ozónidos es Metal + (O3)-1. Los ozónidos se nombran de forma análoga a los peróxidos con la diferencia que en estos compuestos se utiliza el nombre ozónido en lugar de peróxido.
Metal + Grupo ozónido → Ozónido: K + (O3)-1 → KO3
• KO3, ozónido de potasio.
• RbO3, ozónido de rubidio.
• CsO3, ozónido de cesio.
Son compuestos binarios o diatómicos formados por hidrógeno y un metal. En estos compuestos, el hidrógeno siempre tiene valencia -1. Se nombran con la palabra hidruro. Su fórmula general es MHx (x = valencia del metal). Para nombrar estos compuestos en el sistema tradicional se utiliza la palabra hidruro y se agrega el nombre del metal con los prefijos -oso o -ico con las reglas generales para esta nomenclatura. Para los sistemas Stock y sistemático se utilizan las reglas generales con la palabra hidruro como nombre genérico.
Metal + Hidrogeno → Hidruro metálico: 2K + H2 → 2KH.

Los hidrácidos (compuestos binarios ácidos) e hidruros no metálicos son compuestos formados entre el hidrógeno y un no metal de las familias VIA y VIIA ( anfígenos y halógenos respectivamente). Los elementos de estas dos familias que pueden formar hidrácidos e hidruros no metálicos son: S, Se, Te, F, Cl, I y Br, que por lo general trabajan con el menor número de oxidación, -2 para los anfígenos y -1 para los halógenos. Estos compuestos se nombran en el sistema tradicional y de forma diferente según si están disueltos (estado acuoso) o en estado puro (estado gaseoso). Los hidrácidos pertenecen al grupo de los ácidos.
Los hidruros no metálicos son los que se encuentran en estado gaseoso y se nombran agregando al no metal el sufijo -uro y la palabra hidrogeno precedido de la silaba "de". En este caso el nombre genérico es para el elemento más electropositivo que sería el del hidrógeno y el nombre específico es para el elemento más electronegativo que sería el del no metal, por ejemplo H+1 Br-1 (g) bromuro de hidrógeno, bromuro como nombre específico e hidrógeno como nombre genérico.
No metal + Hidrogeno → Hidruro no metálico:Cl2 + H2 → 2HCl(g)
Los hidrácidos provienen de disolver en agua a los hidruros no metálicos y por esa misma razón son estos los que se encuentran en estado acuoso. Se nombran con la palabra ácido, como nombre genérico, y como nombre específico se escribe el nombre del no metal y se le agrega el sufijo –hídrico. Al igual que en estado gaseoso el nombre genérico es nombrado por el elemento más electropositivo.
Hidruro No metálico + Agua → Hidrácido: HCl(g) + H2O → H+1 + Cl-1

Son compuestos binarios entre el hidrógeno y el boro que generalmente se enlazan siguiendo la fórmula BnHn+4. Estos compuestos no se nombran en un sistema de nomenclatura específico ya que las reglas para nombrarlos son especiales. Se utiliza la palabra borano con un prefijo numérico griego que depende del número de átomos de borano presentes en la molécula.
Son compuestos binarios de hidrogeno y silicio que se enlazan generalmente siguiendo la formula SinH2n+2. Los silanos al igual que los boranos no tienen un sistema de nomenclatura específico para ser nombrados y utilizan las mismas reglas de nomenclatura, con la palabra silano como base.
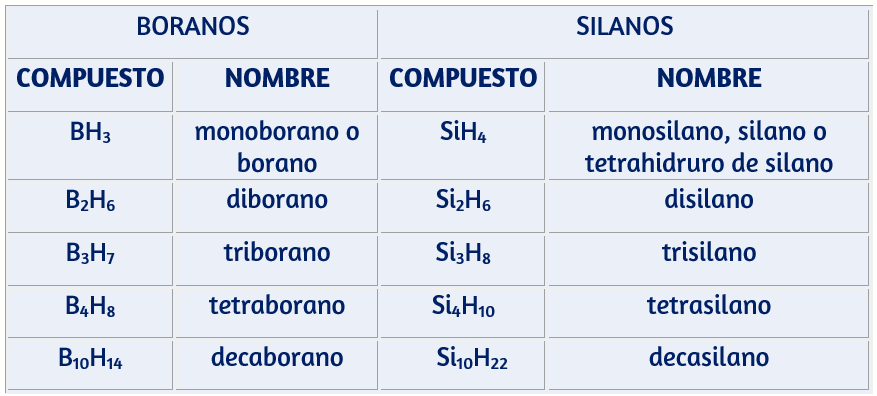
Son compuestos binarios de hidrógeno y germanio que se enlazan generalmente siguiendo la misma fórmula que los silanos GenH2n+2.
Los germanos al igual que los boranos y silanos no tienen un sistema de nomenclatura específico para ser nombrados y utilizan las mismas reglas de nomenclatura que los silanos, con la palabra germano como base.

Estos hidruros son compuestos binarios de hidrógeno y un elementos de la familia V que se enlazan siguiendo la formula N.M.H3. A estos compuestos se les llama por sus nombres comunes, aunque muy raramente se les nombra con las reglas de nomenclatura de los hidruros (metálicos). En estos hidruros no metálicos el hidrógeno es el elemento más electronegativo en el compuesto.
No metal + Hidrógeno → Hidruro no metálico.
N2 + 3H2 → 2NH3

También llamados oxoácidos y oxiácidos, son compuestos ternarios originados de la combinación del agua con un anhídrido u óxido ácido. La fórmula general para los oxácidos es H.X.O donde "X" representa al no metal. En el sistema tradicional se les nombra con las reglas generales para los anhídridos sustituyendo la palabra anhídrido por ácido (ya que de los anhídridos se originan). Para el sistema Stock se nombra al no metal con el sufijo –ato, luego el número de valencia del no metal y por último se agrega "de hidrógeno".
Y para la nomenclatura sistemática se indica el número de átomos de oxígeno con el prefijo correspondiente (según reglas generales para este sistema) seguido de la partícula “oxo” unida al nombre del no metal y el sufijo –ato, por último se agrega al nombre las palabras "dehidrogeno".
Anhídrido + Agua → oxácido.
SO3 + H2O → H2SO4

Compuestos en los que el grupo hidróxido (OH-) se combina con un metal. Se nombran de la misma forma en que se nombraban los compuestos binarios de acuerdo con la nomenclatura de Stock, teniendo en cuenta que ahora el número de oxidación del grupo hidróxido es –1.
Si en la molécula existen varios grupos hidróxido se escriben entre paréntesis y el subíndice correspondiente se adjudica al paréntesis, no a cada uno de los átomos del grupo. Así escribiremos Ca(OH)2
Ejemplos:
a) NaOH: hidróxido de sodio.
b) Fe(OH)3: hidróxido de hierro (III).
c) Zn(OH)2: hidróxido de zinc.
d) AuOH: hidróxido de oro (I).
Son compuesto que se obtienen al combinar un anión procedente de un oxácido con un metal. Se nombran igual que se nombraría, de acuerdo con la nomenclatura de Stock, un compuesto formado por el anión procedente del ácido y el catión del metal correspondiente.
Ejemplos:
a) Na2SO4. El compuesto está formado por un metal, el sodio, y el anión SO42$+$, procedente del ácido sulfúrico y denominado sulfato. El compuesto se denomina sulfato de sodio.
b) FeCO3. Está formado por un metal, el hierro, y el anión CO32$+$, proveniente del ácido carbónico y denominado carbonato. Antes de nombrar el compuesto se ha de averiguar el número de oxidación del hierro, que puede ser +2 o +3. Como el número de oxidación del carbonato es – 2, para que el número de oxidación total sea 0 es necesario que el.
número de oxidación del hierro sea +2. Así pues el nombre del compuesto es carbonato de hierro (II).
c) Au(BrO2)3. El metal es ahora el oro y el anión el Br02)$+$, proveniente del ácido bromoso y denominado por tanto bromito. El número de oxidación del oro es +3 por lo que el compuesto es el bromito de oro (III).
Las sales ácidas son compuestos procedentes de un ácido (aquí nos limitaremos a los oxácidos) que ha perdido alguno (pero no todos) sus hidrógenos sustituyéndolos por cationes generalmente metálicos. Son similares a las oxisales salvo por el hecho de que conservan todavía algún hidrógeno y retienen por tanto cierto carácter ácido. El o los hidrógenos conservados por el anión se escriben en el extremo izquierdo de este. Ejemplos: NaHSO4, K2HPO3.
Solo pueden obtenerse sales ácidas de aquellos ácidos que tengan más de un hidrógeno.
Como sucedía en las oxisales la carga (negativa) y número de oxidación del anión coinciden con el número de hidrógenos perdidos por el ácido:
a) HSO4$+$: la carga y el número de oxidación es - 1 pues procede del H2SO4.
b) HPO32- : la carga y el número de oxidación son -2 pues procede el H3PO3.
Estos aniones se pueden nombrar de dos formas distintas:
1. Anteponiendo al nombre del anión que se obtendría por la eliminación de todos los hidrógenos la palabra hidrógeno con un prefijo (di, tri, etc.) si el anión conserva más de un hidrógeno. Esta es la forma recomendada por la IUPAC y la que utilizaremos preferentemente en el curso.
2. Colocando tras el nombre del anión la palabra ácido (separada de él) con un prefijo (di, tri, etc.) si el anión conserva más de un hidrógeno.
Ahora para nombrar estos compuestos seguiremos el procedimiento habitual: se nombrará primero el anión y a continuación el anión. Por ejemplo, el NaHCO3, puede nombrarse como carbonato ácido de sodio o como hidrógenocarbonato de sodio.
Nota: Durante mucho tiempo se utilizó también para indicar la presencia de un hidrógeno en el anión el prefijo bi- y este compuesto se denominaba (y todavía se hace así, comercialmente) bicarbonato sódico. Esta nomenclatura ya no está permitida y debe evitarse.
El AgH2PO3 es el dihidrógenofosfito de plata o fosfito diácido de plata.
El Cu(HSO4)2 es el hidrógenosulfato de cobre (II) o sulfato ácido de cobre (II).


“Es el peor de los tiempos pero también el mejor porque aún tenemos una oportunidad”. Sylvia Earle.


“La ciencia es un gran juego. Es inspiradora y refrescante, y el campo de juego es el universo entero” (Isidor Isaac Rabi, Premio Nobel de Física 1944)


Un enlace químico es el proceso químico responsable de las interacciones atractivas entre átomos y moléculas, que confiere estabilidad a los compuestos químicos diatómicos y poliatómicos. La explicación de tales fuerzas atractivas es un área compleja que está descrita por las leyes de la química cuántica.En general, el enlace químico fuerte está asociado con la compartición o transferencia de electrones entre los átomos participantes. Las moléculas, cristales, y gases diatómicos (que forman la mayor parte del ambiente físico que nos rodea) está unido por enlaces químicos, que determinan las propiedades físicas y químicas de la materia.
Hay que tener en cuenta que las cargas opuestas se atraen, porque, al estar unidas, adquieren una situación más estable (de menor entalpía) que cuando estaban separados. Esta situación de mayor estabilidad suele darse cuando el número de electrones que poseen los átomos en su último nivel es igual a ocho, estructura que coincide con la de los gases nobles, ya que los electrones que orbitan el núcleo están cargados negativamente, y que los protones en el núcleo lo están positivamente, la configuración más estable del núcleo y los electrones es una en la que los electrones pasan la mayor parte del tiempo entre los núcleos, que en otro lugar del espacio. Estos electrones hacen que los núcleos se atraigan mutuamente.
En el año 1927, la teoría de enlace de valencia fue formulada, argumentando esencialmente que el enlace químico se forma cuando dos electrones de valencia, en sus respectivos orbitales atómicos, trabajan o funcionan para mantener los dos núcleos juntos, en virtud a los efectos de disminución de energía del sistema. En 1931, a partir de esta teoría, el químico Linus Pauling publicó lo que algunos consideran uno de los más importantes papeles en la historia de la química: "Sobre la naturaleza del enlace químico". En este papel, extendiendo los trabajos de Lewis, la teoría del enlace de valencia (TEV) de Heitler y London, y su propio trabajo previo, presentó seis reglas para el enlace de electrones compartidos, las tres primeras de las cuales generalmente ya eran conocidas:
Sus tres últimas reglas eran nuevas:
A partir de este artículo, Pauling publicaría en 1939 un libro de texto: "Sobre la Naturaleza del Enlace Químico" que vendría a ser llamado por algunos como la "biblia" de la química moderna. Este libro ayudó a los químicos experimentales a entender el impacto de la teoría cuántica sobre la química. Sin embargo, la edición posterior de 1939 falló en explicar adecuadamente los problemas que parecían ser mejor entendibles por la teoría de orbitales moleculares. El impacto de la teoría del enlace de valencia declinó durante la década de 1960 y 1970 a la par con el crecimiento en popularidad de la teoría de orbitales moleculares, que estaba siendo implementada en muchos programas de grandes ordenadores. A partir de la década de 1960, los problemas más difíciles de la implementación de la teoría del enlace de valencia en programas de computadoras habían sido mayormente resueltos y la teoría del enlace de valencia vio un resurgimiento.
La teoría de los orbitales moleculares (TOM) usa una combinación lineal de orbitales atómicos para formar orbitales moleculares, que abarcan la molécula entera. Estos orbitales son divididos frecuentemente en orbitales enlazantes, orbitales antienlazantes, y orbitales de no enlace. Un orbital molecular es simplemente un orbital de Schrödinger que incluye varios, pero frecuentemente sólo dos, núcleos. Si este orbital es del tipo en que los electrones tienen una mayor probabilidad de estar entre los núcleos que en cualquier otro lugar, el orbital será un orbital enlazante, y tenderá a mantener los núcleos cerca.
Si los electrones tienden a estar presentes en un orbital molecular en que pasan la mayor parte del tiempo en cualquier lugar excepto entre los núcleos, el orbital funcionará como un orbital antienlazante, y realmente debilitará el enlace. Los electrones en orbitales no enlazantes tienden a estar en orbitales profundos asociados casi enteramente o con un núcleo o con otro y entonces pasarán igual tiempo entre los núcleos y no en ese espacio. Estos electrones no contribuyen ni detractan la fuerza del enlace.
En Química, un enlace iónico o electrovalente es la unión de átomos que resulta de la presencia de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto químico simple, no se fusionan sino uno da y otro recibe.
Dado que los elementos implicados tienen elevadas diferencias de electronegatividad, este enlace suele darse entre un compuesto metálico y uno no metálico. Se produce una transferencia electrónica total de un átomo a otro formándose iones de diferente signo. El metal dona uno o más electrones formando iones con carga positiva o cationes con una configuración electrónica estable. Estos electrones luego ingresan en el no metal, originando un ion cargado negativamente o anión, que también tiene configuración electrónica estable. Son estables pues según la regla del octeto o por la estructura de Lewis adquieren 8 electrones en su capa más exterior (capa de valencia), aunque esto no es del todo cierto, pues hay varias excepciones, la del hidrógeno (H) que se llega al octeto con 2 electrones, el berilio (Be) con 4 , el aluminio (Al) y el boro (B) que se rodean de seis.
Los compuestos iónicos forman redes cristalinas constituidas por iones de carga opuesta, unidos por fuerzas electrostáticas. Este tipo de atracción determina las propiedades observadas. Si la atracción electrostática es fuerte, se forman sólidos cristalinos de elevado punto de fusión e insolubles en agua; si la atracción es menor, como en el caso del NaCl, el punto de fusión también es menor y, en general, son solubles en agua e insolubles en líquidos apolares, como el benceno.
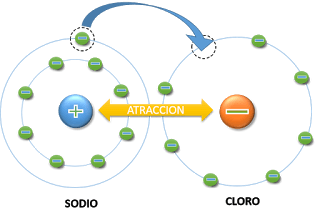
En una unión de dos átomos por enlace iónico, un electrón abandona el átomo más electropositivo y no pasa a formar parte del negativo sino que pasa a formar parte de la nube electrónica del más electronegativo.
El cloruro de sodio (la sal común) es un ejemplo de enlace iónico: en él se combinan sodio y cloro, perdiendo el primero un electrón que es capturado por el segundo: NaCl → Na$+$Cl$+$. De esta manera forman dos iones de carga contraria: un catión (de carga positiva) y un anión (de carga negativa). La diferencia entre las cargas de los iones provoca entonces una fuerza de interacción electromagnética entre los átomos que los mantiene unidos. El enlace iónico es la unión en la que los elementos involucrados aceptarán o perderán electrones.
En una solución, los enlaces iónicos pueden romperse y se considera entonces que los iones están disociados. Es por eso que una solución fisiológica de cloruro de sodio y agua se marca como: Na$+$ + Cl$+$, mientras que los cristales de cloruro de sodio se marcan: Na$+$ + Cl$+$ o simplemente NaCl.
Algunas características de este tipo de enlace son:
En estado sólido no conducen la electricidad. Si se utiliza un bloque de sal como parte de un circuito en lugar del cable, el circuito no funcionará. Así tampoco funcionará una bombilla si utilizamos como parte de un circuito un cubo de agua, pero si disolvemos sal en abundancia en dicho cubo, la bombilla del circuito se encenderá. Esto se debe a que los iones disueltos de la sal son capaces de acudir al polo opuesto (a su signo) de la pila del circuito y por ello éste funciona.
Los iones se clasifican en dos tipos:
a) Anión: Es un ion con carga eléctrica negativa, lo que significa que los átomos que lo conforman tienen un exceso de electrones. Comúnmente los aniones están formados por no metales, aunque hay ciertos aniones formados por metales y no metales. Los aniones más habituales son (el número entre paréntesis indica la carga):

b) Catión: es un ion con carga eléctrica positiva. Los más comunes se forman a partir de metales, pero hay ciertos cationes formados con no metales.

El enlace covalente se presenta entre dos átomos no metálicos. En un enlace covalente no hay perdida ni ganancia de electrones, sino que se comparten para completar el octeto y así alcanzar configuraciones energéticamente más estables.
Se establecen entre elementos con el mismo carácter electronegativo tales como (F2, Cl2, O2) y entre elementos que tengan atracciones similares iguales como es el caso del HCl.
En el enlace covalente, los dos átomos no metálicos comparten uno o más electrones, es decir se unen a través de sus electrones en el último orbital, el cual depende del número atómico en cuestión. Entre los dos átomos pueden compartirse uno, dos o tres pares de electrones, lo cual dará lugar a la formación de un enlace simple, doble o triple respectivamente. En la representación de Lewis, estos enlaces pueden representarse por una pequeña línea entre los átomos.
Existen dos tipos de sustancias covalentes:
Sustancias covalentes moleculares: los enlaces covalentes forman moléculas que tienen las siguientes propiedades:
Redes o sustancias covalentes reticulares: Además las sustancias covalentes forman redes cristalinas, semejantes a los compuestos iónicos, que tienen estas propiedades:
Elevadas temperaturas de fusión y ebullición.
Considérense átomos de hidrógeno, a medida que se aproximan entre sí, se van haciendo notar las fuerzas que atraen a cada electrón al núcleo del otro átomo, hasta que dichas fuerzas de atracción se llegan a compensar con la repulsión que los electrones sienten entre sí. En ese punto, la molécula presenta la configuración más estable.
Lo que ha sucedido es que los orbitales de ambos electrones se han traslapado, de modo que ahora es imposible distinguir a qué átomo pertenece cada uno de los electrones. Sin embargo, cuando los átomos son distintos, los electrones compartidos no serán atraídos por igual, de modo que estos tenderán a aproximarse hacia el átomo más electronegativo, es decir, aquel que tenga una mayor apetencia de electrones. Este fenómeno se denomina polaridad (los átomos con mayor electronegatividad obtienen una polaridad más negativa, atrayendo los electrones compartidos hacia su núcleo), y resulta en un desplazamiento de las cargas dentro de la molécula.
Se podría decir que al átomo más electronegativo no le gusta mucho compartir sus electrones con los demás átomos, y en el caso más extremo, deseará que el electrón le sea cedido sin condiciones formándose entonces un enlace iónico, de ahí que se diga que los enlaces covalentes polares tienen, en alguna medida, carácter iónico. Así pues, para diferencias de electronegatividades mayores de 3 el enlace será predominantemente de carácter iónico, como sucede entre el oxígeno o flúor con los elementos de los grupos 1 y 2; sin embargo, cuando está entre $0$ y $1,9$ será el carácter covalente el que predomine, como es el caso del enlace C-H.
No obstante, según el químico Raymond Chang, esta diferencia de electronegatividad entre los átomos debe ser $2,0$ o mayor para que el enlace sea considerado iónico.
Dependiendo de la diferencia de electronegatividad, el enlace covalente puede ser clasificado en covalente polar y covalente puro o apolar. Si la diferencia de electronegatividad está entre $0,4$ y $1,7$ es un enlace covalente polar, y si es inferior a $0,4$ es covalente apolar.
Cuando un mismo átomo aporta el par de electrones, se dice que el enlace covalente es polarizado. Aunque las propiedades de enlace covalente polarizado son parecidas a las de un enlace covalente normal (dado que todos los electrones son iguales, sin importar su origen), la distinción es útil para hacer un seguimiento de los electrones de valencia y asignar cargas formales. Una base dispone de un par electrónico para compartir y un ácido acepta compartir el par electrónico para formar un enlace covalente coordinado.
Características
En general cuando un átomo comparte los dos electrones para uno solo se llama enlace covalente dativo y se suele representar con una flecha (→).
Se forma entre átomos iguales o diferentes, y la diferencia de electronegatividad debe ser cero o muy pequeña (menor que $0,4$). En este enlace, los electrones son atraídos por ambos núcleos con la misma intensidad, generando moléculas cuya nube electrónica es uniforme.
Un enlace metálico es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí. Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de líneas tridimensionales que adquieren estructuras tales como: la típica de empaquetamiento compacto de esferas (hexagonal compacta), cúbica centrada en las caras o la cúbica centrada en el cuerpo.
En este tipo de estructura cada átomo metálico está dividido por otros doce átomos (seis en el mismo plano, tres por encima y tres por debajo).
Además, debido a la baja electronegatividad que poseen los metales, los electrones de valencia son extraídos de sus orbitales. Este enlace solo puede estar en sustancias en estado sólido.
Los metales poseen algunas propiedades características que los diferencian de los demás materiales. Suelen ser sólidos a temperatura ambiente, excepto el mercurio, y tienen un punto de fusión alto.
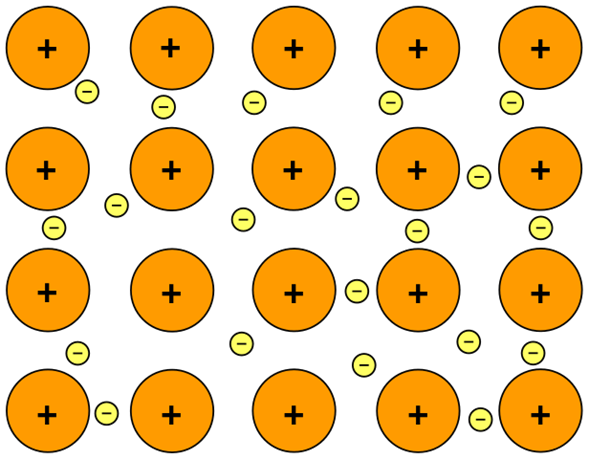
El enlace metálico es característico de los elementos metálicos. Es un enlace fuerte, primario, que se forma entre elementos de la misma especie.
Al estar los átomos tan cercanos unos de otros, interaccionan sus núcleos junto con sus nubes electrónicas, empaquetándose en las tres dimensiones, por lo que quedan los núcleos rodeados de tales nubes. Estos electrones libres son los responsables de que los metales presenten una elevada conductividad eléctrica y térmica, ya que estos se pueden mover con facilidad si se ponen en contacto con una fuente eléctrica. Los metales generalmente presentan brillo y son maleables. Los elementos con un enlace metálico están compartiendo un gran número de electrones de valencia, formando un mar de electrones rodeando un enrejado gigante de cationes. Muchos de los metales tienen puntos de fusión más altos que otros elementos no metálicos, por lo que se puede inferir que hay enlaces más fuertes entre los distintos átomos que los componen. La vinculación metálica es no polar, apenas hay diferencia de electronegatividad entre los átomos que participan en la interacción de la vinculación (en los metales, elementales puros) o muy poca (en las aleaciones), y los electrones implicados en lo que constituye la interacción a través de la estructura cristalina del metal. El enlace metálico explica muchas características físicas de metales, tales como maleabilidad, ductilidad, buenos en la conducción de calor y electricidad, y con brillo o lustre (devuelven la mayor parte de la energía lumínica que reciben).
La vinculación metálica es la atracción electrostática entre los átomos del metal o cationes y los electrones deslocalizados. Esta es la razón por la cual se puede explicar un deslizamiento de capas, dando por resultado su característica maleabilidad y ductilidad.
Los átomos del metal tienen por lo menos un electrón de valencia, no comparten estos electrones con los átomos vecinos, ni pierden electrones para formar los iones. En lugar los niveles de energía externos de los átomos del metal se traslapan. Son como enlaces covalentes identificados.
En principio se debe distinguir qué es un Enlace Químico, siendo éstas las fuerzas que mantienen a los átomos unidos formando las moléculas. Y que existen dos tipos de enlaces químicos, los enlaces covalentes (en donde los átomos comparten dos electrones) y las interacciones débiles no covalentes (interacciones débiles entre iones, moléculas y entre partes de las moléculas).
La diferencia entre un enlace covalente e interacciones débiles no covalentes es que los enlaces covalentes son los responsables de las estructuras primarias, definen la composición e identidad de cada biopolímero y las "configuraciones" que adopta cada grupo molecular, mientras que las interacciones débiles no covalentes son las responsables de la complejidad de las conformaciones que caracterizan la arquitectura molecular de las macromoléculas biológicas y los complejos supraestructurales, es decir, las interacciones intramoleculares (átomos o grupos moleculares dentro de las macromoléculas) e intermoleculares, por lo que son fundamentales para las funciones biológicas.
Las interacciones débiles no covalentes se les llama "débiles" porque representan la energía que mantienen unidas a las especies supramoleculares y que son considerablemente más débiles que los enlaces covalentes. Las interacciones no covalentes fundamentales son:
a) El enlace de hidrógeno (antiguamente conocido como puente de hidrógeno)
b) Las fuerzas de Van der Waals, que podemos clasificar a su vez en:
Las fuerzas de Van Der Waals (o interacciones de Van Der Waals), denominada así en honor al científico neerlandés Johannes Diderik van der Waals, es la fuerza atractiva o repulsiva entre moléculas (o entre partes de una misma molécula) distintas a aquellas debidas al enlace covalente o a la interacción electrostática de iones con otros o con moléculas neutras. El término incluye:
Las fuerzas de Van der Waals son relativamente débiles comparadas con los enlaces químicos normales, pero juegan un rol fundamental en campos tan diversos como química supramolecular, biología estructural, ciencia de polímeros, nanotecnología, ciencia de superficies, y física de la materia condensada. Las fuerzas de Van der Waals definen el carácter químico de muchos compuestos orgánicos. También definen la solubilidad de los alcoholes inferiores. Las propiedades del grupo polar hidróxilo dominan a las débiles fuerzas intermoleculares de Van der Waals. En los alcoholes superiores, las propiedades del radical alquílico apolar (R) dominan y definen la solubilidad. Las fuerzas de Van der Waals crecen con la longitud de la parte no polar de la sustancia.
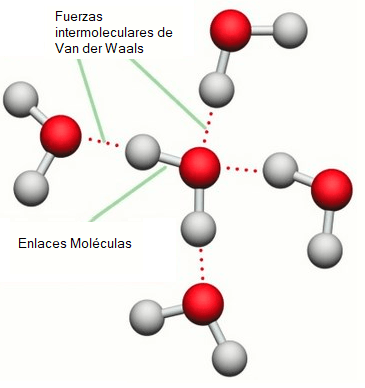
Las fuerzas de Van der Waals incluyen a atracciones entre átomos, moléculas, y superficies. Difieren del enlace covalente y del enlace iónico en que están causados por correlaciones en las polarizaciones fluctuantes de partículas cercanas (una consecuencia de la dinámica cuántica). Las fuerzas intermoleculares tienen cuatro contribuciones importantes. En general, un potencial intermolecular tiene un componente repulsivo (que evita el colapso de las moléculas debido a que al acercarse las entidades unas a otras las repulsiones dominan). También tiene un componente atractivo que, a su vez, consiste de tres contribuciones distintas:
Todas las fuerzas intermoleculares de Van der Waals presentan anisotropía (excepto aquellas entre átomos de dos gases nobles), lo que significa que dependen de la orientación relativa de las moléculas.
Las interacciones de inducción y dispersión son siempre atractivas, sin importar su orientación, pero el signo de la interacción cambia con la rotación de las moléculas.
Esto es, la fuerza electrostática puede ser atractiva o repulsiva, dependiendo de la orientación mutua de las moléculas. Cuando las moléculas tienen movimiento térmico, como cuando están en fase gaseosa o líquida, la fuerza electrostática se reduce significativamente, debido a que las moléculas rotan térmicamente y experimentan las partes repulsiva y atractiva de la fuerza electrostática.
El enlace de hidrógeno (o puente de hidrógeno) es un tipo de fuerzas dipolo–dipolo que se da solo entre un átomo de hidrógeno de una molécula y un átomo de pequeño tamaño y muy electronegativo, como F, O y N.
Estas interacciones intermoleculares son débiles pero más fuertes que las interacciones dipolo dipolo normales. Esto implica que las sustancias que tienen enlaces de hidrógeno, tienen puntos de fusión y ebullición más elevados. Por esta razón, el agua a temperatura ambiente es un líquido y no un gas como como el H2S.
El enlace de hidrógeno intramolecular es responsable parcialmente de la estructura secundaria, estructura terciaria y estructura cuaternaria de las proteínas y ácidos nucleicos. Un átomo de hidrógeno unido a un átomo relativamente electronegativo es un átomo donante del enlace de hidrógeno. Este átomo electronegativo puede ser flúor, oxígeno o nitrógeno. Un átomo electronegativo tal como el flúor, oxígeno o nitrógeno es un aceptor de enlace de hidrógeno, sin importar si está enlazado covalentemente o no a un átomo de hidrógeno.
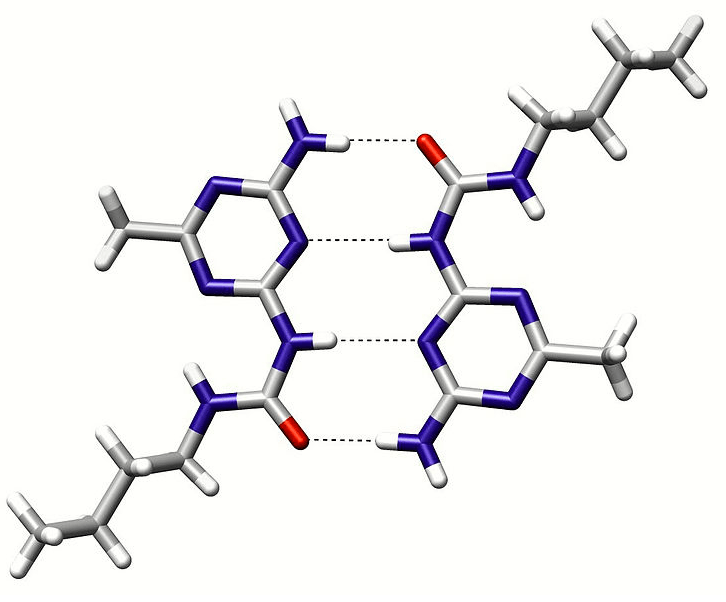
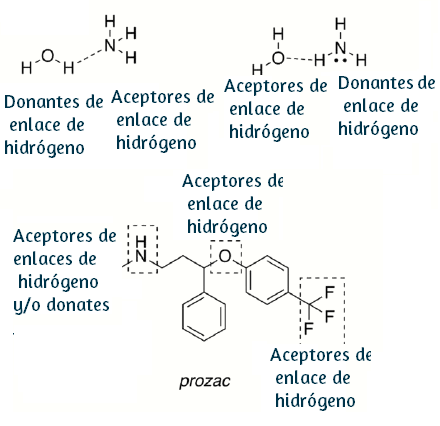
En otras palabras puede expresarse que el puente de hidrógeno puede vincular distintas moléculas e incluso sectores diferentes de una misma molécula. El átomo de hidrógeno, que cuenta con carga positiva, se conoce como átomo donante, mientras que el átomo de oxígeno, flúor o nitrógeno es el átomo aceptor del enlace.
El carbono también puede participar en enlaces de hidrógeno, cuando el átomo de carbono está enlazado a algunos átomos electronegativos, como en el caso de cloroformo, CHCl3. El átomo electronegativo atrae la nube electrónica alrededor del núcleo de hidrógeno y, al descentralizar la nube, deja al átomo con una carga positiva parcial. Debido al pequeño tamaño del hidrógeno en comparación a otros átomos y moléculas, la carga resultante, aunque solo parcial, no representa una gran densidad de carga. Un enlace de hidrógeno resulta cuando esta densidad de carga positiva fuerte atrae a un par libre de electrones de otro heteroátomo, que se convierte en el aceptor de enlace de hidrógeno.
El enlace de hidrógeno suele ser descrito como una interacción electrostática dipolo-dipolo. Sin embargo, también tiene algunas características del enlace covalente: es direccional, fuerte, produce distancias interatómicas menores que la suma de los radios de van der Waals, y usualmente involucra un número limitado de compañeros de interacción, que puede ser interpretado como un tipo de valencia. Estas características covalentes son más significativas cuando los aceptores se unen a átomos de hidrógeno de donantes más electronegativos.
La interacción dipolo-dipolo consiste en la atracción electrostática entre el extremo positivo de una molécula polar y el negativo de otra. El enlace de hidrógeno es un tipo especial de interacción dipolo-dipolo.

Las fuerzas electrostáticas entre dos iones disminuyen de acuerdo con un factor $1/d^2$ a medida que aumenta su separación $d$. En cambio, las fuerzas dipolo-dipolo varían según $1/d^3$ ($d$ elevado a la tercera potencia) y sólo son eficaces a distancias muy cortas; además son fuerzas más débiles que en el caso ion-ion porque $q+$ y $q-$ representan cargas parciales. Las energías promedio de las interacciones dipolo dipolo son aproximadamente $4 kJ$ por mol, en contraste con los valores promedio para energías características de tipo iónico y de enlace covalente ($~400 kJ$ por $mol$).
Estas son ligeramente direccionales, es decir, al elevarse la temperatura, el movimiento transicional, rotacional y vibracional de las moléculas aumenta y produce orientación más aleatoria entre ellas. En consecuencia, la fuerza de las interacciones dipolo-dipolo disminuye al aumentar la temperatura.



"El encuentro de dos personalidades es como el contacto de dos sustancias químicas: si hay alguna reacción, ambas se transforman". (Carl Jung)


Las reacciones químicas ocurren en todos lados. El combustible en nuestros coches se quema con oxígeno para proporcionar energía que mueve al auto. Cuando cocinamos nuestros alimentos o aclaramos nuestro cabello tienen lugar reacciones químicas. En las hojas de los árboles y las plantas, el dióxido de carbono y el agua se convierten en carbohidratos.
En toda reacción química los átomos en las sustancias que reaccionan, que se llaman reactivos, se reordenan para generar nuevas sustancias denominadas productos. Los átomos en los reactivos y en los productos son los mismos, lo que significa que la materia se conserva y no se pierde durante un cambio químico.
Recordar que en un cambio físico se altera la apariencia de la sustancia, pero no su composición, por ejemplo cuando el agua líquida se convierte en gas o en un sólido. En un cambio químico las sustancias que reaccionan se transforman nuevas sustancias con diferentes composiciones y diferentes propiedades, por ejemplo, cuando la plata (Ag), metal brillante, reacciona con el azufre (S) para convertirse en una sustancia opaca llamada sulfuro de plata (Ag2S).
Las reacciones químicas se representan mediante ecuaciones químicas.
Nos indica lo que sucede durante la reacción y mediante símbolos químicos muestra quienes son los participantes de la misma.
Cuando quemamos carbón en un asador, el carbón se combina con el oxígeno para formar dióxido de carbono. La siguiente ecuación representa dicha reacción:
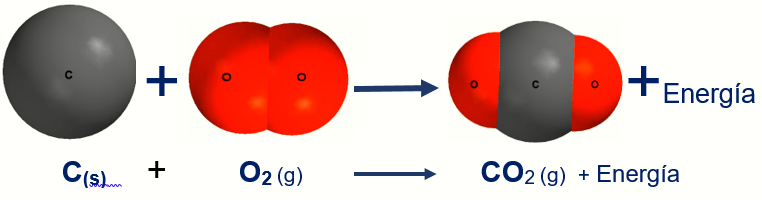
Cuando tiene lugar una reacción química, los enlaces entre átomos de los reactivos se rompen y se forman nuevos enlaces entre los átomos de los productos. Ya mencionamos que en cualquier reacción química, en las nuevas sustancias debe haber el mismo número de átomos que en las sustancias de partida, por lo tanto una reacción se debe escribir a través de una ecuación química balanceada. Las letras minúsculas entre paréntesis indican el estado de agregación de las sustancias, es decir, si se encuentran en estado gaseoso (g), líquido (l), sólido (s) o disueltos en agua (ac). La reacción del ejemplo se puede leer: 1 mol de átomos de carbono sólido se combinan con 1 mol de oxígeno gaseoso para formar 1 mol de dióxido de carbono gaseoso.
¿La ecuación anterior está balanceada? Sí, porque hay un átomo de carbono y dos átomos de oxígeno de cada lado de la ecuación.
En estas reacciones dos o más elementos o compuestos se unen para formar un producto, o lo que es lo mismo, para sintetizar una nueva sustancia.
En estas reacciones dos o más elementos o compuestos se unen para formar un producto, o lo que es lo mismo, para sintetizar una nueva sustancia.
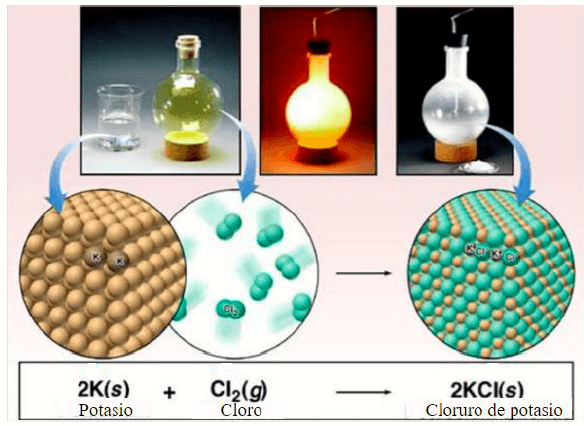
El nitrógeno se combina con el hidrógeno para sintetizar amoníaco.
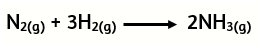
El óxido de magnesio se combina con el dióxido de carbono para dar carbonato de magnesio.
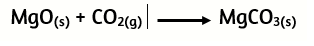
En una reacción de descomposición, un único reactivo se divide en dos o más productos.
Cuando el óxido de mercurio (II) se calienta, los productos son mercurio y oxígeno.
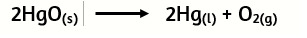
En las reacciones de combustión sD. Reacciones de sustitución se necesita oxígeno y con frecuencia la reacción produce un óxido, agua y calor. Quemar leña en un hogar o gasolina en el motor de un coche son ejemplos de este tipo de reacciones.
Cuando quemamos hidrocarburos en aire, éstos reaccionan con O2 para formar CO2 y H2O.
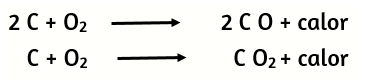
Siempre que se queme un hidrocarburo (compuesto que contiene únicamente carbono e hidrógeno) se obtiene CO2 y agua:
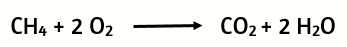
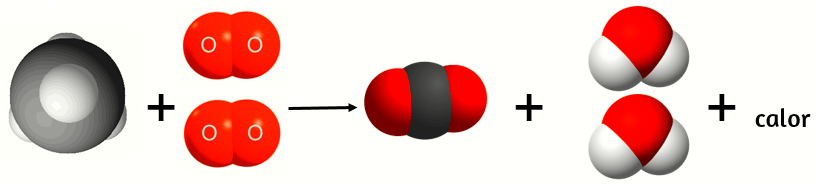
La combustión completa produce CO2. La reacción de combustión incompleta se produce en un ambiente deficiente en oxígeno, genera llama amarilla y produce una mezcla de monóxido de carbono, CO (sumamente tóxico) y residuo carbonoso (C) al que se le llama hollín.
En estas reacciones los elementos en los compuestos se sustituyen por otros elementos. Hay dos tipos: reacciones de sustitución simple o única en donde un elemento no combinado toma el lugar de un elemento en un compuesto. Un ejemplo de este tipo de reacción ocurre cuando el hidrógeno de un ácido se sustituye por un metal reactivo:
Cuando se pone en contacto un trozo de zinc con ácido clorhídrico, se observa un burbujeo producto del desprendimiento de hidrógeno gaseoso.

La figura muestra como ejemplo, la adición de una disolución incolora de yoduro de potasio (KI) a una disolución incolora de nitrato de plomo Pb(NO3)2 la cual produce un precipitado amarillo de yoduro de plomo (PbI2) que lentamente se asienta en el fondo del vaso. (ver ).
La reacción en la que una disolución de hidróxido de sodio reacciona con una de ácido clorhídrico para dar cloruro de sodio y agua, se denomina también reacción de neutralización , pues un ácido (que contiene H+) se neutraliza con una base o hidróxido (que contiene OH-) para producir la sal correspondiente y agua.
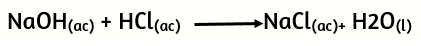
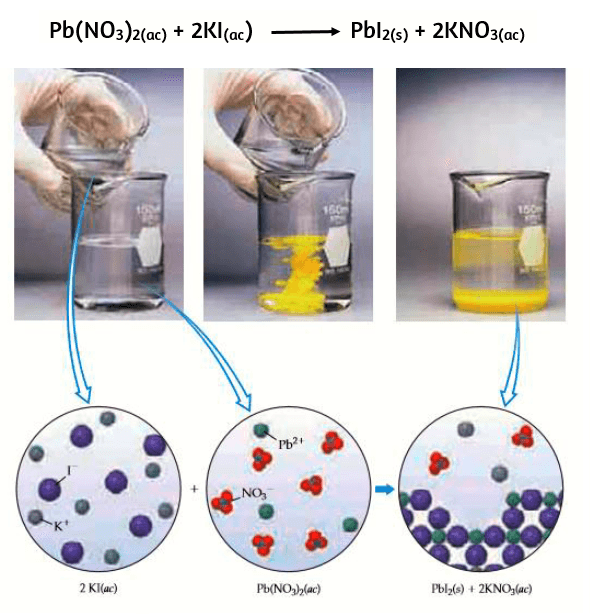
En toda reacción redox se transfieren electrones de una sustancia a otra. Si una sustancia pierde electrones, otra debe ganarlos. La oxidación se define como la pérdida de electrones y la reducción es la ganancia de electrones. En una reacción redox hay cambios en los estados de oxidación de algunos elementos.
El hierro metálico se obtiene al reducir el óxido de hierro (III) utilizando carbono.

En esta reacción el carbono pierde electrones y se oxida y el hierro los gana y se reduce. Vemos que el Fe tiene estado de oxidación +3 en los reactivos y pasa a tener estado de oxidación 0 en los productos, por haber ganado tres electrones, mientras que el C tiene estado de oxidación 0 en los reactivos y pasa tener estado de oxidación +4 en los productos por haberse oxidado al haber perdido electrones.
Si colocamos un clavo de hierro (Fe) dentro de una solución de sulfato de cobre (CuSO4), se depositará cobre (Cu) metálico sobre el clavo y se formará una disolución de sulfato ferroso (FeSO4).
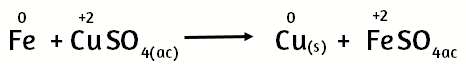
En este caso, el hierro se oxidó de 0 a +2 y el cobre se redujo de +2 a 0.
La palabra estequiometría deriva del griego stoicheion, que significa “elemento” y metría, que significa “medición”. La estequiometría es la relación de las masas atómicas entre reactivos y productos y se basa en un principio fundamental, la ley de conservación de la masa de Lavoisier: la masa total de todas las sustancias presentes después de una reacción química es la misma que la masa total antes de la reacción. Esto es, el mismo número de átomos está presente antes y después de la reacción. Los cambios que ocurren durante cualquier reacción simplemente reacomodan a los átomos.
Una vez que conocemos las fórmulas químicas de los reactivos y productos de una reacción, podemos escribir la ecuación química no balanceada. Luego balanceamos la ecuación determinando los coeficientes estequiométricos que producen números iguales de cada tipo de átomo en cada miembro de la ecuación (reactivos y productos). Para casi todas las aplicaciones, una ecuación balanceada deberá tener los coeficientes enteros más bajos posibles.
En otras palabras la Ley de Lavoisier corresponde a la conservación de la masa: "En una reacción química la masa se conserva. Esto es, la masa de los reactivos es igual a la masa de los productos”.
Veamos un ejemplo: En el laboratorio se hacen reaccionar 5 moles de Aluminio sólido con la cantidad necesaria de una disolución acuosa de HCl para obtener una disolución acuosa de AlCl3 e Hidrógeno gaseoso. ¿Cuántos gramos de sal se forman?
Para la solución, se debe recurrir al concepto de mol, pero un mol de que?, supóngase la sustancia Zinc. Entonces es, la cantidad de zinc que contiene $6,02.10^{23}$ átomos de zinc.
En esa cantidad de zinc (a la que le corresponde una masa de $65,5 g$, ya que la balanza ha sido previamente tarada e indica directamente la masa del zinc contenido en el matraz) hay el Número de Avogadro de átomos de zinc.
Si consideramos ahora un compuesto, como puede ser el agua, deberemos de considerar cuál es la masa de una molécula (unidad elemental, básica) de agua: $18,0 umas$ (unidades de masa atómica).
Tomando una cantidad de (sustancia) agua cuya masa en gramos sea numéricamente igual a su masa atómica, podemos asegurar que estaremos cogiendo $6,02.10^{23}$ moléculas de agua.
Entonces, luego del concepto de mol, la solución al ejercicios es: pero para poder resolver el ejercicio lo primero que debemos hacer es plantear la ecuación química que se produce en la reacción. Planteamos la ecuación química no balanceada:

Determinamos los coeficientes estequiométricos:
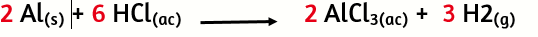
Ahora sí estamos en condiciones de contestar el enunciado.
Con base en los moles de Al que reaccionan (dato del problema) y a la relación estequiométrica entre el Al y el AlCl3 (de acuerdo a la ecuación química balanceada) podemos establecer la siguiente relación:
Transformando los moles de sal formada en gramos, nos queda:
$$5 \textsf{ moles de AlC}_3 × \frac{133.5 g \textsf{ de AlCl}_3 }{1 \textsf{ mol de AlCl}_3} = 667,5g \textsf{ de AlCl}_3$$La disponibilidad de reactivos en una reacción química puede limitar la cantidad de producto que se obtiene. Cuando los reactivos no se encuentran en las proporciones estequiométricas que indica la ecuación química, el reactivo que está en defecto, es decir, que está en menor proporción, se denomina reactivo limitante, porque será el que "limite" la obtención de los productos. El otro reactivo se llama reactivo en exceso.
Ejemplo: Una mezcla de 100, 0 g disulfuro de carbono y 200, 0 g de cloro (gas) se pasa a través de un tubo de reacción caliente produciéndose la reacción:
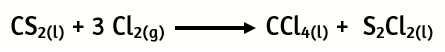
Calcular la cantidad de S2Cl2 que se obtendrá
Como dan cantidades para ambos reactivos, vemos si están en cantidades estequiométricas (justas)
$$100,0 \cancel{g \textsf{CS}_2} \frac{1 \textsf{ mol CS}_2}{76,2 \cancel{g \textsf{CS}_2}} = 1,31 \textsf{ mol CS}_2$$Como puede verse en la ecuación química, 1 mol de CS2 reacciona con 3 moles de Cl2, para reaccionar con $1,31$ moles de CS2 se necesitarían: $1,31 x 3 = 3,93$ moles de Cl2. Por tanto, como sólo existen $2,82$ moles de Cl2:
Reactivo en exceso (no reacciona todo): el CS2. Reactivo limitante (reacciona todo): el Cl2
A la hora de efectuar los cálculos ha de tenerse presente que parte del CS2 quedará sin reaccionar. Por tanto, ha de usarse, bien el reactivo limitante (reacciona totalmente), o bien la parte que reacciona del reactivo en exceso:
Usando el reactivo limitante:
$$2,82 \cancel{\textsf{mol Cl}_2} \frac{1 \textsf{ mol S}_2\textsf{Cl}_2}{3 \cancel{\textsf{ mol Cl}_2}} \frac{135,0 g \textsf{ S}_2\textsf{Cl}_2}{1 \cancel{\textsf{ mol S}_2\textsf{Cl}_2}} = 126,9 g \textsf{ S}_2\textsf{Cl}_2$$Las materias primas (reactivos) con que se fabrican los productos químicos en escala industrial, así como los reactivos de laboratorio, nunca son 100% puros, sino que contienen distintas cantidades de impurezas. Estas impurezas no van a reaccionar y por lo tanto deben tenerse en cuenta al momento de realizar los cálculos estequiométricos. En los reactivos que se adquieren comercialmente, las impurezas están especificadas como se muestra en la siguiente etiqueta. En las especificaciones no solo se da el valor de pureza (riqueza), sino que además se detallan las diferentes impurezas.
Determinación de la pureza de un reactivo.
Ejemplo: Una muestra impura de $50,0 g$ de cinc reacciona con $53,7 g$ de ácido clorhídrico. Calcular el % de zinc presente en la muestra (riqueza)
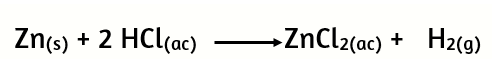
La cantidad de cinc presente en la muestra se puede calcular a partir del ácido consumido suponiendo que las impurezas no reaccionan con el ácido:
El cálculo de la pureza se reduce a calcular un tanto por ciento:
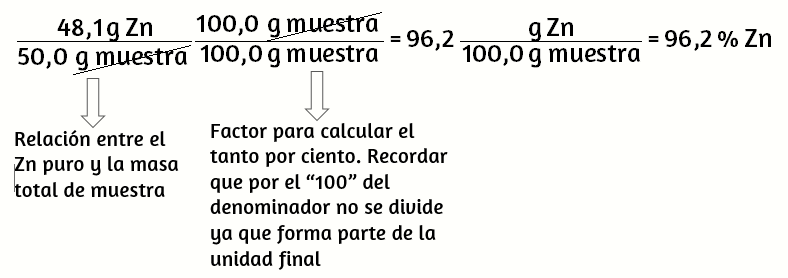
En cualquier proceso químico, ya sea a escala industrial o de laboratorio, la cantidad de producto que se obtiene es siempre menor que la calculada teóricamente (por la proporción estequiométrica) porque hay factores que afectan al proceso químico, principalmente factores técnicos, por ejemplo: el tiempo y la forma de calentamiento, la presión a la que se trabaja (para los gases), la eficiencia del catalizador empleado, la construcción del equipo utilizado, etc.
Por lo tanto hay que definir lo que se conoce como rendimiento de una reacción, que es el porcentaje real obtenido, en relación con el valor teórico calculado.
$$\% \textsf{Rendimiento} = \frac{\textsf{Producción real (dada)}}{\textsf{Producción teórica (calculada)}} × 100$$El rendimiento de una reacción química es muy importante en la industria, ya que determina la rentabilidad económica del proceso. Un bajo rendimiento obliga a investigar y probar nuevas técnicas y distintos procesos para mejorar la eficacia de la producción.
Ejemplo: El nitrato de plomo(II) reacciona con el yoduro de potasio para dar un precipitado amarillo de yoduro de plomo(II).
a) Plantear y ajustar la ecuación correspondiente al proceso.
b) Cuando se hacen reaccionar $15,0 g$ de nitrato de plomo(II) se obtienen $18,5 g$ de yoduro de plomo(II) ¿Cuál es el rendimiento del proceso?
a) Ecuación ajustada:
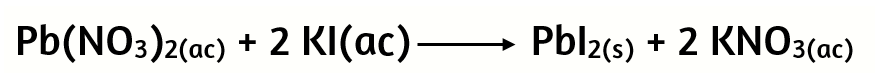
b) Gramos de yoduro de plomo(II) que deberían obtenerse teóricamente:
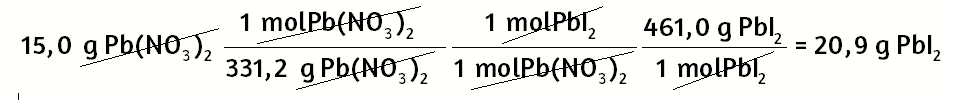
c) Cálculo del rendimiento:


"Pasteur a los jóvenes científicos: No os dejéis corromper por un escepticismo estéril y deprimente; no os desalentéis ante la tristeza de ciertas horas que pasan sobre las naciones. Vivid en la serena paz de los laboratorios y las bibliotecas". (Louis Pasteur)

Con estas prácticas de laboratorio, se pretende que aquellos que están interesados en aprender a fabricas algunos productos de aseo, e incluso aquellos de uso personal, de uso diario., por lo que las formulaciones que se incluyen corresponden a aproximaciones a los productos que se comercializan en los supermercados, por lo tanto, estos se podrán ajustar adicionando ciertos reactivos que en su momento ofrecerán una mayor protección antibacteriana, o mejor suavidad en caso de productos para el cuerpo, o el cabello, así mismo, si se tratara de alguna loción podrá activarse su aroma.
Para las prácticas diseñadas para la elaboración de estos productos, aparte de las normas de manejo y comportamiento en el laboratorio, con el objetivo de manejar adecuadamente las cantidades requeridas en la formulación, es recomendable que se disponga como mínimo de los siguientes implementos: medidores de volumen, medidores de masa, la balanza, medidores de temperatura, termómetro, papel indicador de pH, si se requiere, será necesario un destilador, un viscocímetro, recipientes para mezclas en acero inoxidable y canecas para almacenamiento debidamente esterilizadas, lo mismo, que agua destilada.

Vasos de Precipitados: Son vasos de cristal con escala impresa en su exterior. Se pueden utilizar para medir volúmenes, aunque no sería con tanta precisión; son para cuando las mediciones no son tan exigentes tubo de ensayo: Tubo de cristal, cerrado por uno de sus extremos, que se utiliza para hacer análisis químicos.
Probeta: Está formado por un tubo generalmente transparente de unos centímetros de diámetro y tiene una graduación desde 5 ml hasta el máximo de la probeta, indicando distintos volúmenes. Puede estar constituido de vidrio (lo más común), o de plástico. La ventaja de ser de vidrio es que las mediciones van a ser más exactas comparada con una probeta de plástico.
Matraz Erlenmeyer: Se trata de un frasco de base plana, cuerpo en forma de cono y cuello cilíndrico que se utiliza para contener o calentar sustancias líquidas.
Balanzas: La balanza es un instrumento que sirve para medir la masa. La balanza analítica es una clase de balanza utilizada principalmente para medir pequeñas masas.

Además, se debe contar con un termómetro, papel indicador de pH, recipientes de acero inoxidable, espátula metálica, agua destilada.
En cuanto a la interpretación de las mezclasen porcentaje se ha de tener presente que:
Cuando se requiere adicionar a una mezcla 10% de carboximetil celulosa (CMC), se debe interpretar: que para $100$ gramos del producto se requieren $10$ gramos de CMC.
Si el porcentaje se refiere al agua, por ejemplo, 40% de agua, se debe interpretar: que para $100$ gramos o $100$ mililitros de producto se necesitan $40$ gramos de agua.
Cuando se trabaja con productos que se declaran como c.s o c.s.p quiere decir que se debe completar la fórmula con el componente respectivo.Las diferentes formulaciones que se presentan en este capítulo han de ser ajustadas utilizando posiblemente, algún aroma, suavizante, o ajustar según la región, con su presión y temperatura. Estas han sido autorizadas por el Ingeniero Mauricio Escobar Valencia, para su reproducción total o parcial de su libro Química Objetiva, con documento en notaria 11 de la ciudad de Medellín, el día 11 de noviembre de 2007. Al iniciar la obtención de algún producto, debe realizarse bajo las normas de seguridad e higiene establecidas para los laboratorios, teniendo presente que algunos de los reactivos utilizados son tóxicos, así entonces, la manipulación y obtención de cualquiera de estos productos es bajo la responsabilidad de quien utiliza cada formulación
Se obtiene un moderno líquido que no mancha ni opaca y posee un excelente efecto limpiador, quedando el vidrio completamente transparente y brillante, este producto debe ser aplicado usando un rociador y secando luego con un paño seco y limpio.
Para $100 Kg$ de limpiador de vidrios.
Se obtiene un líquido limpiador con amplio poder desengrasante y gran formación de espuma. Dejando limpios y brillantes los utensilios de cocina:
Para preparación de $100 Kg$ de lavaplatos.
Procedimiento: Calentar el agua a $70° C$ y agregar Sales de Amonio Cuaternario, en un recipiente aparte mezclar sobre el agua, mientras se revuelve suavemente, envasar inmediatamente para evitar la evaporación del perfume. Agregar Colorante Vegetal al gusto.
Para su preparación se requiere:
Preparación: Mezclar el agua con el Texapón y diluirlo, hasta que el texapón desaparezca a lo que esto haya sucedido agregamos el restantes de los ingredientes, revolvemos bien. Envasamos rápidamente listo.
NOTA: Arreglar el Ph de 6 a 9 con Ácido Cítrico. Utilizamos Peachímetro.
Para su preparación se requieren los siguientes reactivos:
Preparación: En un recipiente plástico, agregamos el agua y disolvemos el Texapón en esta, hasta que esté completamente diluido. Una vez logrado esto, agregamos en orden el resto de los reactivos y mezclamos lentamente, hasta que sea homogénea. Envasamos rápidamente y listo para ser utilizado.
NOTA: Si queremos que el producto sea más denso, agregamos Cloruro de Sodio (NaCl) en pequeñas cantidades hasta obtener lo deseado.
NOTA: El Ph arreglarlo de 4 a 8 con ácido cítrico o con TEA (Trietenolamina).
Para su preparación, se requiere:
Preparación: En un recipiente de aluminio hervimos el agua con el metil parabeno y el color al mismo tiempo, en otro recipiente derretimos el suavitex al baño María (es decir, derretir el producto en una olla con agua caliente, sin sacar el producto de su envase). Se lo agregamos al agua y por último la fragancia y el color, mezclar muy bien, a medida que la mezcla baja de temperatura, va tomando presentación más viscosa similar las que existen en el mercado. Envasamos y listo para ser utilizado e lavadora.
Para su preparación, se requieren los siguientes reactivos:
Preparación: En un recipiente plástica agregar el agua y el CMC y lo disolverlo hasta que quede el agua sin residuos, puede disolverse con las manos o con una batidora o esperar su hidratación por unas horas. A lo que esto haya sucedido, agregar el Metil Sódico que es el preservante, luego agregar la fragancia con la Cumarina, o el PPG-20, el Arkopal y mezclar bien estos tres productos, para luego adicionarlo a la primera mezcla, mezclando bajo agitación continua. Por último, agregar el resto de los reactivos, mezclar bien y dejar por espacio de dos días, bien tapados para que la mezcla tome cuerpo o concentración. Pasado este lapso de tiempo, proceder a envasar, (este producto es tipo fabuloso).
NOTA: Si se va a fabricar desinfectante con fragancia de Lavanda, el colorante deberá ser Anilina Mineral de color violeta. Este colorante hay que disolverlo aparte, en un litro de agua, agitar bien y en el momento de aplicárselo a la mezcla, en la boca del litro ponemos papel de filtro, esto es con el fin de filtrar el colorante, ya que contiene unas pequeñas piedrecitas que al caerle al piso, lo manchan. Si se utiliza colorante vegetal no hay necesidad de hacer este procedimiento. Arreglar el Ph de 8 a 12 con Trietalonamina, y luego medir su pH, debe utilizar Termómetro para productos químicos.
Los reactivos requeridos para obtener este producto (tipo sampic)
Preparación: En un recipiente plástico, agregar el agua más el CMC y agitar fuertemente hasta que el CMC se mezcle completamente, (este aumenta la viscosidad la mezcla). Después agregar el resto de los reactivos en orden, mezclar y dejar reposar por espacio de dos días, luego envasar.
Los reactivos requeridos para obtener este producto son:
Preparación: Mezclar el color a la grasa con el acetato y luego homogenizar bien, por último agregar los demás reactivos. Envasar.
Los reactivos requeridos para obtener este producto son:
Preparación: En un recipiente plástico mezclar todos los reactivos en orden, menos el agua, mezclar bien hasta lograr que quede una mezcla homogénea, después vamos adicionando el agua poco a poco hasta que se vaya formando una crema, una vez logrado esto, empacar rápidamente en moldes plásticos y dejar secar por dos o tres días.
NOTA: Arreglar el Ph de 8 a 11 con Glicerina. Utilizar Termómetro.
Los reactivos requeridos para obtener este producto son:
Preparación: En un recipiente de peltre o aluminio, agregar los primeros cuatro reactivos, mezclar bien y poner al fuego lento hasta que los productos se fundan: al mismo tiempo, en otro recipiente de esmalte o de aluminio agregar el resto de los reactivos, menos el aroma y el color y también llevar al fuego lento hasta que alcance una temperatura de $80°C$ (o sea, que esté a punto de ebullir), una vez logrado este proceso unir las dos mezclas bajo agitación continua, hasta el punto de crema por último agregar la fragancia y el color, se le prueba el pH, que deberá ser de 9 hasta neutro.
NOTA: Si el pH se excede a lo establecido, rebajarlo con ácido muriático.
El Detersin-CR, es utilizado en hospitales y clínicas como excelente desinfectante, bactericida y germicida, úsese también en el lavado de ropa, vajillas, pisos, baños, piscinas, etc.
PRECAUCION: En la fabricación de este producto utilizar guantes, mascarillas, gafas y ropa adecuada; mantener fuera del alcance de los niños.
Es un aceite mineral utilizado por décadas en diferentes aplicaciones a nivel cosmético para limpiara y suavizar la piel, de fácil elaboración casera, de uso únicamente exterior, no afecta la piel con reacciones alérgicas de muy buen comercio.
Los reactivos requeridos para obtener este producto son:
Preparación: mezclar estos dos componentes para empacarlos preferiblemente en envases plásticos de buena calidad.
Para la reparación de dos litros y medio, se requieren los siguientes reactivos:
Preparación: en un recipiente preferiblemente de plástico se mezcla el carbopol 940 con el agua y la trietanolamina por 3 minutos y se deja reposar por 20 minutos para que se forme el gel, en otro recipiente aparte se prepara la silicona cosmética el pvp el etanol y la esencia y se mezcla hasta que el pvp este bien disuelto y se le adiciona al gel agitando moderadamente por 5 minutos y por ultimo el color previamente disuelto en agua.
Este tipo de producto es utilizado en centros de estética, obteniendo buenos resultados, siempre y cuando sea ayudado por una dieta y una rutina de ejercicios, ningún gel hace milagros, lo que hace es actuar como placebo y eso funciona, aquí, generalmente, lo que se logra es una deshidratación de la piel, cuando se aplica este gel se debe de caminar mínimo por 1 hora, y dejarlo por no menos de 15 minutos, para retirarlo con abundante agua.
Para su preparación, se requiere:
Preparación: en un recipiente preferiblemente de plástico se mezcla el carbopol 940 con el agua y la trietanolamina y el metilparabeno por 5 minutos y se deja reposar por 1 hora para que se forme el gel, en otro recipiente aparte se mezcla muy bien el resto de los componentes dependiendo que tipo de gel se quiera obtener frío o caliente reafirmante, agitando continua y moderadamente por 10 minutos y se le adiciona al gel agitando moderadamente por otros 5 minutos y por ultimo el color previamente disuelto en agua, se debe dejar reposar 2 horas el gel liporeductor antes de empacarlo.
Este producto contiene preparados botánicos, se trabaja con diferentes tipos de platas medicinales que ayudan a mantener la piel suave y libres impurezas causadas por el medio ambiente y el estrés.
Para obtenerlo en laboratorio se requiere de los siguientes reactivos:
Preparación: lo primero que debemos hacer es tratar el agua agregando el extracto natural, en el caso de la manzana por cada litro de agua 3 manzanas medianas rojas, las que se llevan a ebullición por 7 minutos, ésta un relajante natural; la manzanilla y la caléndula igualmente se llevan a ebullición por 7 minutos, $50$ gramos por litro, ellas, limpian las impurezas de la piel; la miel $50$ gramos por litro para hidratar la piel seca; el durazno, $50$ gramos, también se hierve por 7 minutos, por cada litro, para limpiar la piel de espinillas; el pepino cohombro, el que se hierve por 7 minutos para cerrar poros; jugo y cáscaras de mandarina para la celulitis, 3 mandarinas medianas por litro; venas varices o gota, tomillo, salvia y romero se dejan hervir en el agua por 20 minutos; $50$ gramos de hoja de calabaza se hierve 15 minutos, manchas en la piel; astringente $30$ gramos de hojas de menta se dejan hervir 20 minutos; angustia y estrés, lavanda $20$ gramos por litro, se hierven por 15 minutos, también puede utilizar la ruda.
Lo segundo que debemos hacer es el gel, en un recipiente plástico mezclamos el agua (tratada con los extractos), el metilparabeno, el carbopol y la tietranolamina por 5 minutos luego lo dejamos reposar que se forme el gel por una hora para adicionar el resto de los componentes agitando continua y moderadamente y se deja reposar otra hora antes de empacarlo.
Este producto se utiliza con fines medicinales para aminorar dolencias musculares y para resfriados como antidescongestionante nasal.
Para su preparación, se requiere:
Preparación: en un recipiente metálico se mezcla el ácido esteárico y el aceite mineral y se colocan en la estufa, a baja temperatura hasta que se disuelva bien el ácido esteárico con constante agitación, una vez disuelto se le agrega el mentol cristalizado y se continua agitando hasta que se disuelva por completo, cuando termina el proceso pasamos a hacer la prueba de solidificación, vertimos un poco en un plato y lo dejamos secar 2 minutos para analizar su consistencia la cual debe quedar no muy dura, de tal manera que permita untarse en los dedos fácilmente, cuando se quiera mas sólida se la agrega mas ácido esteárico, al contrario si se quiere mas blanda se le adiciona mas aceite mineral, el mentol cristalizado se puede variar en su cantidad, y agregarle un poco más, siempre tratando de prevenir reacciones alérgicas, para empacarlo no debe estar muy caliente, se debe de tapar superficialmente para que no pierda el brillo mientras termina el proceso de secado, luego que solidifique se tapa herméticamente, se puede empacar en cualquier tipo de envases, plástico, vidrio e incluso en tubos.
Con esta formulación, se obtiene un líquido que no mancha ni opaca y posee un excelente efecto limpiador, quedando el vidrio completamente transparente y brillante.
Productos desinfectantes con fuerte fragancia tipo Lavanda, requieren de los siguientes reactivos para su producción.
Procedimiento: Calentar el agua a $70° C$ y agregar Sales de Amonio Cuaternario, en un recipiente.
aparte mezclar sobre el agua, los demás reactivos, mientras se mezcla suavemente, envasaren recipiente apropiado. Agregar Colorante Vegetal al gusto.