Química en la vida cotidiana
EL JABÓN
John Jairo García MoraSonia Jaquelliny Moreno Jiménez
Química en la vida cotidiana: el jabón
Margarita Emilia Patiño Jaramillo
John Jairo García MoraSonia Jaquelliny Moreno Jiménez
Instituto Tecnológico Metropolitano
Córdoba (España)
2022
Título de la obra:
Química en la vida cotidiana: el jabón
Autores:
Margarita Emilia Patiño Jaramillo
John Jairo García Mora
Sonia Jaquelliny Moreno Jiménez
Código JavaScript para el libro: Joel Espinosa Longi, IMATE, UNAM.
Recursos interactivos: DescartesJS
Fuentes: Lato y UbuntuMono
Red Educativa Digital Descartes
Córdoba (España)
descartes@proyectodescartes.org
https://proyectodescartes.org
Proyecto iCartesiLibri
https://proyectodescartes.org/iCartesiLibri/index.htm
ISBN: 978-84-18834-37-0

Esta obra está bajo una licencia Creative Commons 4.0 internacional: Reconocimiento-No Comercial-Compartir Igual.
Tabla de contenido


Introducción
Este libro interactivo muestra la importancia de la química en la vida diaria de los seres humanos, pues gracias a esta ciencia, nuestra esperanza de vida se ha duplicado en los últimos 100 años, contribuyendo en áreas como el diagnóstico, la prevención y el tratamiento de enfermedades. Baste mencionar que la aplicación de la química a la farmacología ha hecho posible la elaboración de vacunas, antibióticos y todo tipo de medicamentos, que han supuesto una reducción drástica de los índices de mortalidad.
 A ellos debemos uno de cada cinco años de nuestra vida y gracias a ellos podemos vivir en mejores condiciones hasta edades más avanzadas.
A ellos debemos uno de cada cinco años de nuestra vida y gracias a ellos podemos vivir en mejores condiciones hasta edades más avanzadas.
Y, en la cotidianidad, se utilizan gran cantidad de productos para una buena convivencia, por lo que se tratará, entonces, de la importancia de los implementos de aseo personales, como es el jabón, el champú, desinfectantes, desengrasantes y algunos compuestos cosméticos.
Al escuchar la palabra química muchas personas lo asocian con “peligro” o con “la comida ya no es natural, lleva cantidad de productos químicos que son nocivos”. De lo que no somos conscientes es de que la química está presente todo el día en nuestra vida, de no ser por la química no tendríamos medicinas, agua limpia, gasolina para los vehículos, vajillas y vestido entre infinidad de productos.
Video: Química en la vida cotidiana Fuente del video: autores. Imagen de Karolina Grabowska.
La Química es una ciencia activa y en constante crecimiento, cuya importancia resulta vital en nuestro mundo. Se encuentra presente en prácticamente todas las actividades de nuestra vida diaria. Por ejemplo, al alimentarnos, la comida nos proporciona energía que se produce mediante diferentes reacciones químicas dentro de nuestras células.
Esa energía la usamos para correr, jugar, estudiar y trabajar, entre otras actividades. En este momento puedes leer sin problemas gracias a que en tu cuerpo se está liberando energía proveniente de las reacciones químicas que, sin darte cuenta, se están generando en tu organismo.
También los alimentos mismos que consumimos (carne, leche, frutas y otros) son producto de reacciones químicas complejas. En la naturaleza, estas reacciones se efectúan diariamente en los organismos. Un ejemplo es la fotosíntesis. A través de ella, las plantas sintetizan sacáridos (familia de compuestos que incluyen el azúcar) que son almacenados en órganos especializados, como las frutas que comemos (ahora sabes por qué las manzanas y las peras son dulces). Y así podemos seguir enumerando muchas otras reacciones en las cuales la química se hace presente en nuestras vidas.
La química está presente cuando fumas un cigarrillo, cuando lavas la ropa o cuando te bañas, cuando respiras y hasta cuando escribes en tu cuaderno.
Todo lo que tenemos a nuestro alrededor es química, no la podemos desligar de nuestra vida, tanto es, para el cuidado de nuestro cuerpo utilizamos una amplia variedad de productos como jabón, champú y la pasta de dientes entre otros.
También los productos cosméticos y los perfumes que contribuyen a mejorar nuestro aspecto diario tienen su origen en la Química. A pesar de que estamos muy familiarizados con estos productos, la mayoría de las personas desconocen su composición.
Muchas cremas cutáneas contienen proteoglicanos. Los proteoglicanos están constituidos por un núcleo proteico al que se encuentran unidos covalentemente un tipo especial de polisacáridos denominados glicosaminoglicanos, normalmente se encuentra en los tejidos conjuntivos del cuerpo (dermis y cartílagos) y su mecanismo de acción principal es la absorción de agua para mantener un nivel óptimo de hidratación en estos tejidos.
En este libro hablaremos de los jabones, de ellos podemos decir que están formados por moléculas con doble personalidad: a una les gusta el agua y a la otra, las grasas.
La importancia de estos productos de higiene es tal que según un estudio realizado sobre 120 países el uso del jabón es el principal responsable de la reducción de la mortalidad infantil.AGRADECIMIENTOS
Para esta producción, se ha requerido el apoyo de personas que con su sapiencia me han apoyado y dirigido, como ha sido el maestro Juan Guillermo Rivera Berrío, Vicerrector académico de la Institución Universitaria Pascual Bravo.
De los autores
MARGARITA EMILIA PATIÑO-JARAMILLO
Profesora Asociada del Instituto Tecnológico Metropolitano

- Ingeniera Química
- Tecnóloga Textil
- Especialista en docencia universitaria
- Posgrado en didáctica de las ciencias con énfasis en matemáticas y física
- Master en educación (ambientes virtuales de aprendizaje)
JOHN JAIRO GARCÍA-MORA
Profesor Titular 2 del Instituto Tecnológico Metropolitano

- Tecnólogo Mecánico
- Licenciado en Educación: Tecnología
- Especialista en Docencia Universitaria
- Especialista en Gestión Energética Industrial
- Master en Educación y Desarrollo Humano
SONIA JAQUELLINY MORENO-JIMÉNEZ
Investigadora del Instituto Tecnológico Metropolitano

- Tecnóloga en Calidad
- Tecnóloga en Producción
- Ingeniera de Producción
- Diplomada en Pedagogía
- Master en Gestión de la Innovación Tecnológica, Cooperación y Desarrollo Regional

Conociendo el jabón
Descripción del jabón
Todos los días nuestras actividades comunes nos ponen en contacto con este producto químico, y sólo necesitamos saber que sirve para limpiar, que suele tener un olor agradable y que sus formas pueden ser variadas. El impacto de la demanda de este producto se observa en los métodos empleados para elaborarlo. La química detrás de este producto responde a varias incógnitas: ¿Cómo funciona un jabón?, ¿Por qué hace burbujas?, ¿Por qué limpia?, ¿De dónde viene? ¿Por qué sus diferentes presentaciones?, ¿Es lo mismo jabón y detergente?

Introducción
A los jabones les debemos uno de cada cinco años de nuestra vida y gracias a ellos podemos vivir en mejores condiciones hasta edades más avanzadas.
Todo comienza con las grasas de origen animal o aceites vegetales que se transforman en jabones. No es cuestión de magia: Esto se llama química, e implica una reacción muy sencilla denominada saponificación. Un jabón contiene las sales de sodio o potasio de los ácidos grasos, producto de la mezcla de un cuerpo graso (triglicéridos con un álcali, que puede ser hidróxido de sodio o de potasio).Wade, Leroy (2004) Química orgánica, Madrid: Pearson educación. p. 1162-1168.
Historia del jabón
En la Prehistoria, aunque no se sabe cuándo, se usaba una mezcla de ceniza y agua, que era un agente de limpieza más eficaz que el agua sola.
Se sabe que los fenicios, griegos y romanos ya usaban algún tipo de jabón. En la antigua Roma se fabricaba un jabón mediante cocción de una mezcla de cenizas de madera, grasas animales y caliza. Durante la Edad Media, el jabón era un artículo de lujo al que pocos tenían acceso. A lo largo de los siglos, se ha fabricado jabón de forma artesanal empleando cenizas vegetales y sustancias grasas. Esa mezcla fue encontrada por los esclavos que trabajaban en el río, los que notaron sus propiedades para limpiar sus manos y la ropa.
La primera referencia literaria sobre el jabón fue encontrada en tabletas de la arcilla realizadas en los años 3000 A.C.
en la Mesopotamia. Ahí se podía observar una receta para hacer jabón con una mezcla de potasa y aceite. Los restos de jabón más antiguos que se han encontrado son de origen babilónico, que datan del año 2800 A.C. estos restos de jabón fueron hallados en tarros de arcilla, donde ellos describían como una mezcla de grasas con cenizas, pero no se menciona su uso.
Posteriormente, en 1.550 A.C. un papiro egipcio, hace referencia a la utilización de sustancias jabonosas para el lavado de ropa y para el tratamiento de enfermedades de la piel, este producto consistía en una mezcla de agua, aceite y ceras vegetales o animales.
Alrededor de los años 600 A.C. los fenicios utilizaban el jabón en la limpieza de las fibras textiles de lanas y en la preparación para tejer los paños.
En Medio Oriente el uso y tratamiento de la grasa con el álcali es usado desde hace unos 5000 años. Donde los antiguos israelíes habían escrito unas leyes que sobre la limpieza personal.
Los escritos bíblicos relatan que al mezclarse cenizas y aceite se obtenía un producto para lavar el pelo. Se cree la fabricación de jabón fue traído a Europa por los fenicios en los años 600 A.C.. Parece que al principio el propósito del jabón era estrictamente medicinal para distintos tratamiento en la piel, fue a partir del los años 200 D.C. que se utilizo para la higiene.En textos romanos de historia del año 77 D.C. relatan que los galos hacían el jabón con el sebo de las cabras y la ceniza de la haya (potasa), utilizándolo como un tinte y ungüento para el pelo. También menciona el uso de la sal común, agregada a la mezcla, para endurecer las barras de jabón. Galema, Titus. Oblitas, Samuel. Castellvi, Xavi.Manual de Jabón. Teoría y desarrollo práctico a escala local. Disponible aquí
Con la caída del imperio romano, la fabricación de jabón en Europa fue desapareciendo pero alrededor de los años 700 D.C. la fabricación de jabón se convierte en un arte en Venecia y se registra su exportación.
En los años 1100 D.C. en Inglaterra es usado un jabón de origen francés, utilizado por las clases altas. Era una mezcla de la grasa del cordero, ceniza de madera y soda cáustica, la cual que conservaba la textura de la grasa.
En los años 1200 D.C. Marsella, Génova, Venecia y Savona se convirtieron en centros del comercio del jabón debido a su abundancia local de depósitos de aceite de oliva y de soda.
La mayoría de los fabricantes de jabón no tenía ninguna idea acerca de lo que ocurría durante el proceso. Ellos empleaban el método de ensayo y error, confiando en la suerte, y creyendo en muchas supersticiones.
En los años 1400 D.C. aparece el jabón de Marsella, el precursor de los jabones actuales, preparado con una mezcla de huesos que son ricos en potasio y grasas vegetales. La fabricación de jabón siguió siendo un arte relativamente primitivo hasta el los años 1500 D.C. cuando se desarrolladas las técnicas que proporcionaron un jabón más puro.
Los primeros colonos norteamericanos una vez instalados, prepararon su propio jabón para no depender de los envíos ingleses. Para ello usaban ceniza de madera y grasa de animales.
En 1783, el químico sueco que Carl Wilhelm Scheele hirvió aceite de oliva con óxido del plomo, produciendo una sustancia que llamó glicerina. Esta reacción es la que ocurre en el actual proceso de fabricación de jabón.
El descubrimiento de la glicerina estimuló a otro químico francés, Michel Eugène Chevreul, a investigar la química de las grasas y de los aceites empleados para fabricar jabón. En 1823, descubre que las grasas simples se descomponen en presencia de un álcali para formar los ácidos grasos y los gliceroles.
Con todo esto, la fabricación del jabón alcanza la madurez en 1791, cuando el químico francés Nicolas Leblanc, inventó un proceso para obtener el carbonato de sodio, o soda, de la sal ordinaria.
Durante la 2º Guerra Mundial, los americanos desarrollaron un tipo de jabón que podía utilizarse con agua del mar, así nació el jabón dermatológico, el menos agresivo de todos los jabones.
La línea del tiempo en la historia del jabón:
Es de anotar que no es hasta el siglo XIX, cuando los científicos descubren el papel de las bacterias en el desarrollo del mal olor, que aparecen los primeros desodorantes y consigo los primeros jabones bactericidas.
Química del jabón
Un jabón es un producto de primera línea en su uso, pero su formulación implica lograr el equilibrio entre muchas de sus características, la dureza, la formación de espuma, la limpieza, el aroma, la duración, la cremosidad, entre varias otras.
En la fabricación del jabón, los carácteres físicos y químicos del producto dependen directamente de las materias primas empleadas. De las grasas y aceites se emplean el sebo, la manteca, aceite de nueces, los residuos de la refinación y del endurecimiento de aceites de semilla y algunos aceites marinos.
El jabón generalmente es el resultado de la reacción química entre un álcali (normalmente hidróxido de sodio o de potasio) y algún ácido graso (manteca de cerdo o aceite de coco) esta reacción se denomina saponificación y consiste en una reacción química entre un ácido graso y una base o alcalino en la que se obtiene como principal producto la sal de dicho ácido y de dicha base. Estos compuestos tienen la particularidad de ser anfipáticos, es decir tienen una parte polar y otra apolar, con lo cual pueden interactuar con sustancias de propiedades dispares.
Gráficamente explicado, sucedería la siguiente reacción:
Ácido Graso $\space \longrightarrow \space$ Éster + Agua
Principales reactivos para jabón
Agua
Para obtener los mejores resultados, debemos utilizar agua de lluvia, destilada, o agua desmineralizada.
Soda cáustica o lejía
Se trata de una sustancia química, una base muy fuerte llamada hidróxido de sodio, NaOH. Si se aspira, ingiere o se tiene contacto con la piel o los ojos resulta muy peligrosa.
Nunca debe estar al alcance de niños o animales. También afecta las ollas de aluminio. Es necesario tener especial cuidado en la elección de los utensilios y envases a utilizar para mezclar manejar y conservar la lejía
Utilice cucharas de madera o de plástico y ollas esmaltadas, de plástico o de cristal. Para protegernos debemos usar protetor para los ojos y guantes de caucho al manejar los cristales de la lejía o la solución de la lejía después de haberla mezclado en el agua.
Disuelva la lejía en agua fría. Cuanto más fría mejor. Nunca vierta el agua en la lejía. Hacer esto podía hacer que la mezcla explote. Vierta siempre la lejía en el agua. Si usted no la mezcla inmediatamente mientras la vierte en el agua, la lejía se irá al fondo y solidificará rápidamente. De todos modos no es un problema ya que golpeándola ligeramente con el utensilio de mezcla lo disolverá.
Cuando se realiza la mezcla, ocurre una reacción química entre la lejía y el agua que genera calor (cerca de 80ºC, reacción exotérmica).
Pero si se está haciendo una producción grande de jabón, la lejía puede incluso comenzar a hervir el agua con las pequeñas gotitas del agua de la lejía salpicando peligrosamente, entonces, si esto comienza a suceder, pare de mezclar hasta que cese de burbujear. Generalmente, no toma más que un minuto disolver los cristales de soda cáustica en el agua. Se dará cuenta porque el agua se pondrá relativamente clara. Antes de usar el agua de la lejía debe enfriarse a la temperatura ambiente para poder agregarla a la grasa.
El NaOH o álcali, es el agete saponificador o neutralizante. En el procedimiento ordinario para hacer jabón se usa el cloruro de sodio en grandes cantidades para precipitar el jabón de su solución en la lejía.
Los jabones potásicos, que se hacen empleando como álcali el hidróxido de potasio, también conocido como potasa cáustica, son más solubles en agua que los de sodio, y son los denominados jabones blandos. No pueden precipitarse de la lejía por el cloruro de sodio, porque se formaría jabón de sodio.
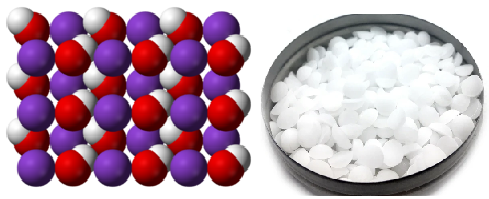
Clic aquí para ver en la Web
Las combinaciones de las dos clases de jabones tienen las deseables características de los jabones duros mas la rápida solubilidad y la facilidad de formar gran cantidad de espuma, característica peculiar de los jabones blandos.
Grasas y aceites
Casi cualquier grasa o aceite se puede utilizar para hacer jabón. Las grasas para la fabricación de jabón incluyen las grasas animales tales como sebo (de la carne vacuna), manteca de cerdo (grasa de cerdo), y los aceites derivados de diferentes plantas como son (oliva, maíz, girasol, etc.) y las grasas hidrogenadas.
Las grasas animales tienen diferente dureza, el sebo de vaca es duro, la manteca de cerdo de dureza media y la grasa de pollo más blanda. Se acepta generalmente que las grasas más duras hacen un mejor jabón, por lo tanto, hay que tener en cuenta que uno de los ácidos grasos más convenientes en los jabones son el láurico, el mirístico, el palmítico y el oleico, que contienen de 12 a 18 átomos de carbono.
Los ácidos mencionados anteriormente son saturados, excepto el oleico, forman la mayor parte de la materia del sebo y del aceite de coco. Este aceite y el sebo, en relaciones de 3:1 y 4:1, se utilizan en la mayoría de los jabones fabricados para lavanderías y para el tocador. Las fórmulas dependen de la calidad deseada sobre el producto terminado.
Es evidente que los carácteres de los jabones están directamente relacionados con los ácidos grasos de las materias primas utilizadas, por lo que es conveniente saber lo que hará una grasa particular para la porducción de calidad, así que es recomendable que haga una producción pequeña solamente usando la grasa en cuestión y vea qué resultados consigue.
Los ácidos mencionados anteriormente son saturados, excepto el oleico, forman la mayor parte de la materia del sebo y del aceite de coco. Este aceite y el sebo, en relaciones de 3:1 y 4:1, se utilizan en la mayoría de los jabones fabricados para lavanderías y para el tocador. Las fórmulas dependen de la calidad deseada sobre el producto terminado.
Aparte que las materias primas utilizadas sean las adecuadas para una buena calidad del jabón, debe tenerse en cuenta que estos estén limpios y libres de impurezas. No deben ser rancios, tener exceso de sal ni contener partículas sólidas.
La grasa rancia y sucia puede ser limpiada hirviéndola por algunos minutos en una olla grande con cuatro partes de agua por cada parte de grasa. Una vez hervida déjela enfriar y cuando solidifique separe la grasa de la olla en una sola pieza.
Una forma para hacer esto es calentar con agua caliente el exterior del recipiente, esto derrite una capa delgada de grasa en el interior del recipiente lo que permite que salga con más facilidad. Cuando retire la grasa raspe toda la suciedad que habrá quedado en el fondo de la grasa. Si sigue sucia, repita el proceso de limpieza de nuevo.
El sebo y grasa animal
Las grasas animales se extraen del tejido adiposo de algunos animales y, dependiendo del origen, tienen diferentes características. Las grasas más comunes son el sebo y la manteca de cerdo y más recientemente se han incorporado al mercado otras más exóticas como la de emú o el avestruz.
Una de las grasas animales más frecuentes para hacer jabones es el sebo se suele obtener del ganado bovino, comúnmente de la vaca.
Se obtiene también otro sebo más duro del los carneros u ovejas pero suele ser menos habitual. La parte más rica en sebo suele ser alrededor de los riñones, que es le de mejor calidad, y recibe el nombre de sebo en rama. Este tipo de grasa contiene una mayor cantidad de ácido esteárico produciendo jabones más duros.
Las propiedades del sebo, salvando las diferencias, son equivalentes a la manteca de cacao ya que proporciona sobre todo dureza y cremosidad en la espuma. Produce jabones duros y blancos y se suele utilizar entre un 20 y un 40%. En algunos lugares el jabón se realiza con sebo y aceite de coco al 50%.
Los sebos se clasifican por el American Institute of Meat Packers según su color, su título, su porcentaje de ácidos grasos libres y su contenido de humedad, materia insoluble y materia insaponificable.
El título del sebo crudo es un factor importante para determinar la calidad del sebo y la dureza del jabón que éste producirá. El título se define como el punto de solidificación de los ácidos grasos contenidos en el sebo, expresado en grados centígrados. Una grasa cuyo título excede los 40ºC, se clasifica como sebo, y hasta 40ºC se considera como grasa o manteca.
El contenido de humedad, materia insoluble y materia insaponificable es material que no produce jabón.Jabones. Introducción. Ver documento original. El sebo de alto título produce jabones duros y el de título bajo, jabones blandos.
La manteca
La manteca es otra cosa. También se obtiene de la grasa animal pero normalmente del cerdo. Su tacto es más untuoso y recuerda al aceite de palma pero tiene un olor bastante fuerte.
Los jabones realizados con manteca son blancos, duros y bastante duraderos. Limpian bastante bien las manchas de la ropa y resultan suaves para la piel. A efectos prácticos también se parece bastante al aceite de palma por lo que no produce mucha espuma pero endurece más que ella. Se usa hasta un 40%.
Para obtener tanto una como otra, tienen bastante trabajo, haciéndose desde los despojos, pero a mí me parece que merece la pena probarlo ya que, como digo, producen jabones muy buenos.
Existen obviamente otras grasas animales como las grasas de pato o de pollo. Proporcionan características al jabón similares a la manteca. Cada una con sus peculilaridades en función de su composición.
Otros productos de origen animal para la elaboración de jabones
La lanolina, que se obtiene de la lana de las ovejas, es una grasa que se ha utilizado tradicionalmente para el sobreengrasado de los jabones. Proporciona suavidad y acondicionamiento en la piel y el cabello y su composición química es similar a la cera. Se conoce la lanolina anhidra (que no contiene agua) y POE que es soluble en agua por lo que puede resultar especialmente interesante para el sobreengrasado del jabón líquido. Esta última se somete a un proceso químico para que tenga estas cualidades.
La cera de abejas no es una grasa, pero sí un ingrediente frecuentemente utilizado en los jabones. Proporciona sobre todo dureza y también acondicionamiento. Se suele usar un máximo del 5% de la fórmula del jabón.
Para usar la cera de abejas en los jabones es necesario derretirla previamente en aceite caliente, mezclándola con éste hasta su completa disolución.
Aceites especiales para los jabones
Suelen ser los aceites que contienen más cantidad de ácidos linoleico y linolénico y estos deben de ser muy emolientes. Además contienen cantidades mayores o menores de ácido gadoleico, que los hace regenerativos, y vitaminas y oligoelementos que los hacen nutritivos de la piel.
Son aceites muy caros e inestables por lo que hay que apoyarlos siempre con vitamina E en una cantidad aproximada del 5% de su peso. Esta vitamina es un potente antioxidante que evita su enranciamiento.
El uso de estos aceites en el sobreengrasado de los jabones hace que sean más suaves y beneficiosos para la piel. Entrañan cierto riesgo del enranciamiento de los jabones por lo que hay que usarlos en pequeña cantidad.
Algunos aceites o ingredientes se suelen utilizar en pequeña cantidad, un máximo del 10%. A considerar en esta clasificación:
- Aceite de rosa mosqueta, que por su fama de regenerador de cicatrices y antiarrugas es el más solicitado. Es uno de los más inestables.
- Aceite de borago, es mucho menos conocido que el aceite de rosa mosqueta y por eso un poco menos caro pero su composición es muy parecida y su efecto también. Se utiliza también para tratamiento de pieles muy delicadas porque proporciona elasticidad.
- Aceite de argán. Seguimos con los aceites prohibitivos en cuanto a su precio. El efecto es similar al de los otros dos pero en este caso contiene menor cantidad de linólénico por lo que es un poco más estable. Tiene un olor profundo como de fruto seco un poco rancio.
- El aceite de jojoba no es un aceite propiamente dicho. Es más bien como una cera líquida. Tienen propiedades emolientes y humectantes y proporciona brillo en las composiciones para el cabello.
- Aceites como el de germen de trigo, semilla de uva, nuez o incluso el girasol son alternativas más baratas a estos aceites ya que su composición es similar. En estos casos también hay que usar la vitamina E.
- La manteca de karité es la excepción de todos ellos, en el sentido de su composición, porque caro es de narices. No tiene linoleico ni linolénico en cantidades apreciables pero sí vitaminas y oligoelementos. Además también está de moda. Tiene gran cantidad de ácido esteárico y es por eso que se presenta en forma de manteca, en estado semi-sólido. Proporciona cremosidad en la espuma y bastante suavidadMendrulandia. Aceites especiales y su aplicación en el jabón.
Aceites esenciales en el jabón
Aunque también se pueden utilizar fragancias o perfumes para dar olor a los jabones puede resultar de mejor gusto utilizar casi exclusivamente los aceites esenciales.
Ya no sólo porque sus propiedades son más efectivas y son más estables que las fragancias sino porque huelen mucho mejor las composiciones hechas con ellos. Eso no significa que no se puedan usar fragancias. Las hay que van muy bien para los jabones.
Se nombran entonces, una serie de esenciales en algunos casos por ser de la tierra y en otros por considerarlos indispensables. Hay muchísimos por lo que se hace una selección de unos pocos nada más. Para el uso de estos hay que tener buen olfato e imaginación.
Algunos aceites esenciales destacados
Iniciemos hablando de la reina de las esencias, la lavanda. Es la reina porque es un aroma que va bien en combinaciones femeninas, masculinas e infantiles. También sirve incluso para mascotas. Es decir, que va bien en cualquier caso.
Aunque algunas, pocas, personas la odian, generalmente a todo el mundo le gusta y aunque tiene un punto de amargo, recuerda al frescor del campo y a ropa limpia.
La lavanda combina muy bien con todas las que vienen a continuación y proporciona además un efecto relajante y es antiséptica.
En el apartado de elaboración de fragancias se habla de las diferentes notas aromáticas. La lavanda tiene una nota aromática alta.
- La esencia de
canelase debe usar en poca cantidad por que puede ser incluso irritante de la piel (en estado puro). Casi todo el mundo sabe como huele pero es un aroma dulzón y un poco picante. Combina muy bien con los cítricos.
- La esencia de
naranjaes exquisita, pero hay que utilizar gran cantidad para que se pueda percibir el aroma, pero hay que fijarla con otras esencias como el lemongrass, el pachuli o el sándalo si no queremos que desvanezca enseguida como el resto de cítricos.Existen versiones denominadas desterpenadas que, procediendo de esencias naturales, están modificadas para hacerlas más potentes.
La naranja combina muy bien con casi todo, con aromas florales, frutales y aguas de colonia. También tiene un efecto relajante y se supone que reafirmante de la piel.
- La esencia de
romeroes parecida a la lavanda pero más balsámica y resinosa, Combina muy bien con otras plantas aromáticas y con las esencias mencionadas anteriormente. Tiene efecto tonificante y estimulante de la memoria. Nota aromática media-alta - La esencia de
eucaliptoes una esencia muy frecuente y barata también. Es un aroma balsámico y penetrante pero muy volátil por lo que también conviene fijarlo con otras esencias.Aunque a priori no lo parezca, combina bien con aromas dulzones como la vainilla, el almizcle y los frutales. También combina bien con la menta y el árbol del té.
Tiene efecto antibacteriano e incluso antiparasitario, es bastante aromático.
- La esencia de
mejoranaes un aceite muy herbal pero también muy dulzón. Recuerda un poco al orégano pero es más complejo. Combina muy bien con todas las aromáticas y proporciona un sutil y delicado toque de hierbas en composiciones más sofisticadas.Es un poco más cara que las anteriores. Puede ser usado como antioxidante. Nota aromática media.
- La esencia de
árbol del tétambién se usa mucho. Tiene un aroma balsámico y profundo. Combina muy bien con las de tipo herbal y tiene muchas propiedades y aplicaciones. Las más frecuentes son como antiséptico, anit acné y anti parasitaria. - La esencia de
sándaloaunque tiene olor, se supone que se anula cuando se mezcla con otros aceites esenciales pero proporciona durabilidad fijándolos. Combina por tanto con casi todos los aceite esenciales y tiene un cuerpo más bien masculino.Es tipo madera dulce y tiene propiedades humectantes y relajantes, mejora el humor. Además también está clasificado como afrodisíaco. Nota aromática baja.
- La de
pachuli(también patchouli) es una esencia espesa reconcentrada que huele bien pero demasiado. Puede resultar empalagosa. Se usa en muy poca cantidad y como fijador principalmente.Combina con cítricos, flores y casi con cualquier tipo de esencia. Tiene propiedades antisépticas, anti acné, fungicidas, antiinflamatorias, antidepresivas y anti estrés.
- La esencia de
vetiver, que no es tan común, según la combinación, puede recordar al mar. Combina muy bien con los cítricos y con los florales, no tanto con los herbales. Proporciona serenidad y es un buen inductor para la meditación. Su olor es parecido al del pachuli.
Coloreando el jabón
Hay principalmente dos tipos de colorantes: líquidos y en polvo. Y de estos últimos también hay dos tipos: hidrosolubles y liposolubles, lo que significa que se mezclan o bien en agua o en aceite.
Los que se mezclan en aceite se pueden agregar al jabón desde un principio, por que así con el movimiento y eso, se disuelven mejor. Los hidrosolubles hay que mezclarlos previamente con agua y se suelen añadir después de la traza.
Si además queremos separar parte del jabón para colorearlo de otra manera, pues se lo añadimos una vez separado.
Los líquidos suelen utilizarse para los jabones de glicerina u otros cosméticos.
Para los jabones en frío suelen ir mejor los liposolubles que vienen en polvos.
Identificación de los colorantes cosméticos
Se identifican generalmente por el color index CI seguido de un número de 5 cifras o por su nombre. Por ejemplo el CI77007 es el azul ultramar (o ultramarino).
La base de jabón determinante del color
Se puede también utilizar como base para el color el colorante blanco conocido como dióxido de titanio. En condiciones normales es completamente inocuo y tiñe bastante de blanco por lo que produce jabones más blancos. Pero además, puede servir de base para afianzar mejor otros colores, que además tomarán un tono más pastel.
Por otro lado, jabones realizados con grasas más blancas producen jabones más blancos y éstos son más fáciles de colorear. Los colorantes, no obstante, deben de ser siempre de grado cosmético. De nada sirve gastar tiempo y dinero en hacer jabones si luego le vamos a poner cualquier ingrediente de origen y calidad dudosos.
Tanto los lipo como los hidrosolubles se pueden disolver en alcohol de 96º. Al principio la mezcla es estable pero al cabo de un rato el colorante se deposita en el fondo. Se agita un poco en el momento de su uso y está perfectamente utilizable. Así incluso se pueden mezclar para conseguir colores intermedios.
Otros agentes colorantes
Otra fuente de posibles colores son las arcillas. Las hay verde, blanca, rosa, roja, azul y gris, que yo sepa. Aportan también dureza y producen una suave exfoliación.
Como se ha referenciado en párrafos anteriores, los aceites utilizados para la elaboración del jabón también pueden darle color, así el de cáñamo proporciona un verde intenso, el aceite de zanahorias, el de rosa mosqueta o el de germen de trigo proporcionan distintos grados de naranja, el de oliva desde amarillos a verdosos que al final quedan más o menos marfil.
Por su parte, el coco, palmiste, sebo, manteca y karité producen jabones muy blancos que pueden resultar idóneos para ser coloreados.
Los colores naturales de origen vegetal como la clorofila o algas (para el verde), la cúrcuma (amarillo), el pimentón (rojo anaranjado), etc, son menos estables en el jabón y con el tiempo acaban perdiéndose. El caramelo, cacao o el café (para los marrones) son más estables.
Resistencia al pH de los colorantes en los jabones
Tanto si se utilizan óxidos, colores sintético o naturales, es importante que sean resistentes al pH elevado de los jabones en su momento de elaboración.
En algunos casos el color varia completamente a la acción cáustica y en otros vuelve a su color original cuando el jabón baja su pH. Hay productos que especifican su tolerancia al pH y para los jabones en frío es importante conocer ese dato.
Cantidad y pureza determinan el acabado
Cada colorante es un mundo por lo que sólo el fabricante (o el vendedor debidamente formado) te puede dar información precisa sobre ellos y sobre su uso y cantidad. También los hay de distinto grado de pureza. A priori parece mejor comprar los más concentrados, pero a la hora de la verdad, los otros son más fáciles de controlar.
Los hidrosolubles suelen migrar en los jabones de más de un color. Contaminando el color adyacente. Además colorean el agua cuando se usan y esto, a veces, resulta demasiado escandaloso.
Otros colorantes
Las micas de colores también se pueden usar pero no son otra cosa que mica con colorante (generalmente óxidos). De manera que tienen que ser también colorantes cosméticos que aguanten el pH al que lo exponemos. También existen colorantes sólidos. Suelen ser colorantes diluidos en ácido esteárico y que necesitan un poco de calor para repartirse bien.
Las sales y sus efectos en el jabón
Para entender como funciona en la masa de un jabón debemos de saber primero que la pasta de jabón es un coloide o sea, una emulsión con un comportamiento particular.
Emulsión o coloideLos coloides son mezclas heterogéneas de por lo menos dos fases diferentes con la materia de una de las fases en forma finamente dividida (sólido, líquido o gas), denominada fase dispersa, mezclada con la fase continua (sólido, líquido o gas), denominada medio de dispersión. La ciencia de los coloides está relacionada con el estudio de los sistemas en los cuales por lo menos uno de los componentes de la mezcla presenta una dimensión en el intervalo de 1 a 1000 nanómetros (1 nm = 10 -9 m). Aula química del jabón es más estable a mayor temperatura pero depende también de la concentración de sales que contenga. Si le agregamos un poco de una sal la emulsión, se vuelve más clara, menos espesa, pero si el nivel de sales es mayor, se desestabiliza y descompone en dos fases: acuosa y grasa. Si agregamos sales desde la fase inicial, difícilmente alcanzaremos una emulsión estable.
¿Qué es una sal?
Entendemos por sales los compuestos iónicos que forman cristales generalmente solubles en agua.
Pero vamos a hablar fundamentalmente de los carbonatos sódico y potásico y del cloruro sódico o sal común. Un poco menos de los silicatos. En realidad, una sal es el producto de mezclar un ácido con una base consiguiendo un resultado neutro o una base débil. Todos los jabones son sales.
Utilización de los carbonatos en los jabones
Los carbonatos son capaces de saponificar los ácidos grasos libres.
Así si tenemos ácido esteárico y lo mezclamos con una solución de carbonato sódico obtenemos estearato sódico, una sal que no es más que jabón. Sin embargo, los carbonatos no tienen la capacidad de saponificar una grasa ya que esta está esterificada como triglicérido. Para ello se caustifica el carbonato con cal viva. Es la forma en que se hacía antiguamente con las cenizas.
Además los carbonatos tienen la cualidad de volver más fluida la masa del jabón cuando se trabaja en caliente o se hace un refundido. Pero, si excede cierto nivel, la emulsión se descompone. Como efecto sobre el producto, los jabones que contienen carbonato son más duros y secan antes.
A partir de cierta cantidad de carbonato, el jabón adquiere cierta textura plástica y translucidez. Ablanda el agua, haciéndolos más espumosos y también tiene un efecto más desengrasante que puede resultar un poco más agresivo a la piel.
El cloruro de sodio en los jabones
El cloruro de sodio o sal común tiene los mismos efectos que los mencionados para los carbonatos para la elaboración de la masa del jabón pero con un efecto más exagerado, por lo que la cantidad a utilizar debe de ser muy inferior.
Al contrario que con los carbonatos, la sal reduce el factor espumante de los jabones.
Hay que tener en cuenta que un jabón con exceso de sales tiende a ser eflorescente, o sea que le salen los cristales de sal a la superficie, y potencia la cualidad higroscópica del jabón, o sea que atrae a la humedad del ambiente mojándose su superficie. La cualidad de producir la separación entre fases es la que permite que un jabón se pueda cortar.
Tengamos en cuenta que la concentración salina de la lejía es muy alta por las bases cáusticas y que esto hace que se pueda cortar (separar). Además se debe tener en cuenta que el agua del grifo puede portar sales (magnesio y calcio) lo cual aumenta la salinidad y posibilidad de separación.
En caso de que un jabón se corte, se puede remediar añadiendo agua destilada para disminuir la salinidad.
Los silicatos, se usan conjuntamente con los carbonatos e incluso con la sal común como elementos de carga. Es decir, añadiéndolos al jabón hacen que éste retenga mayor cantidad de agua, creando estructuras que dan la solidez que de otra manera no tendría y proporcionando más peso y volumen al producto. No obstante, estos jabones no suelen reunir las características cosméticas.
Conservación de los jabones
Los motivos por los cuales se estropean los jabones fundamentalmente son dos: el deterioro bacteriológico y la oxidación. Algunos de los consejos que se dan a continuación también valen para otros productos.
Importancia de los conservantes en los jabones
En primer lugar, la proliferación de bacterias, hongos y levaduras se produce en mayor medida donde hay agua y, si además, encuentran alimentos, se puede convertir en el espacio de cultivo idóneo.
Generalmente prefieren medios neutros o ligeramente ácidos por lo que los jabones no son muy susceptibles de dicha proliferación, ya que el medio es alcalino en presencia de agua y al secarse desaparece ésta.
El problema puede surgir al añadir algunos aditivos, que hidratados pueden alimentar a ciertos microorganismos. Es el caso de vegetales en polvo, frutos, harinas e incluso flores.
A veces es suficiente con la propia alcalinidad del jabón para preservar estos ingredientes pero si están en trozos grandes la conservación es algo deficiente.
Para este caso es conveniente utilizar algún conservante, y en productos como las cremas o jabones en pasta, con mucha más razón, ya que no se deshidratarán. Los benzoatos, se recomienda en algunos sitios, no se debe usar para jabones ya que funciona sobre todo en medios ácidos; los compuestos de amonio cuaternario son más activos para pH alcalino.
Esto quiere decir que cuando los fabricantes industriales meten sus conservantes químicos a los cosméticos, no lo hacen para fastidiarnos, lo hacen porque son necesarios.
Las alternativas naturales para ellos, como el extracto de semilla de pomelo o el extracto de romero, no son tan eficaces y algo costosos.
Los antioxidantes en los jabones
Los aceites están constituidos por esteres de ácidos grasos, algunos ácidos grasos libres y muy poco material insaponificable.
Los ácidos grasos tienen mayor o menor grado de saturación, siendo los más saturados los más estables y por tanto duraderos.
Los insaturados en cambio, son más susceptibles de reaccionar con otros compuestos, y de ellos, los oxidantes son los más activos. Esto significa que cuanto más insaturado sea un aceite mayor probabilidad de oxidación tiene.
A esta degradación de las grasas le solemos llamar enranciamiento, ya que produce compuestos volátiles de olor rancio.
Para evitar esta oxidación se utilizan los antioxidantes que retrasan la oxidación de los aceites. Esta oxidación, téngase en cuenta, solo requiere del aire, y a mayor temperatura y mayor grado de humedad, el efecto es más rápido.
Por eso todos los aceites se conservan mejor refrigerados y bien tapados. Antioxidantes hay muchos y actúan de diferente manera, pero para los aceites en cosmética, se usa mucho los tocoferoles o vitamina E.
Estos se asocian a las insaturaciones impidiendo que lo hagan otros compuestos. Su efecto puede ser potenciado por la vitamina C (ácido ascórbico) que también es un antioxidante al igual que los carotenoides.
En la figura 1.3 podemos observar el esquema de una molécula de vitamina C o ácido ascórbico.
La vitamina E se encuentra de manera natural y puede ser absorbida por los humanos mediante la alimentación. Son alimentos ricos en vitamina E muchos aceites (el de girasol, nueces, sésamo, soja, palma o de oliva) o frutos secos (las nueces, las almendras o las avellanas). En los humanos es muy raro tener carencia de esta vitamina; normalmente sólo pasa cuando tenemos problemas para asimilar las grasas.
Es más frecuente en alimentos vegetales, pero también se encuentra en alimentos animales como la yema de huevo.
La vitamina E es uno de los antioxidantes más efectivos, y como tal se incluye en multitud de cosméticos. Desde el punto de vista químico, dentro del grupo de la vitamina E se engloban varias estructuras:
- Tocoferoles: a (alfa), β (beta), δ (delta) y γ (gamma)
- Tocotrienoles: a (alfa), β (beta), δ (delta) y γ (gamma)
Las utilidades de la vitamina E en el día a día son muchas: influye en el corazón, en el colesterol, en el sistema neurológico, en la vista, en nuestros genes.
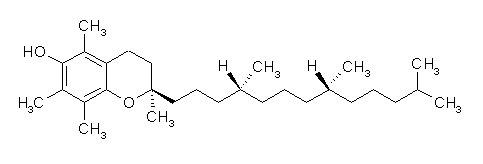
Para la cosmética, la vitamina E le aporta propiedades fundamentales ya que tiene un hidrógeno que puede ceder sin inestabilizarse un electrón, de manera que puede ceder a los radicales libres una partícula para que dejen de serlo… así que sirven para reducir el estrés oxidativo y, por tanto, el envejecimiento.
Esta capacidad antioxidante se ve reforzada por la vitamina C que corta la formación encadenada de los radicales libres en la vitamina E (junto a los ascorbatos y el ubiquinol) cuando la vitamina E cede partículas a otros radicales libres.LA VITAMINA E, TOCOFEROL Y TOCOTRIENO. Fuente: Reabeautys.
De los Tocoferoles se ha hablado de su inestabilidad en las fórmulas, y a menudo en las fórmulas se añaden derivados sintéticos que supuestamente aguantarán mejor en ellas.
- Alfa-tocoferol,α-tocoferol, $C_{29}H_{50}O_2$, puede tener también apariencia de polvo blanco, así que, no sólo es líquido. En alimentación se suele usar una versión sintética, que se numera como E-306. Es la forma con la que más estudios se han hecho, y por tanto la más conocida; y no sólo la más potente como vitamina.
- Beta-tocoferol, β-tocoferol, $C_{28}H_{48}O_2$
- Gama-tocoferol, gamma tocoferol, γ-tocoferol, $C_{28}H_{48}O_2$. Apariencia: líquido viscoso amarillo pálido. Su forma sintética usada en alimentación es el E308.
- Delta-tocoferol, δ-tocoferol, $C_{27}H_{46}O_2$ y de nuevo aparece como un líquido viscoso y de color amarillo pálido. El delta-tocoferol sintético usado en alimentación suele numerarse en la lista de ingredientes como E-309.
La vitamina C es un antioxidante natural que tiene propiedades antioxidantes, anti radicales libres, efectos antiinflamatorios y un papel importante en la formación de colágeno. Aporta efectos anti envejecimiento de la piel mejorando su luminosidad y textura. Esta vitamina, ácido ascórbico, es más efectivo que el ácido kójico y la arbutina (glucósido de hidroquinona), ya que no solo puede inhibir la bioactividad de la tirosinasa sino que también puede revertir la hiperpigmentación al reducir directamente la melanina acumulada.
Sin embargo, el ácido ascórbico es muy inestable, se oxida muy fácilmente por el contacto con el aire, el calor y por la luz. Además requieren un pH muy ácido, lo que convierte a estas formulaciónes en cosméticos muy vulnerables a la oxidación e irritantes.
Aparte de los anteriores antioxidantes, se cuentan los carotenoides.
Es importante anotar que el pH también influye en el enranciamiento y es una de las razones por la cual el ácido graso saponificado se estabiliza y se conserva mejor. Es el aceite usado como sobreengrasado el que queda vulnerable ante la oxidación.
Del mismo modo influye también la luz que acelera las reacciones y descompone algunas sustancias. O sea, que si ponemos por ejemplo el puré de un aguacate en un jabón y sólo añadimos un antioxidante conseguiremos que la grasa del aguacate no se enrancie (o tarde más) pero el jabón se puede estropear.
En general, una vez secado el jabón, que esté envuelto de modo que quede aislado del aire prolongará su durabilidad, más si está en un lugar seco, fresco y oscuro.

Química del jabón
Jabón:su fórmula química y conceptos básicos
Un jabón pudiera parecer un producto muy simple, pero su formulación implica lograr el equilibrio entre muchas de sus características, la dureza, la formación de espuma, la limpieza, el aroma, la duración, la cremosidad, entre varias otras, pues debe tenerse en cuenta que el jabón básicamente es una sal sódica o potásica resultante de la reacción química entre un álcali (hidróxido de sodio o de potasio) y un lípido; esta reacción se denomina saponificación. El lípido puede ser de origen vegetal (como el aceite de coco) o animal (como la manteca de cerdo). El jabón es soluble en agua. Por sus propiedades detersivas se utiliza para el lavado de ropa, corporal, jabones bastante delicados exclusivos para la piel del bebé, entre otros.

Introducción
Los ácidos grasos que se utilizan como materia prima del jabón son los siguientes pueden ser aceites vegetales: coco, soja, maíz, oliva, lino, algodón. Aceites animales: de pescado, grasas animales los se combinan con cremas, perfumes y colorantes para darles vistosidad.
Tradicionalmente, es un material sólido. En realidad la forma sólida es el compuesto seco, sin el agua que se emplea en la reacción mediante la cual se obtiene el jabón. La forma líquida es el jabón disuelto en agua. En este caso, su consistencia puede presentar distintas viscosidades.
Fórmula química y conceptos básicos
La imagen 2.1 representa una molécula de jabón. En rojo, la cabeza, con carga, es afín al agua porque son de polaridad similar. La cadena azul, denominada lipofílica, es afín a las grasas y repele al agua.
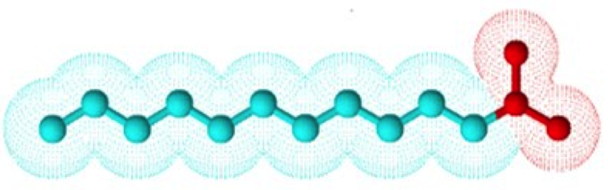
A causa de esta estructura, el jabón posee una doble afinidad hacia la polaridad de otras moléculas y puede orientarse según el medio donde se encuentre.
En el agua, el jabón forma entre 100 y 200 micelas; es decir, asociaciones o conglomerados de moléculas que orientan sus cabezas con carga hacia la superficie del agregado molecular, mientras que las cadenas alifáticas quedan hacia dentro. La micela es una partícula energéticamente estable, ya que los grupos con carga están unidos mediante enlaces de hidrógeno de baja energía con las moléculas del agua circundante, mientras que los grupos afines a las grasas se orientan hacia el interior de la micela e interactúan con otros grupos de características similares.
Los jabones limpian debido a las afinidades diferentes de los extremos de sus moléculas. La suciedad grasa no se elimina fácilmente sólo con agua, que la repele por ser insoluble en ella.
Sin embargo, el jabón posee una cadena larga alifática o hidrocarbonada sin carga que interactúa con la grasa, disolviéndola, mientras que la región con carga se orienta hacia el exterior, formando gotas.
Una vez que la superficie de la gota grasa está cubierta por muchas moléculas de jabón, se forma una micela con una pequeña gota de grasa en el interior. Esta gota de grasa se dispersa fácilmente en el agua, ya que está cubierta por las cabezas con carga o aniones carboxilato del jabón, como se observa en la Figura 2.2.
La mezcla que resulta de dos fases insolubles (agua y grasa), con una fase dispersada en la otra en forma de pequeñas gotas, se denomina emulsión. Por lo tanto, se dice que la grasa ha sido emulsionada por la solución jabonosa. De esta manera, en el proceso de lavado con un jabón, la grasa se elimina con el agua del lavado.
Una micela es una estructura de agrupación molecular que une un conjunto de partículas de una forma peculiar. A través de la formación de estas estructuras es el mecanismo por el cual algunos jabones solubilizan las grasas. Pero, cómo lo consiguen? Porque sabemos que las grasas (aceites) y el agua, se repelen entre sí. Sencillo. Las micelas se conforman en estructuras circulares polarizadas, donde su porción externa atrae a la parte grasa (lipófila) mientras que su porción interna atrae al agua (hidrófila).
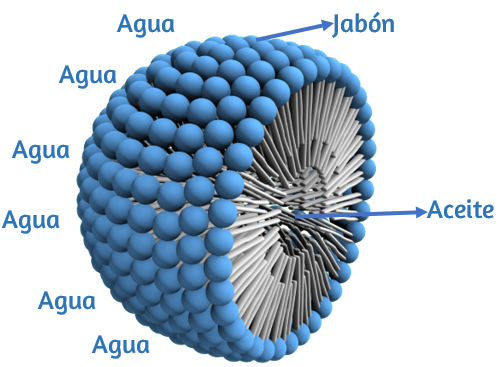
Principios para la elaboración del jabón
Química del jabón
Como ya se ha dicho, los jabones son sustancias que ayudan a limpiar la suciedad, el aceite y la suciedad de grasa de superficies, metales, la piel o el cabello.
Se restringe el término jabones, frente al término detergentes, a las sales sódicas o potásicas de ácidos carboxílicos de cadena larga.
Un ácido carboxílico se define por la presencia de un grupo caroxílico, -CO2H. Si el anión del grupo carboxílico es equilibrado con un catión de sodio o potasio y , por otro lado, une mediante enlaces covalentes a una cadena larga de grupos -CH2- y termina en el grupo CH3-, entonces tenemos una molécula de jabón. Podemos generalizar la estructura molecular del jabón de esta manera:
$ CH_3 \space - \space \big(CH_2\big)_n \space - \space CO_2 - \space Na^{2+}$
El componente $CH_3-(CH_2)_n$ se parece mucho a las cadenas largas de las moléculas de los hidrocarburos como la gasolina o el aceite mineral, provenientes del petróleo. Esta parte de las moléculas del jabón tienden a disolverse fácilmente en hidrocarburos o materiales parecidos, pero no en agua.
Sin embargo, el otro extremo de la molécula de jabón es iónico. Como el cloruro de sodio (sal común) y otras sustancias iónicas, este extremo iónico tiende a disolverse en agua, y no en hidrocarburos.
Como resultado tenemos una molécula con dos tendencias contradictorias en cada extremo. Una estructura hidrofílica que es atraída por el agua y rehuye los hidrocarburos y las sustancias aceitosas o grasosas. Y una estructura hidrofóbica que rehuye el agua pero se mezcla fácilmente con las sustancias aceitosas o con grasa.
Lo anterior, porque los jabones son sales sódicas o potásicas de los ácidos grasos, solubles en agua. Se fabrican a partir de grasas o aceites (que son mezclas de triacilgliceroles), o lo que es lo mismo, acilgliceroles con tres moléculas de ácido graso, en general de cadena
larga, que pueden ser iguales o diferentes; se habla de triacilgliceroles simples cuando hay el mismo ácido graso en las tres posiciones del glicerol, pero la mayoría son triacilgliceroles mixtos, con, al menos, dos ácidos grasos diferentes. Las propiedades de los triacilgliceroles 10 van a depender del tipo de ácidos grasos que contengan), como se muestra en la figura 2.4, estos mediante el tratamiento con un álcali o base fuerte (hidróxido de sodio, que dará jabones duros, o hidróxido potásico, que dará jabones blandos más adecuados para jabones líquidos y cremas de afeitar). Por sus características, los jabones son surfactantes aniónicos.
Procesos en la fabricación del jabón
Saponificación
Es el proceso de fabricación de los jabones a partir de triacilgliceroles (triglicéridos),es necesario tener presente que los triacilgliceroles son moléculas bastante inertes químicamente, pero los ácidos grasos se separan del glicerol mediante hidrólisis alcalina fuerte, saponificación.
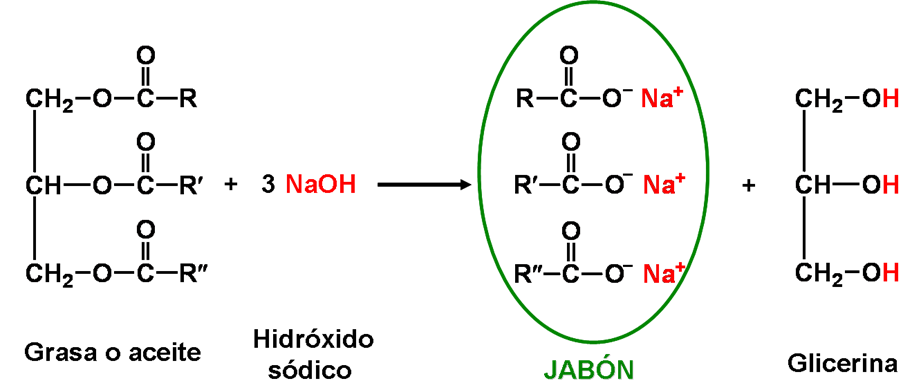
La segunda posibilidad para la fabricación de jabones es la neutralización de ácidos grasos con álcali. Para ello, primero es necesario hidrolizar las grasas y aceites empleando alta presión que separan los ácidos grasos de la glicerina o glicerol. Después se purifican los ácidos grasos por destilación y ya se pueden neutralizar con el álcali para dar el jabón.
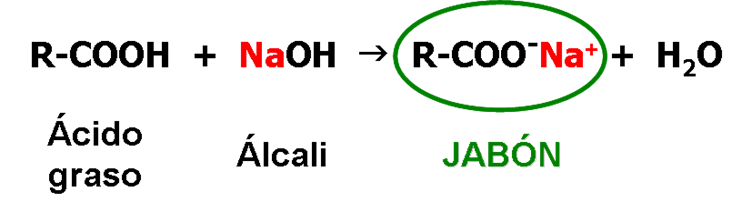
De la figura 2.4, puede concluirse que al unir una grasa, que está constituida por triglicéridos, a una solución alcalina, constituida por agua y sosa cáustica, los triglicéridos se separan en una molécula de glicerina y tres cadenas de ácidos grasos. Estos se unen rápidamente a una molécula de sodio y constituyen el jabón, dejando en su interior la glicerina restante.
Muy importante, tener presente que la saponificación es una reacción exotérmica lo que significa que produce calor. Cuanta más cantidad de jabón hay, más caliente se pone, sobre todo en el centro. Este calentamiento puede producir la gelificación, siendo ésta el estado que alcanza el jabón una vez enmoldado si llega a tener la suficiente temperatura, saponificando completamente. Se puede evitar el paso por el estado de gel no dejando que la masa alcance la temperatura necesaria. Para ello se puede partir de ingredientes muy fríos y moldes poco aislantes o incluso dejando el jabón solidificar en la nevera.
Salado
Consiste en el agregado de una solución concentrada de sal común (cloruro de sodio, NaCl) para separar el jabón de la glicerina formada y del exceso de hidróxido de sodio. Como el Jabón es insoluble en agua salada, se acumula en forma de grumos y sube a la superficie por su menor densidad.
Después de varias horas, se extrae por la parte inferior la mezcla de glicerol y agua salada.
Cocción
Al jabón formado en la caldera se le agregan nuevas cantidades de Na(OH) para lograr una saponificación completa, y se calienta. Al enfriarse, se separan nuevamente dos capas: la superior, de jabón, y la inferior, de lejía. Al jabón se le agrega agua y se cuece nuevamente; de esta manera se eliminan los restos de sal, glicerina y lejía.
Amasado
Tiene por objeto lograr una textura homogénea, sin gránulos. Durante esta etapa se le incorporan a la pasta sustancias tales como perfumes, colorantes y resinas, para favorecer la formación de espuma persistente.
Modelado
El jabón fundido se vuelca en moldes de madera donde, por enfriamiento lento, toma la forma de panes o pastillas; mediante equipos desecadores, se disminuye el contenido de humedad hasta el 20%.
Prácticamente todos los jabones contienen de 10 a 30% de agua. Si el Jabón fuera anhidro sería muy difícil de disolver. Casi todos los Jabones contienen perfume, aun cuando no se manifieste, cuya función será eliminar el olor a jabón puro.
Los jabones de tocador se fabrican a partir de materiales selectos y generalmente contienen 10 a 15% de humedad, poseen muy pocos materiales adicionales con excepción de perfume y una pequeña fracción de dióxido de titanio como agente blanqueador.
Calidad de un jabón
Para determinar si el jabón es de calidad, se deben de realizar pruebas analíticas, tanto durante el proceso de fabricación como en el producto terminado. Entre las pruebas tenemos: Materia insoluble en alcohol, alcalinidad libre, humedad, ácidos grasos libres y acidez libre.
La materia insoluble en alcohol se basa en la determinación gravimétrica de la materia insoluble en etanol, la materia insoluble en alcohol contendrá la mayoría de las sales alcalinas, tales como carbonatos, boratos, silicatos, fosfatos y sulfatos, lo mismo que almidón; se puede usar para determinación aproximada de esos constituyentes. Esas sales no son completamente insolubles en alcohol, y para determinaciones exactas deberán usarse proporciones del jabón.
La alcalinidad libre, los jabones presentan alcalinidad libre que permite que las grasas y/o aceites que no reaccionan, no se enrancien con el tiempo, es por eso que se les deja cierta alcalinidad libre o soda cáustica (0.03 a 0.05%). La alcalinidad libre en los jabones reacciona con la grasa que tenemos en la piel,
causando el efecto de sequedad y pudiendo generar irritación dependiendo de la sensibilidad de la piel; en el caso de la piel sensible puede provocar alergias al perfume, o al colorante, al antibacterial y otros aditivos que se incorporan al jabón.
La humedad está presente en la mayoría de los productos naturales y su determinación es fundamental en características decisivas para la producción, el almacenamiento y comercio. Los productos cosméticos son a menudo emulsiones en base acuosa.
Por lo tanto, el contenido de agua es esencial, ya que demasiada agua conduce al crecimiento bacteriológico o una experiencia táctil inaceptable para los consumidores. Demasiada poca agua puede afectar la homogeneidad del producto cosmético y es indeseable desde una perspectiva de costo. Por consiguiente, las determinaciones del contenido de agua son comunes en la industria cosmética.Clasificación de los Jabones
Existe una amplia gama de jabonesClasificación de los jabones Fuente: Portal de arquitectura Arqhys.com, por lo que tenemos que escoger el que más nos convenga según la necesidad:
Jabones duros
Son los elaborados con grasas y aceites con alto contenido de ácidos saturados, que saponifican con hidróxido de sodio. Son empleados para lavar ropa y objetos.
Jabones blandos
Tipo de jabón elaborado en base a aceite de semilla de algodón, a aceite de lino y aceite de pescado, los cuales llegan a saponificar con hidróxido de potasio. Entre ellos se encentra los jabones líquidos.
Jabones humectantes
Son jabones especiales para piel seca que está muy maltratada, los cuales la hidratan y la acondiciona, gracias a los materiales que le compone, donde en su mayoría contienen: grasas, aceites vegetales o cremas.
Jabones comunes
Se trata de jabones espumosos y sólidos que son elaborados en base a potasio o sodio, y a sebo graso. Por sus componentes se puede emplear tanto para la piel como para el cabello.
Jabones dermatológicos
Son jabones especiales para el cuidado de la piel, los cuales ofrecen una limpieza mucho mayor y mas suave, ya que posee agentes sintéticos de limpieza con los cuales se logra cerrar perfectamente los poros de la piel.
Jabones naturales
Se trata de jabones aromáticos que contienen esencias frutales y florales, los cuales presentan propiedades propiedades relajantes debido a su rico aroma.
Jabones suaves
Es el tipo de jabón que se recomienda a personas con piel muy sensible, los cuales están compuestos por aguas termales y otros elementos especiales.
Jabones terapéuticos
Son los jabones que suelen indicar los médicos para tratar ciertas enfermedades cutáneas de sus pacientes, como es el caso de la micosis cutánea y de la psoriasis. Estos son perfectos para limpiar el rostro de una forma profunda.
Jabones líquidos
Como indica su nombre, son jabones no sólidos, que deben ser aplicados con una esponja para garantizar el correcto uso y el buen aprovechamiento del mismo. Estos se comercializan en envases de plásticos, que tienen un tapa dosificadora que permite que el líquido sea usado sin desperdiciarse.
Jabones de glicerina
Son jabones de gran uso para piel grasa, ya que logra controlar la cantidad de grasa, evitando así las espinillas o el efecto de brillo en el rostro.
Jabones de leche
Es un jabón elaborado con leche que por sus propiedades logra favorecer el rejuvenecimiento de la piel.
Jabón de avena
Jabón que contiene como principal elemento la avena, lo cual es perfecto para tratar cicatrices de herida y para suavizar la piel.
Jabón de concha nácar
Es el tipo de jabón que se suele utilizar para eliminar ciertas manchas de la piel.
Jabón de miel
Son jabones que logran mantener la piel humectada, además otorga firmeza y elasticidad.
Jabones en barra
Son jabones de bajo costo y de fácil utilización, que se comercializan de forma sólida, ahora bien, se recomienda mantenerlo en jaboneras que permitan que el agua se escurra, para que este se mantenga seco, de esta modo se evitará el escurrimiento y la producción de hongos y bacterias.
Jabones medicados
Se refiere a los jabones que están compuestos por ingredientes antisépticos y anti-bacterianos, los cuales son útiles para prevenir y disminuir infecciones en la piel, como es la seborrea, el acné, la caspa, etc.
Jabón azul
También llamado jabón de panela. Tipo de jabón empleado para tratar el acné, es muy barato y se suele comercializar en Venezuela.
Jabones infantiles
Son jabones suaves y neutros que se fabrican con variados colores y figuras con el objetivo de llamar el interés del niño, motivándolo así al baño diario.
Jabones neutros
Son jabones de gran recomendación para pieles infantiles y delicadas, ya que proveen una alta protección.
Jabones perfumados
Como indica su nombre, son jabones de baño que logran dejar un rico roma en la piel.
Jabón de marsella
Es un jabón que se suele elaborar en Francia, el cual se hace en base a aceites vegetales.
Jabones astringentes
Son jabones especiales que logran disminuir considerablemente el exceso de grasa y el brillo en la piel.
Jabón de afeitar
Es un jabón especial para afeitar que crea un cremosa y densa espuma que ayuda a que la navaja se deslice más fácil sobre la piel, evitando que esta corte o irrite.
Jabones exfoliantes
Se trata de jabones que poseen gránulos muy pequeños que logran eliminar las células muertas y la suciedad de la piel.
Jabón de ceniza
Es un jabónClasificación de los jabones Fuente: Jabón de ceniza. Tomado de Jabón de Ceniza. Mundo huerto, volviendo a la tierra. potásico de excelente calidad a partir de cenizas de madera, con lo que se le da valor a las cenizas que de otra forma seguramente acabaría en la basura.
La ceniza de madera es esa sustancia pálida, similar al polvo, que queda en el fondo de las estufas que se prenden con madera (la leña) o de cualquier fuego con combustible sólido y que se compone de óxidos metálicos y sales, entre otras cosas.
Pues bien, la ceniza tiene más usos, y uno de los más antiguos es la utilización como sustancia detergente y quitamanchas, es decir, como jabón.
En el caso de la ceniza, el álcali suele estar compuesto por varios hidróxidos y carbonatos de potasio, calcio, sodio, magnesio, etc. solubles en agua.
Por tanto, a diferencia del jabón de sosa, el de ceniza es mucho más rico en su composición y, para algunas aplicaciones, mucho más efectivo.
La lejía de ceniza
Se conoce con este nombre al lixiviado que resulta de saturar las cenizas de agua, de forma que el líquido que se desprende es la lejía.
Las cenizas se vierten en un recipiente agujereado por la base, luego se va añadiendo agua sobre ellas. Cuando ya no pueden absorber más, el líquido comenzará a caer por el orificio de la base.
Al pasar el agua a través de las cenizas, disuelve los compuestos químicos solubles, principalmente el carbonato de potasio, pues la ceniza de madera contiene carbonato de potasio ($K_2CO_3$).
Esta sal en agua da lugara a una solución fuertemente alcalina, ideal para elaborar jabón o para utilizar directamente como lejía.
Debido a que la sal predominante en la lejía de ceniza es el carbonato potásico, el jabón resultante será principalmente jabón potásico, aunque contendrá también otros compuestos.
Ete jabón tiene un olor muy característico si encuentras la versión sin perfume. Es blando, de color oscuro y tiene propiedades curativas para la piel. Su uso diario elimina escamas de codos, rodillas y pies, además, deja la piel muy suave y tersa.
No crea espuma porque no tiene glicerina y saponina, pero sus propiedades exfoliantes, astringentes y desengrasantes dejan la piel limpia y suave .
Usos del jabón de cenizas
- Para el cuidado de la piel del rostro
- Para el acné
- Para el cabello
- Para los piojos
Durante el día nuestra piel acumula la suciedad que se encuentra en el medio ambiente y células muertas, aunque laves tu rostro, siempre tendrás un pequeño porcentaje de esta mezcla sobre él, causando obstrucciones en los poros y puntos negros.
El jabón de tierra puede evitarlo, solo debes utilizarlo en la mañana y en la noche, masajeando suavemente y dejándolo actuar por cinco minutos. Luego debes enjuagarlo con agua fría.
Es perfecto para combatir brotes de acné. Solo debes lavar tu rostro tres veces al día y no utilizar cremas grasosas sobre tu cutis.
Tradicionalmente se ha utilizado este jabón para lavar el cabello, pues mantiene alejadas a las plagas, fortalece el folículo piloso y mantiene el cuero cabelludo libre de caspa y de grasa.
Esta plaga indeseable puede ser eliminada utilizando jabón de tierra durante un mes. Lava su cabello dos o tres veces al día y déjalo actuar por 10 minutos. Recuerda enjuagar con abundante agua.
- Humecta la piel
- Para barba y bigote perfectos
Este jabón humecta los pies, rodillas y codos, incluso la piel más áspera queda con la suavidad y tersura de la juventud.
Aplica sobre la barba húmeda y masajea suavemente para estimular la circulación y fortalecer el folículo piloso.
Hoy en día, a este jabón no se le añade grasa animal, sino aceites vegetales y esencias florales o frutales. Sin embargo, puedes encontrar autentico jabón de tierra confeccionado con la receta tradicional en tiendas dedicadas al esoterismo, tiendas botánicas y en la sección naturista de mercados artesanales.Disponible en Jabón de tierra.

Fabricando un jabón
Fabricando el jabón
La elaboración del jabón es quizá una de las reacciones químicas más antiguas que se conocen, posiblemente la segunda después de la fermentación del mosto para obtener vino. Como en la historia se ha descrito que desde tiempos ancestrales ya se usaba el jabón, quizá no tan científicamente elaborado como se lo conoce hoy, sin embargo sí en su estado más esencial, que es de agente limpiador a través de su reacción química al mezclarse con agua y existiendo la necesaria fricción entre sus elementos. En la actualidad se mantiene esa libertad en la elaboración de jabón, siendo desde la forma más simple, en la que cualquier persona puede elaborar su jabón con poco de conocimiento químico y claro de la forma industrial ya se destaca la expresión masiva en la que técnicamente el jabón es producido con un nivel exacto y calculable de componentes para su comercialización en masa.

Introducción
Al momento de fabricar un jabón el aspecto primordial es la seguridad en el manejo de los reactivos para evitar accidentes y quizá lo más importante a tener en cuenta es la peligrosidad de la sosa o soda cáustica (hidróxido de sodio), o de la potasa cáustica. Ambos reactivos son peligrosos y hay que mantenerlos fuera del alcance de los niños y de los animales.
Cuando estos reactivos se mezclan con el agua se produce una lejía que, al contacto con la piel, puede producir quemaduras químicas importantes y en los ojos ya ni te cuento.
Siguiendo las simples indicaciones que vienen a continuación, el riesgo es mínimo, pero aun así, no me hago responsable del mal uso que podáis dar a estas instrucciones.
- Hay que guardar el hidróxido de sodio (también llamado sosa cáustica o lejía) herméticamente cerrado, bien identificado y en un lugar alejado de los niños y las mascotas.
- Usar siempre: guantes, mascarilla y gafas protectoras. También hay que procurar llevar ropa que cubra el cuerpo, sin olvidarse de los pies y un delantal para evitar que una posible salpicadura estropee la ropa ya que la sosa es muy corrosiva.
- En caso de contacto con la lejía o con la masa del jabón sin saponificar hay que lavar con abundante agua varias veces. En caso de contacto con los ojos hay que lavar abundantemente durante unos minutos y acudir inmediatamente al médico.
- La manipulación de lejías cáusticas no es un juego de niños. En caso de querer mostrarles como se hace el jabón, siempre debe de ser con la supervisión de un adulto responsable
- Cuando se trabaja con productos químicos hay que tener muy en cuenta el recipiente donde se almacenan. Cada recipiente tiene su indicación y cada producto sus requisitos. Hay que etiquetarlo todo muy bien y nunca mezclarlos con otros productos que no sean para los jabones. Mantenerlo todo siempre lejos del alcance de los niños y las mascotas.
Muy importante
Hay que añadir la sosa al agua. Primero el agua, después la sosa y disolver bien. La mezcla comenzará a echar vapor, hay que mantener la cara alejada de ellos, aun llevando la mascarilla. Estos vapores duran poco tiempo pero la mezcla sigue muy caliente por lo tanto es muy importante hacer este proceso en un lugar bien ventilado.
- Cuidado y precaución con los aceites esenciales
Otro factor a tener en cuenta son los aceites esenciales. Algunos de ellos son bastante corrosivos. No tan peligrosos como los álcalis pero sí lo suficiente como para tener que evitar el contacto directo con la piel y, si se produjese ese contacto, hay que lavar también abundantemente. Otro peligro que entrañan es el derrame. Ahí más que nada es el residuo oloroso que en algunos casos puede durar muchos días y, aun siendo de un buen olor, ser bastante desagradable.
Todas estas advertencias son para mostrar el peligro real que entraña la lejía cáustica pero con un uso racional, cuidadoso y ordenado no tiene porqué entrañar verdadero riesgo.
- Cuidados especiales con otros reactivos
También para casos especiales podemos usar disolventes como el alcohol o el propilenglicol u otros ingredientes en general, en cuyo caso hay que tener siempre en cuenta toda la información de seguridad que aportan tanto sobre su almacenaje como de su manipulación.
- Nunca dejar las mezclas fuera del alcance de tu supervisión
- Lavar todos los utensilios utilizados con los guantes puestos
- No utilizar el jabón hasta pasadas 4 semanas por lo menos. Este es el tiempo, mas o menos, que tarda en completarse el proceso de saponificación. Es la peor parte, te devora la impaciencia por probarlo
Primeros pasos para fabricar un jabón
Para realizar los primeros experimentos es recomendable iniciar por reciclar el aceite usado, y si no, utiliza o aceite de oliva o manteca de cerdo. Ya se tendrá tiempo de usar materiales más sofisticados cuando se adquiera cierta práctica.
Es muy importante que la sosa, NaOH, sea lo más pura posible preferiblemente al 99 %. La buena para hacer jabón es esta. Si el agua, además, es destilada o desmineralizada es mucho más difícil que se corte el jabón.
Es necesario emplear una báscula (Cuanto más precisa mejor, las digitales suelen serlo) para pesar los reactivos. No uses el cálculo.
Para familiarizarse con el proceso iniciemos con el siguiente jabón, que sirve para limpiar suelos, platos o ropa:
- 1 kg de aceite usado ( un kilo)
- 700 g de agua
- 145 g de sosa cáustica
En el siguiente vídeo se presenta la preparación de un jabón a partir de aceite usado de cocina. En este caso, de oliva. Este tipo de jabones sirve para quitar las manchas, limpiar los suelos o lavado de la vajilla. No es un jabón cosmético por lo que no se debe de usar en la piel.
Con esta fórmula, para hacer la lejía, los ingredientes serán aproximadamente: 40g agua por cada 100g de aceite y 15g sosa por cada 100g de aceite (ya filtrado).
Cada año son miles de litros de aceite residual de cocina los que pasan a contaminar nuestros ríos y campos por ser un producto poco biodegradable. O en el mejor de los casos suponen un gran consumo energético en las plantas de depuración.
Con unos pasos sencillos es muy fácil convertir ese residuo en un producto no solamente útil y económico sino mucho más fácil de degradar. Uno de los factores de deterioro del aceite de cocina es la liberación por parte de ciertos ácidos grasos de sustancias que producen mal olor.
Al saponificar, algunas de estas sustancias pasan a convertirse en jabón reduciendo significativamente el mal olor e incluso el color..
Por otra parte, dependiendo del método, se puede limpiar, dejando sus impurezas en un exceso de líquido por debajo del jabón. También quedarían disueltos en ese líquido, del que nos desharemos, los mucílagos responsables del mal olor, el exceso de sosa y la glicerina.
En el siguiente vídeo se presenta la preparación de un jabón a partir de aceite usado de cocina. En este caso, de oliva.
Este tipo de jabones sirve para quitar las manchas, limpiar los suelos o lavado de la vajilla. No es un jabón cosmético por lo que no se debe de usar en la piel.
Fabricando jabón con aceite reciclado Fuente del video: Medrulandia. Imagen de silviarita en Pixabay
Utilidades del jabón con aceite usado
Más que para un uso cosmético, se trata de un jabón para lavar los cacharros, los pisos e incluso la ropa, por eso se puede permitir un ligero exceso de sosa para garantizar la completa saponificación de las grasas.
Con eso también se mata los malos olores, se consigue que el jabón terminado flote sobre un poco de líquido que contendrá los excesos de sal y sosa.
Cantidades recomendables para un jabón con aceites reciclados
Se usa el valor de saponificación 140 para el aceite de oliva. Si en él se han frito grasas animales, algunas de ellas se quedan en el aceite, por lo que el valor se puede subir hasta 150. Esto significa que por cada kilo de aceite de oliva vamos a añadir de 140 a 150 gramos de sosa para convertirlo en jabón.
Podemos añadir también sal, no más de un 1% del peso total, diluida en agua para conseguir un jabón un poco más blanco, más duro y más límpio.
Así para realizar el jabón necesitamos 1 kg de aceite usado, entre 500 y 800gr de agua (sí, he dicho gramos, todos los ingredientes hay que medirlos en gramos), 12 g de sal y 145 g de sosa cáustica.
La oscilación de la cantidad de agua va en gustos, preferiblemente usar 500 y se puede usar mucho menos, pero se hacen jabones estupendos con cantidades mayores de 800 también.
Reactivos para obtener un buen jabón
El secreto para conseguir un buen producto es partir de los mejores ingredientes posibles. Del mismo modo, para conseguir productos naturales hay que partir de materias primas lo más naturales posibles.
- EL AGUA Y EL HRÓXIDO DE SODIO O POTASIO, (la sosa cáustica)
Lo más habitual, es elaborar jabones sólidos con sosa cáustica. Tambíen se pueden elaborar con potasa cáustica por lo que, aunque en adelante diga sosa, se puede aplicar a ambas. Además hay que tener muy claro que sosa no es lo mismo que sosa cáustica y lo mismo pasa con la potasa. Casi siempre que hablemos de sosa estaremos hablando de la sosa cáustica (NaOH).
Sosa cáustica y agua constituyen la lejía y hay que decir de ellos pocas cosas pero muy importantes:
La primera, por ser la más importante, es que siempre se sigan las normas de seguridad para trabajar con sosa. No está de más recordar que es un producto peligroso si no se toman las debidas precauciones.
- LA PUREZA DE LOS REACTIVOS DETERMINA LA CALIDAD FINAL DEL JABÓN)
El agua es conveniente que sea lo más blanda posible, es decir, que tenga la mínima cantidad de sales disueltas. No es imprescindible pero es recomendable que se use agua destilada o desmineralizada. Si no, agua de lluvia muy bien filtrada. Si no, agua mineral (de mineralización débil) y por último, del grifo.
La razón fundamental es que para diluir otra sustancia cuanto más pura sea el agua, mejor.
La sosa cáustica debe de ser también lo más pura posible. En los frascos de envase suele poner el grado de pureza. Es frecuente encontrar NaOH (sosa cáustica) al 99%. También es posible encontrarla al 50% y esta, por supuesto, es mucho menos recomendable ya que hay que compensar esa diferencia añadiendo más cantidad.
Si por ejemplo tenemos una sosa de la que sabemos que es del 90%, tendremos que añadir la diferencia a nuestra fórmula, o sea, poner un 10% más de sosa de la que indica la fórmula.
Los aceites y su uso en los jabones
- ACEITES VEGETALES:
Se pueden hacer perfectamente jabones de gran calidad exclusivamente con aceites vegetales.
Tipos según su forma de extracción
Se debe intentar que se trate siempre de aceites de primera presión en frío que son los que, por no tener más proceso que el mecánico, mantienen más sus propiedades naturales originales.
Esto significa que los frutos se exprimen por medios mecánicos, sin aplicación de calor ni disolventes, lo que hace que conserven sus vitaminas e insaponificables.
También nos encontraremos con aceites refinados a los que se les ha suprimido total o parcialmente su olor y/o color, son perfectamente válidos para nuestros jabones.
Tipos según su composición
Los aceites están compuestos básicamente de diglicéridos y triglicéridos de ácidos grasos. Cada aceite tiene unas propiedades diferentes en función de su composición y podemos combinarlos para obtener lo mejor de cada uno de ellos. Se suele hacer una distinción genérica entre aceites duros y aceites blandos.
Los primeros, los aceites duros, son aquellos en los que predominan los ácidos grasos saturados y suelen permanecer en estado sólido a temperatura ambiente (20ºC). Al calentarlos se derriten y se ponen en estado líquido. La mayoría de las mantecas se consideran aceites duros.
Los aceites blandos tienen predominio de ácidos grasos insaturados y se mantienen en estado líquido a temperatura ambiente. Además, los aceites blandos suelen ser más vulnerables al enranciamiento,que es la capacidad que tienen los aceites de reaccionar con el oxígeno y otros elementos y que producen su degradación y mal olor. Por eso es recomendable tener presente su fecha de caducidad.
Algunos aceites vegetales y su uso en los jabones
Uno de los mejores aceites para jabonear, es el aceite de oliva. Es un aceite a priori blando, ya que no se congela a bajas temperaturas pero produce un jabón bastante duro. Lo cual significa que no tiene por qué estar relacionado lo uno con lo otro. No obstante, al mojarse, es un jabón lamioso, sobre todo si tiene un sobreengrasado alto, que tiende a gastarse pronto. Además no produce demasiada espuma pero es un jabón suave que deja la piel mejor que ningún otro. Se suele usar de un 50 a un 100% (jabón de Castilla) del porcentaje de aceites en la fórmula.
El aceite de coco es un reactivo casi imprescindible para la jabonería. Su principal particularidad es la cantidad de espuma que produce y su enorme limpieza. Tanto es así que, un jabón sólo de coco, puede resultar demasiado limpiador y producir sequedad en la piel. Proporciona además bastante solubilidad y un rápido secado del jabón lo cual lo hace un buen complemento para el aceite de oliva. Se suele usar de un 10 a un 30% como máximo. Se usan jabones con más porcentaje de coco para aguas muy duras incluso saladas.
El aceite de ricino, para este aceite hay que asegurarse que se trata de primera presión en frío y que es de grado cosmético. El de ricino es un aceite muy espeso. Proporciona acondicionamiento al jabón. Viene muy bien para hacer champú y jabones para el cuidado de la piel y el cabello pero, por su extrema solubilidad, no conviene usarlo en exceso. Produce un jabón muy duro pero al contacto con el agua se deshace completamente. Es un aceite que acelera bastante la traza. Se suele usar de un 5 a un 10% como máximo del total de los aceites.
La manteca de cacao es un aceite que, por ser más costoso, se usa en menor cantidad. Proporciona suavidad, emoliencia, dureza y cremosidad en la espuma. Además, aunque también la hay desodorizada, proporciona muy buen aroma a chocolate. Es muy duro y tiene un punto de fusión bastante alto. Se usa de un 5 a un 15% normalmente.
El aceite de palma se usa sobretodo por su característica de dar cuerpo al jabón, haciéndolo más duro y con un tacto más untuoso. Es un aceite duro, relativamente barato y produce una espuma muy cremosa. Se suele usar de un 10 a un 30%. Tiene, no obstante, muy mala prensa por los métodos de producción aunque existen también con certificados de sostenibilidad.
El aceite de palmiste o hueso de palma, procedente del hueso de la palma, tiene características casi idénticas al de coco pero resulta un poco más suave y se puede usar en mayor cantidad. Procede del hueso del dátil de la palma y por tanto tiene su misma mala prensa. Como en el de coco, sus cualidades proceden de que los componen ácidos grasos de cadenas muy cortas. Ésto se puede traducir en que en el mismo peso de aceite hay más moléculas y eso, al combinarlos con los álcalis, se traduce en más moléculas de jabón.
El aceite de maíz es un aceite barato que produce burbujas y acondicionado de la piel pero del que no conviene abusar pues tiene tendencia al enranciamiento. Se puede alargar su tiempo de vida añadiendo vitamina E pero, en ese caso, no sé si resulta rentable su utilización. Se puede usar de un 5 a un 15%.
Del mismo modo, el aceite de girasolno conviene para la elaboración de jabones por su facilidad de enranciamiento. En todo caso los jabonbes realizados con la modalidad de alto-oleico pueden soportar un poco más.
Cálculo de la formulación de un jabón
Lo más bonito de la creación de jabones es la subjetividad que conlleva. Cada uno los hace a su antojo y a la medida de sus necesidades. Así puede apetecernos hacer un jabón más limpiador, más suave, más espumoso, más duro o blando...
Lo de hacerla a mano la formulación es muy importante, para asi saber de dónde salen sus cálculos y los conceptos que la fundamentan. Más adelante se presenta la calculadora para la formulación de jabón.
Lo que se ha de tener en cuenta para hacer una formulación
No hay una norma. Sólo unas indicaciones a tener en cuenta. Hay aceites que se estropean antes que otros. Se denomina enranciamiento al deterioro de los aceites, y los más sensibles son aquellos ricos en ácidos grasos insaturados.
Se debe a que esas insaturaciones se degradan convirtiéndose en compuestos que generan mal olor.
Para evitarlo se pueden utilizar agentes antioxidantes y el más común es la vitamina E acetato. También se puede utilizar aceite de semilla que es más bien un conservante.
Otros aceites, como el de girasol o el de germen de trigo por ejemplo, son muy ricos también en esta vitamina pero la cantidad que contienen no suele ser suficiente para prolongar por mucho tiempo la vida de ese aceite al contacto con el aire.
Tipos de aceites según su composición
Los aceites saturados son mucho más estables y por tanto duraderos pero no tienen la suavidad que aportan los otros. Podemos diferenciar dos grandes grupos:
- Los aceites duros
Se denominan así los aceites constituidos fundamentalmente por triglicéridos de ácidos grasos saturados, que vienen a ser el de coco, palmiste, karité, cacao, palma, sebo y manteca.
- Los aceites blandos
Son aquellos cuyo contenido son los triglicéridos de ácidos grasos insaturados, entre los que están el de oliva, ricino, aguacate, maíz, germen de trigo...
Dentro de este grupo están los aceites secantes, con alto contenido de los ácidos grasos insaturados linoleico y linolénico, que suelen ser los más emolientes y los más fácilmente enranciables. Son ejemplos de estos el de rosa mosqueta, argán, cáñamo y menos apreciado el de girasol.
A simple vista y en un clima templado se puede decir que son blandos los que se presentan en forma líquida y duros los que se presentan en forma sólida o como manteca. Esto es relativo por que por ejemplo el coco, hasta 25ºC, permanece sólido y a más temperatura es un aceite líquido.
Indicadores a la hora de hacer un jabón
Primero hay que iniciar por la selección de los aceites. Se suelen proveer con análisis que contienen dos indicadores que interesan fundamentalmente para realizar la receta: El índice de saponificación (SAP) generalmente indica la cantidad de hidróxido de potasio(KOH) necesario para saponificar un gramo de ese aceite. Así, si por ejemplo el del coco es 0.258, hacen falta 258 gramos de KOH para saponificar un kilo de aceite de coco.
Como normalmente solemos usar soda cáustica (NaOH) y no potasa cáustica, podemos convertir ese valor en su equivalente dividiéndolo por 1,4025. Es decir la equivalencia entre los álcalis más comunes es de que 1 g de potasa equivale a 1,4025 gramos de sosa.
El índice de yodo (IY) expresa la cantidad de yodo que absorbe un compuesto que va en función de la insaturación de éste. Esto significa que cuanto más alto sea este índice más posibilidades tiene el aceite de estropearse. Por lo tanto no es conveniente abusar de aceites que tengan un IY muy alto.
Se considera que un valor por encima de 70 puede resultar propenso al enranciamiento. Existe un indicador que se usa frecuentemente para elaborar una receta que se denomina valor INS. Este se calcula restando el valor SAP al IY. Si el aceite de coco tiene un valor SAP de 258 y un valor IY de 10, calculamos 258 - 10 = 248; luego su valor INS es de 248. El de palma es 199-53=146. El del aceite de oliva es 190-84=106 y el de girasol es 189 - 133 = 56. Así cuanto más bajo, más blando y más propenso al enranciamiento, y cuanto más alto, más duro y limpiador. Se establece que un buen equilibrio ronda los 130 - 160.
Cálculos de una fórmula de jabón, elección de aceites
Todos los cálculos de la fórmula se hacen mediante promedio aritmético. Así supongamos un jabón de coco (15%), palma (30%), girasol (5%) y oliva (50%). Usamos un kilo de grasas.
Para calcular el promedio de IY (por el orden de arriba):
$$ (0.15 * 10) + (0.30 * 53) + (0.05 * 133) + (0.50 * 84) = 1.5 + \\15.9 + 6.65 + 42 = 66.05$$
Para calcular el promedio de INS (por el orden de arriba):
$$ (0.15 * 248) + (0.30 * 146)+(0.05 * 56)+(0.50 * 106)\\ = 37.2 + 43.8 + 2.8 + 53 = 136.8$$
Los dos valores están dentro del margen establecido pero por ser el valor INS bajo el jabón saldrá más blando y suave. El valor de IY es un poco alto, se acerca demasiado al límite establecido por lo que la adición de un poco de vit E lo protegerá del enranciamient
Como otro ejemplo vamos al otro extremo quitando el girasol y añadiendo esa cantidad de coco:
coco (20%), palma (30%) y oliva (50%)
Para calcular el promedio de IY (por el orden de arriba):
$$(0.20 * 10) + (0.30 * 53) + (0.50 * 84) = 2 + 15.9 + 42 = 59.9$$
Para calcular el pormedio de INS (por el orden de arriba):
$$(0.20 * 248) + (0.30 * 146) + (0.50 * 106) = 49.6 + \\43.8 + 53 = 146.4$$
Los dos valores están otra vez dentro del margen establecido pero, por ser el valor INS un poco más alto, el jabón saldrá más duro y limpiador. El valor de IY es más bajo que antes. Ya no se se acerca al límite establecido por lo que la adición de vit E ya no es necesaria. Sólo probando ambas recetas sabremos cual se ajusta más a nuestros gustos y necesidades.
Cálculo del ácali de un jabón
Continuando con el cálculo de la lejía, la que se compone de sosa y agua. Para calcular la sosa lo primero que tendremos en cuenta es el sobreengrasado y para calcular el agua tendremos en cuenta la concentración.
Elegimos el primer ejemplo con una concentración del 30% y un sobreengrasado del 9%.
CALCULAMOS LA POTASA TOTAL
$$(150 * 0.258) + (300 * 0.199) + (50 * 0.189) + (500 * 0.190) \\= 38.7 + 59.7 + 9.45 + 95 = 202.85$$
Aplicamos el descuento del 9% (para lo que multiplicamos por 0.91, 91%)
$$202.85 * 0.91 = 184.5935; aproximando = 184.6$$
Lo convertimos ahora a sosa dividiéndolo entre 1.4025:
$$\frac{184.6}{1.4025} = 131.6$$
Por lo que la cantidad de sosa será 131.6 gramos (que poderemos dejar en 132 aproximadamente)
Cálculo del agua del jabón
Ahora calculamos el agua en función de la concentración. Si sabemos que el 30% de la lejía es 131, nos falta calcular cuanta agua será el restante 70%. Lo hacemos mediante una regla de tres (teoría de la proporción): ¿Si 131 equivales al 30%, cuánto será el 70%?
$$\frac{131\space gramos}{30\%}=\frac{x \space gramos}{70\%}$$
Por lo que:
$$ x = \frac{131\space gramos * 70\%}{30\%} \backsimeq 306 \space gramos$$
Si dispusiéramos de la concentración y quisiéramos saber la proporción calculamos para este caso:
$$Proporción = \frac{(100 - concentración)}{concentración} = \frac{}{} = 2.3333$$
Y sabiendo la proporción y la cantidad de sosa podemos calcular el agua:
$$131 \space gramos * 2.3333 = 305.6 \space gramos \backsimeq 306 \space gramos$$
Y ya tenemos todos los reactivos. Veamos:

Y le ponemos un poco de vit E acetato (aproximadamente 5 gramos, para evitar el enranciamiento. Es mucho más fácil hacer los cálculos utilizando las calculadoras online, en algunas como la calculadora de mendrulandia además predice los resultados del jabón producido. Algunos enlaces: SOAPCALC SOAPCALC. y CALCUWORD calcuworld.com/belleza/jabones/.
En la práctica se utilizará una mejor que la otra, según la experiencia.
Cómo crear una fragancia para el jabon
Para crear una fragancia primero hay que saber un par de asuntos referidos a las fragancias. La primera es que las diferentes esencias, que serán nuestros reactivos (en el mundo del jabón, se habla de ingredientes), tienen diferentes comportamientos.
Basándonos principalmente en el tiempo de evaporación podemos distinguir entre notas altas, medias y bajas. Las notas altas son aquellas que se volatilizan más rápido y por tanto duran menos y las notas bajasson las que se evaporan más lentamente y por tanto duran más.
Las notas medias tienen un tiempo intermedio de evaporación. Además, en casi todos los casos, las notas altas son más ácidas y frescas y las bajas son más dulces, pastosas e incluso un tanto no de olor agradable.
Las notas, como si se tratara de un acorde musical, interactúan entre ellas. Algunas son completamente armónicas proporcionando un aroma equilibrado y por supuesto agradable. Otras son disonantes y el olor puede ser desagradable o simplemente inestable.
Hay que buscar siempre mezclas que no se anulen puesto que no tendría entonces sentido. Generalmente las notas altas suelen ser las que primero se perciben, por lo tanto son la primera señal de la fragancia.
Después las notas medias son las que le dan cuerpo a la mezcla, proporcionándole el carácter. Las notas bajas, que se suelen usar en menor proporción, son las que sirven para dar durabilidad y estabilidad a la mezcla.
La forma de diseñar una fragancia o bouquet consiste en conocer bien las materias primas de que se dispone e ir mezclándolas en diferentes proporciones hasta conseguir la combinación que de desea. Al ser tan embriagadoras las esencias, no podemos abusar de la prueba de olfato pues acabamos por no distinguir nada. Así hay que oler la mezcla desde relativamente lejos y venteándola con la mano.
Una manera de comprobar el resultado de la posible mezcla es impregnar un algodón contando las gotas de cada ingrediente y meterlo en una bolsa para que se impregne el aire de dentro del aroma del algodón. Si olemos el algodón no estará tan clara la mezcla como si olemos el aire impregnado. Una vez que estemos satisfechos con la fragancia la podremos reproducir convirtiendo el número de gotas en gramos. Realizadas con notas armónicas altas, medias y bajas, las fragancias deben ser estables y no precisar ningún tipo de fijador artificial, aunque los hay. Además de las mencionadas como notas bajas, como fijadores naturales hay que destacar la tintura de benjuí, el bálsamo de Perú y la raíz de lirio.
Una fragancia elemental es la de rosa realizada con:

Midiendo el pH de los jabones
Para saber si un jabón es apto para su uso debemos medir antes su pH. El pH es un coeficiente que mide la acidez o alcalinidad de una disolución acuosa e indica la concentración de iones de hidrógeno presentes en ella.
S e mide a través de una graduación llamada escala de pH, que va desde el extremo más ácido = 0 al extremo más alcalino = 14, y en el centro está el 7, el valor neutro. El agua destilada tiene un pH neutro de 7 y el agua corriente suele tener un pH que se encuentra entre 6,5 y 8,5.
e mide a través de una graduación llamada escala de pH, que va desde el extremo más ácido = 0 al extremo más alcalino = 14, y en el centro está el 7, el valor neutro. El agua destilada tiene un pH neutro de 7 y el agua corriente suele tener un pH que se encuentra entre 6,5 y 8,5.
Un jabón bien realizado tiene que tener un pH neutro. Es decir, la sosa debe haber neutralizado todos los ácidos grasos de las grasas y por tanto existir un equilibrio entre ácidos y bases, o sea un estado neutro. Ahora bien, por ser el jabón como es, una sal débil, al contacto con agua, se disocia parte del álcali produciendo un efecto de causticidad leve. El pH, medido con tiras marcará entre 9 y 10, será básico.
Si pretendemos neutralizar ese efecto cáustico mediante un ácido, por ejemplo el cítrico, conseguiremos la separación parcial del jabón.
No se volverá a asociar y por tanto, sólo tendremos ácidos grasos y material neutro, en este caso, citrato sódico. Lo cual no es bueno para nuestro jabón.
Recordemos que el jabón es sólido, así que para medir su pH hay que humedecer la superficie del jabón del cual queremos conocer su índice de pH, para luego deslizar una tira medidora de ph sobre la superficie húmeda del jabón. Inmediatamente el color de la tira en contacto con el agua cambiará de color, por lo que hay que comparar el color resultante con el índice de colores de pH para poder indentificar el nivel de pH que tiene nuestro jabón. De esta forma sencilla y rápida podrás conocer el pH de tu jabón y verificar que es correcto para su uso en la piel.
El pH de la piel es ácido, normalmente se encuentra entre 3.5 a 5.5; rango en el que habitan aproximadamente 1,5 millones de microorganismos por centímetro cuadrado, los cuales se alimentan de la suciedad a la que se expone la epidermis todos los días. Estos microorganismos cumplen con una función benéfica para la piel, ya que secretan sustancias bactericidas que dificultan la colonización de microorganismos patógenos.
Cuando se presenta algún cambio en el pH de la piel, ya sea alcalino o ácido, causado por el jabón que utilizamos, puede provocarse irritación o alteración de la flora bacteriana que habita en ella, facilitando así la colonización de microorganismos patógenos. La importancia del pH en el jabón que toca nuestra piel.
El jabón con un pH mayor a 8 sobresatura la capacidad buffer de la piel (propiedad de mantener estable el pH), con el riesgo de modificar su pH hasta 3 unidades, mientras que los jabones de pH neutro pueden hacerlo en menos de 1 unidad, por lo que se recomienda el uso de jabones con pH entre 7 y 8.
De lo anterior radica a importancia de seleccionar un jabón que mantenga el equilibrio del pH natural de nuestra piel.
Una de las ventajas más importantes del empleo de jabones artesanales, radica en que se obtienen a partir de grasas vegetales saponificadas, las cuales son alcalinas por naturaleza. Es decir, todos los jabones en cuya elaboración se ha empleado aceite vegetal y sosa, dan como resultado una sal detergente junto a una glicerina hidratante obtenida durante la saponificación, la cual no se extrae del producto final, sino que funge como protector de la piel al disminuir el porcentaje de jabón que entra en contacto con la superficie cutánea.
Medir el pH del jabón con FENOLFTALEÍNA.
La fenolftaleína, de fórmula $C_{20}H_{14}O_4$,  es un indicador de pH que en disoluciones ácidas permanece incoloro, pero en disoluciones básicas toma un color rosado con un punto de viraje entre pH = 8,2 (incoloro) y pH = 10 (magenta o rosado). Sin embargo, en pH extremos (muy ácidos o básicos) presenta otros virajes de coloración: la fenolftaleína en disoluciones fuertemente básicas se torna incolora, mientras que en disoluciones fuertemente ácidas se torna anaranjado.
Demostraciones con fenolftaleína y análogos. Pero recordemos que el agua hace que el jabón suba a más de ese pH pero no hemos dicho que el alcohol no produce ese efecto. De manera que si diluimos un trocito de jabón en alcohol de 96º y le echamos unas gotas de solución de fenolftaleina y no cambia
es un indicador de pH que en disoluciones ácidas permanece incoloro, pero en disoluciones básicas toma un color rosado con un punto de viraje entre pH = 8,2 (incoloro) y pH = 10 (magenta o rosado). Sin embargo, en pH extremos (muy ácidos o básicos) presenta otros virajes de coloración: la fenolftaleína en disoluciones fuertemente básicas se torna incolora, mientras que en disoluciones fuertemente ácidas se torna anaranjado.
Demostraciones con fenolftaleína y análogos. Pero recordemos que el agua hace que el jabón suba a más de ese pH pero no hemos dicho que el alcohol no produce ese efecto. De manera que si diluimos un trocito de jabón en alcohol de 96º y le echamos unas gotas de solución de fenolftaleina y no cambia
a color rosa, es que el jabón es neutro (esto además demuestra lo que decía antes de la sal débil).Para preparar esa solución se diluye fenolftaleina al 0,1% en alcohol de 96º.
DWCP - Proceso de jabón en frío con descuento de agua
El método de saponificación en frío consiste también en mezclar materias grasas y sosa durante unos 20 minutos, pero sin calentarlos. Además, al contrario de la saponificación en frío, agregamos en la mezcla un exceso de aceite para para asegurarnos que toda la sosa reaccione y así provocar una saponificación completa.
Dejamos reposar nuestra mezcla entre 24 y 48 horas en unos moldes de madera. Empieza entonces la primera fase de saponificación durante la cual se produce un calentamiento natural de la mezcla.
El proceso en frío conlleva que el jabón una vez desmoldado y cortado necesite entre 4-6 semanas más para madurar. En este tiempo se seca, se endurece y el pH baja a valores entre 8, 5-9, 5.
La saponificación en frío por lo tanto sigue un proceso artesanal, lento debido al periodo de curación necesario para obtener una reacción completa.
Se puede considerar DWCP el rango de concentración comprendido entre 30 y 50%. En algunos jabones, los que tienen aceites más duros, es mejor usar valores más bajos de concentración o sea más agua. Pero aquí existe una cuestión a menudo se obvia que es que los aceites más blandos admiten concentraciones mayores.
Que a partir de cierto grado de concentración es probable que, si se llega a determinada temperatura, tiendan a cortarse, lo que se refleja como un jabón friable (que se desmenuza).
Es decir, que hay que trabajar en frío además de muy rápido ya que estos jabones tienden a alcanzar la traza espesa muy rápidamente.
Pero, tenga en cuenta, que la lejía cuanto más concentrada más peligrosa, más quema por lo tanto cuidado. Hay que trabajar muy rápido para lo que hay que tener todo muy bien preparado de antemano y muy bien organizado.
La temperatura de partida de los ingredientes es directamente proporcional a la posibilidad de fracaso. Es decir que hay que esperar que aceites y lejía estén fríos para empezar a mezclarlos.
Tenga cuidado con ingredientes que aceleren mucho la traza y batir poco o nada con la batidora si usas ese tipo de implementos.
Por todo lo dicho es un proceso que requiere un poco más de cuidado y experiencia que otros mencionados. Sobre todo por que la mezcla esté bien proporcionada para que el jabón llegue a reaccionar completamente.
Ventajas del jabón saponificado en frío Healthy Home
Los jabones saponificados en frío contienen glicerina naturalmente producida durante la saponificación. La glicerina permite una mejorhidratación de la piel y, por lo tanto, mejor preservación. Por eso, los jabones saponificados en frio se recomiendan especialmente para pieles secas y sensibles.
Otra ventaja es que al no calentar las grasas vegetales y la sosa, conservamos los beneficios del aceite y mantenemos sus propiedades emolientes, suavizantes, protectoras y nutritivas. El método de saponificación en frío permite conservar al máximo todos los componentes.
Destacamos así la presencia de vitamina E (tocoferol), un antioxidante que permite ralentizar el envejecimiento y la oxidación de los aceites vegetales presentes en el jabón. Es por esa razón que, es aún más interesante seleccionar materias primas de calidad, naturales, orgánicas y evitar cualquier pesticida o disruptor endocrino.
Por lo tanto, los jabones saponificados en frío son generalmente una garantía de calidad. Las materias primas son cuidadosamente seleccionadas, principalmente orgánicas. Los aditivos son generalmente de origen natural, como aceites esenciales para perfumar o arcilla para colorear.
Además, gracias a la preservación de los beneficios de los aceites grasos en el proceso de saponificación en frío, la sensación de la piel después del lavado es mucho más agradable y suave que cuando se usa un jabón convencional.
Elegir un jabón saponificado en frío, es elegir un producto de calidad, respetuoso de nuestra piel y del medioambiente.
Lavado de un jabón con sal
Es una técnica que consiste en diluir un jabón en agua saturada en sal, esto se lleva a cabo para que la sal rompa la molécula del jabón y de esa forma se separe de otras sustancias como aromas, exceso de sosa, grasas no saponificables, etc y así, al no ser soluble en el agua, el jabón se separa y acaba flotando en la superficie (parte útil), el agua que queda en la parte inferior contiene “la suciedad” y la glicerina del jabón, éste agua se desecha. Hacer lavado con sal es conveniente cuando:
- Lotes de jabón que no nos han salido bien…
- Tenemos muchos restos de jabón de distintos tipos y colores…
- Se nos ha estropeado y huele a rancio…
- El jabón huele “rarito” por que lo hicimos con aceite reciclado y no nos gusta el olor…
- Por que está mal formulado y tiene el pH demasiado alto…
¿Técnica del lavado con sal?
La técnica del lavado del jabón con sal (relargage o precipitación salina) es una técnica usada tradicionalmente para elaborar el famoso Jabón de Marsella. Básicamente consiste en derretir el jabón en agua saturada con sal, que hace que el jabón se separe de los otros componentes.
La sal disocia (“rompe”) la molécula de jabón, separándola de otras sustancias que si son solubles en agua (como un exceso sosa, fragancias, malos olores, colorantes,…) y los ácidos grasos sin saponificar. Es decir, el jabón pierde solubilidad y se separa del agua.
Como las moléculas de jabón no son solubles en agua salada, se separan y flotan, por lo que la pasta de jabón flotará en la parte superior y en la parte inferior quedará el agua sucia. Filtramos la pasta de jabón (separamos el sólido del líquido) y tiramos el agua sucia.
Respecto a la glicerina, es muy apreciada en jabones de uso cosmético, pero en jabones para la lavadora, no es tan interesante, ya que puede dejar manchas blancas en la ropa oscura. En el agua que desechamos, está la glicerina del jabón (aprox. un 10% del peso del jabón). En procesos industriales, esta glicerina se recupera y purifica mediante destilación.
Con el lavado del jabón con sal, obtendremos un jabón para la lavadora más puro, más “limpio”, de muchísima más calidad.
Proceso de lavado de un jabón con sal
- Cortamos 500 gr de jabón en trocitos pequeños o lo rallamos. Añadimos 1 litro de agua y lo dejamos en remojo 1 o 2 días. Yo lo hago así por que es más cómodo, pero si tienes prisa, rállalo o tritúralo y pasa al siguiente punto. AULA NATURAL
- Ponemos 1 litro de agua al fuego. Añadimos la sal.
Cuanto más “sucio” el jabón, más sal. Mínimo recomendado: 100 gr de sal por litro de agua. Máximo 360 gr de sal por litro de agua, que es el coeficiente de solubilidad de la sal (aunque añadas más sal no se va a diluir).
- Calentamos el agua hasta que se diluya la sal.
- Añadimos la pasta de jabón que teníamos en remojo (o directamente el jabón rallado). Lo calentamos todo a fuego medio/bajo hasta que se haya fundido todo el jabón (entre 30 y 60 min.).
- Batimos para asegurarnos que no queda jabón sin diluir. Apagamos el fuego y dejamos enfriar.
- Al cabo de unas horas, cuando ya está frio, separamos la pasta de jabón (será como una pastilla dura) y desechamos el agua*. Podemos separarlo antes, pero estará blando y será más dificil manejarlo. Es mejor tener paciencia y esperar a que se enfríe.
Con la pasta obtenida, se podra obtener un buen jabón liquido para lavadora o usarlo en polvo también para la lavadora.

Preparación del sebo y su uso en el jabón
Jabones con sebo de vaca.
Los jabones obtenidos con sebo de vaca tienen un buen aroma. Obviamente no huele a vaca. Otras cualidades que aporta al jabón son la blancura, la dureza y la cremosidad y consistencia de la espuma. Se mezcla con aceite de oliva y algo de aceite de coco pero siempre se ha usado sólo con coco y ha funcionado perfectamente. Es un ingrediente comparable a la manteca de cacao que ya sabemos que resulta carísima.
El sebo se debe limpiar quedándonos sólo con el sebo más puro, siendo éste el más duro y blanco, denominado sebo en rama. Si conseguimos triturarlo en gusanillos, mucho mejor porque se le sacará mayor rendimiento.
Una opción es ponerlo a cocer en una olla con igual peso de agua y un 3% de sal y se cuece para que se vayan rompiendo los tejidos celulares y soltando así su contenido. Los restos se van oscureciendo y reduciendo y quedan flotando en una mezcla blanquecina. En menos de una hora el primer paso del proceso debe de finalizar y, aun caliente, lo colamos con una tela en otro recipiente.
La otra opción es hacer esto sin agua. El rendimiento es mayor pero hay que cuidar que no queme la grasa lo que se traduciría en un sebo más oscuro y oloroso. Hay que hacerlo a fuego muy lento y sin dejar de removerlo.
El resultado lo dejamos enfriar, si es en la nevera mejor, de manera que el sebo se queda flotando sobre el agua y solidifica, permitiéndonos separarlo fácilmente del agua que permanece líquida. La parte inferior del sebo tendrá más impurezas, por lo que se puede eliminar esa capa o lavar bajo el grifo de agua fría.
Este sebo ya nos serviría para hacer el jabón pero, para mi gusto, aun tiene bastante olor y posiblemente algo de color. Ahora se trata de depurarlo o purificarlo para quitar, entre otras cosas, los ácidos grasos libres que propician la ranciedad. Eso nos permitirá guardarlo por más tiempo.
Algo más sobre el sebo y su uso en el jabón
Depuración y desodorización del sebo de vaca
Para la primera depuración se debe usar una lejía muy, muy suave que reaccionará con los ácidos grasos convirtiéndolos en jabón. Estamos hablando de que para un kilo de sebo pondremos medio de agua y de 3 a 5 gr de sosa cáustica. Cociendo esto brevemente se obtendrá una espuma grisácea en la superficie, que iremos eliminando con una espumadera, como con el caldo, hasta que deje de aparecer.
A la vez en el agua se irán depositando las sustancias mucilaginosas. Esta vez hay que dejarlo enfriar lo más lentamente posible para favorecer que se decanten las impurezas. Cuando se enfríe completamente, se procede como en el paso anterior y lo separamos del agua.
Este penúltimo paso te lo saltas o no, según tu nivel de exigencia olfativa. Se vuelve a cocer con un 2% de sal y un 1% de alumbre lo que lo debe desodorizar completamente. Cuando se enfríe completamente, se procede como en el paso anterior y lo separamos del agua.
Cogemos el sebo ya decantado, blanqueado y desodorizado y lo calentamos para eliminar todo el agua que contenga, que lo hará cuando supere los 100ºC y es posible que aun ahora suelte algo de espumita por encima que eliminaremos con un colador metálico o espumadera.
Una vez frío, tendremos un sebo de primera que producirá unos jabones de gran calidad.
Alguna ayuda para hacer mejor nuestros jabones
Para hacer jabones nos conviene apoyarnos en algunas herramientas. En algunos casos se trata de tablas para comprender los ingredientes. En otros se trata de aplicaciones que nos facilitan los cálculos y así dedicarnos más enteramente a hacer jabones, una de estas tablas es la tabla de saponificación.
La tabla de saponificación es necesaria para hacer los cálculos para la elaboración del jabón. Se ofrecen dos valores SAP para dos tipos de álcali en función de si se quiere obtener jabones sólidos o líquidos.
El valor del yodo determina la tendencia al enranciamiento y el valor INS nos aproxima a las características finales de un jabón realizado con esa grasa.
La tabla de saponificación es una aproximación, ya que cada lote de grasa puede variar. Que los valores que aquí se exponen son los valores medios. Otra cosa que suele ocurrir es que podemos encontrar tablas para KOH o para NaOH, lo que nos puede confundir a la hora de calcular el álcali. Aquí aparecen los dos valores. La relación entre ambos es de 1,4025. Es decir que 1000g de NaOH equivalen a 1402,5g de KOH. Para más detalles se puede consultar la ayuda de la calculadora de saponificación.
Haciendo jabón
Jabón de glicerina
El proceso de fundir y verter es el método más sencillo de elaboración del jabón y no por ello simple. Las combinaciones, formas, olores y colores son ilimitados, dejando en manos de la imaginación de cada cual infinitas posibilidades.
Se llaman jabones de glicerina porque, sobre todo originalmente, se les añadía en la fabricación glicerina líquida para impedir que el jabón cristalice, y esto les da el aspecto transparente. También existen bases de glicerina bases opacas.
Para la elaboración de jabones de glicerina, se requiere saber lo siguiente:
En condiciones normales el jabón suele cristalizar de forma amorfa, es decir, desordenadamente. Es la disposición de este tipo de cristales la que proporciona opacidad al jabón. Hay otras formas de cristalización que producen un resultado transparente y esas son las que nos interesan. los reactivos que lo hacen posible, son:
Hay ingredientes que favorecen este tipo de cristalización. Principalmente los alcoholes. Por su precio, se dejó de utilizar el alcohol en beneficio de la glicerina que a los jaboneros de la época les salía más barata por ser un subproducto de la elaboración de jabón. De ahí viene la denominación de jabón de glicerina.
También hay que tener en cuenta los ingredientes de carga. Se denomina carga a aquellos elementos que sirven para dar mayor rendimiento al aceite y esto quiere decir que, con la misma cantidad de aceite, sale mayor cantidad de jabón.
Algunos elementos de carga, como el almidón, el talco, la arcilla, etc., producen también opacidad pero algunos como el azúcar o la sosa pesada (carbonato sódico hidratado) no solo no producen opacidad sino que favorecen la transparencia. Teniendo esto en cuenta se comprenderá mejor para qué sirven los ingredientes de la fórmula de la que vamos a partir.
Elaboración de la base del jabón de glicerina
En esta formulación, el aceite de coco proporciona la espuma, el de ricino mejora la transparencia y el ácido esteárico proporciona dureza (en este caso es fundamental para que tenga consistencia). El azúcar proporciona transparencia y consistencia y el alcohol transparencia.
El proceso es en caliente, mezclando los aceites previamente derretidos, con la lejía previamente mezclada. Por las características del ácido esteárico, la saponificación es inmediata.
El porceso en caliente consiste en que al al proceso de fabricación del jabón se le aplica calor con una fuente externa. Hay muchas formas de aplicar ese calor pero nos centraremos, para esta explicación, en el proceso en el horno. Hay que decir también que todo esto se puede hacer perfectamente con dos ollas: al baño maría, en el microondas o a fuego directo. Pero al horno es el método más sencillo y más seguro.
El jabón en caliente tiene dos ventajas principales: Una es que no hay que esperar (o hay que esperar muy poco) para poder usarlo y la otra es que una vez finalizado el proceso de saponificación, le podemos agregar colorantes, aromas y aditivos sin miedo a que por la alcalinidad se nos echen a perder.
La formulación para elaborar un kilo es: (ver en la sección 3.5.6, cómo se hace la base de glicerina).

Para la elaboración de jabones seguiremos al pie de la letra las indicaciones en el proceso en frío sólo que esta vez no le vamos a añadir las esencias ni lo vamos a verter en el molde. Es preferible no poner tampoco el sobreengrasado o incluso dejar un ligero SE negativo para que la mezcla esté más fluida y añadirlo al final del proceso, con las esencias.
En lugar de eso, una vez mezclados los aceites con la lejía, lo vamos a meter en el horno a una temperatura aproximada de 80ºC. Hay que asegurarse que el jabón esté bien 'trazado' antes de meterlo en el horno.
De media a una hora aproximadamente veremos como el jabón gelifica. Esto es que se vuelve semilíquido y transparente. Cuando su aspecto sea completamente homogéneo y todo el jabón presente ese aspecto de gel, lo removemos bien y lo dejamos otro ratito en el horno. Dependiendo de la cantidad de agua que le hayamos puesto, la masa será más o menos removible.
Fluidificación del jabón o cómo hacer para removerlo
Podemos usar algunos ingredientes para conseguir que la masa sea más fluida y por tanto más fácil de remover y de moldear. Entre estos ingredientes está el sodio lactato (añadiendo hasta un 3% del peso de las grasas) que aporta además dureza y suavidad al jabón. O como decía más arriba, también se le puede poner un sobreengrasado inicial negativo, o sea un poco más de sosa de la que necesitaría y que luego se debe compensar con el sobreengrasado. También se puede hacer una mezcla suave de sal y/o carbonato sódico o potásico a partes iguales en una cantidad máxima del 1% del peso total del jabón, diluido en 4 o 5 veces su peso en agua destilada.
Así por ejemplo para un jabón de 2 kg se pondrían 10 gr de sal, 10 gr de carbonato sódico diluidos en 100 gr de agua destilada. Esto se le agregará después de que el jabón gelifique completamente. Después de unas dos horas en el horno podemos comprobar el pH del jabón y si nos sale un resultado aceptable, damos por concluida su cochura. COCHURA: Cocción, especialmente la que se hace en el horno.
Añadir el sobreengrasado y otros aditivos al jabón
Si habíamos decidido reservar un aceite más delicado para el sobreengrasado, éste es el momento de añadirlo. Si le vamos a poner colores, los cuales al no verse afectados directamente por la acción de la sosa resultarán más homogéneos y duraderos, se los ponemos justo antes de añadir los aromas.
En este caso no tenemos que temer por el hecho de que las esencias vayan a 'fraguar' el jabón de golpe porque, al estar ya hecho, no debe de cambiar su consistencia.
También las esencias cunden más si no se ven sometidas a la acción de la sosa pero hay que tener cuidado porque, si la masa está demasiado caliente, se puede volatilizar gran parte de la esencia y por esto, es lo último que debemos añadir antes de verter en el molde. Si el molde lo permite, incluso le podemos poner en él las esencias y mezclarlas ahí con el jabón.
Cuidado con la temperatura
Hay que evitar altas temperaturas en el horno ya que producirían burbujas en el jabón perjudicando su aspecto, pero hay que mantener la temperatura lo suficientemente alta como para que el jabón permanezca fluido. Si está un poco frío y no se han añadido ingredientes fluidificantes el moldeado se puede volver una pesadilla.
Un problema que puede darse con determinada facilidad es que al no estar suficientemente trazado el jabón, se separe (se corte) al meterlo en el horno. En ese caso hay que sacarlo, añadir poco a poco agua fría, removiendo hasta que se vuelva a emulsionar. Ese exceso de agua habrá que cocerlo luego de más para que se evapore.
Seguimos pensando que el jabón elaborado en frío tiene una textura más suave que el de en caliente pero es un método que como he dicho también tiene sus ventajas.
Haciendo la base de glicerina
Al mezclar las grasas con los álcalis la masa solidifica de golpe, pero no hay que desesperar y remover hasta que sea homogénea y semilíquida. Para ello tiene que tener bastante temperatura, alrededor de 80ºC. La olla conviene que tenga una altura suficiente para prevenir la posible subida de la masa que puede llegar a hervir por la velocidad del proceso de saponificación del ácido esteárico.
Una vez que todo está bien homogéneo se mete en el horno o baño maría (entre 80 y 90ºC) durante 2 horas para conseguir la saponificación total de las grasas. Ésta se verificará mediante la prueba de pH, bien con fenolftaleina, con tiras o con la lengua.
Cuando esté completada la saponificación se añadirá, a una temperatura de 60ºC, el jarabe previamente realizado con el azúcar y el agua, hasta su completa homogenización, lo que da al jabón un aspecto y consistencia más plásticos.
Por último, hay que añadir (evitando los vapores y lejos de cualquier llama) poco a poco el alcohol. Esto hace que la masa se vuelva completamente transparente y muy,muy líquida. Casi como agua, que nadie se preocupe. A veces se usa la batidora a velocidad muy lenta para completar la mezcla.
El resultado hay que colarlo por los posibles restos de jabón no disuelto y verterlo en un molde a ser posible que se pueda tapar dejándolo reposar hasta que se enfríe completamente. Ya debe de estar realizada nuestra base de glicerina.
Posibles problemas al hacer la base de glicerina
Puede suceder que quede una capa superior de espuma que no tiene mayor relevancia al retirarla y puede que parte del aceite no saponificado quede también en esa capa superior. Por eso es tan importante hacer la prueba del pH.
Si el jabón tiene un exceso de sosa, nada conveniente, hay que compensar ese exceso añadiendo aceite cuando se refunda la base.
Las variaciones que ofrece la receta son infinitas, como no. Pero hay que destacar la existencia del Propilenglicol y Dipropilenglicol como disolventes a sustituir parte de alcohol o la glicerina y el sorbitol que también produce más transparencia.
También la sal común en cantidad muy moderada produce más dureza lo que permite la utilización de otros aceites.
Jabón medicinal de tocador
Este es un jabón de tocador elaborado en una base de aceites vegetales de la palma africana y la glicerina como humectante, adicionando otros tipos de componentes se logran jabones medicinales como el de caléndula, el de manzanilla y los de frutas naturales, cáscaras y cortezas con diferentes aplicaciones.
Para su preparación se deben seguir los siguientes pasos:
En un recipiente preferiblemente de vidrio agregamos todos los componentes y los colocamos en la estufa a fuego medio mezclando constante y moderadamente con una cuchara de madera o plástica resistente al calor, hasta que se disuelva la base de jabón de palma.
Luego la dejamos reposar por media hora hasta que se forme una nata en la parte de encima la cual se rompe y se vierte el liquido a los moldes tratando que no sea muy alto para que no formar burbujas, por ultimo, se dejan secar por 1 hora, este es el jabón de glicerina humectante, para elaborar jabones medicinales para lo cual se debe de recurrir a las plantas y a los frutos como es el caso de la mandarina la cual sus cáscaras son excelentes para combatir la celulitis, lo que se hace es hervir las cáscaras o los frutos o las cortezas en el proceso y sacarlas antes que forme la nata o dejarlas, para hacer jabones de tocador exfoliantes, para lo que se parten pequeños trozos de estropajo y se adicionan a la mezcla, podría utilizar la manzanilla y la caléndula para las impurezas de la piel, miel para hidratar la piel, pepino para cerrar poros y piel mixta, durazno para limpiar espinillas.
Para jabones esotéricos la canela de uso comestible, si se utiliza otro tipo de canela, puede ocasionar picazón en la piel; sándaloru o ruda, también se hierve, algunas como los cítricos y en vez de agua se utiliza el jugo puro, y las otras se pueden licuar como el durazno por ejemplo.

Jabón de baño
El jabón de baño es un elemento comúnmente utilizado para la higiene personal y la limpieza; por lo que elaborarlo reciclando aceite vegetal desecho de los alimentos que se preparan fritos, causa un costo bajo de materias primas, un proceso de reciclaje que contribuye con el medio ambiente reduciendo la polución en los suelos, contaminación de mantos acuíferos, ríos, lagos y mares, otorgando beneficios para las cafeterías, comedores, carritos de comida, etc. ya que reciben dinero a cambio de ese aceite.
Para el porcedimiento a seguir es muy importante el paso a paso y la medida de los reactivos (ingredientes):
Notas importantes
Antes de mezclar el aceite en la lejía debe estar a punto de hervir, La caldera debe estar muy limpia, los moldes con la pasta deben estar en un sitio fresco.
Advertencias para la fabricación: El empaste podrá retardarse o adelantarse. Si empieza el empaste antes de los 5 minutos es por que la lejía está demasiado fuerte; en este caso, hay que debilitarla por medio del agua fría, mezclada con la misma cantidad de aceite y si después de 25 minutos de mezclar continuamente no se efectúa el empaste, se prueba la parte líquida con la lengua, si esta muy picante le falta aceite o grasa y hay que ponérsela en la cantidad conveniente: si está muy salada es señal de que le falta lejía.
Para pintar el jabón , debes tener en cuenta los colores mas fuertes en la jabonera moderna son tres: Rosado, Azul, Violeta.
COLOR ENCARNADO: se obtiene por medio de pequeñas cantidades de bermellón, diluido en dos cucharadas de aceite y dos de lejía a 12º. Se hace una masa y se va echando con el jabón al mismo tiempo que este pasa al molde.
COLOR AZUL: unos gramos de azul de ultramar, la mitad de añil, mezclado con 2 cucharadas de aceite de oliva y otras dos de lejía a 12º.
COLOR VIOLETA: se obtiene fácilmente con bermellón y azul de ultramar y se mezcla con lejía y aceite de oliva a 12º, y se aplica del mismo modo que los anteriores.
COLOR VERDE: esta coloración se obtiene con bicromato y azul de ultramar.
Para la fabricación del Jabón de tocador (de baño) hay que tener presente las recomendaciones anteriores y se debe fundir la grasa en el baño maría, se mezcla el color preparado y cuando haya adquirido la temperatura conveniente se le añade la lejía, se procura a la mezcla la misma cantidad de calor durante la operación, se agrega continuamente hasta que empiece a empaste que es cuando se le agrega el perfume, se continua mezclando hasta que se vierta en el molde el cual se tapa con cuidado.
A continuación se presentan algunas fórmulas de jabones de tocador; todas de excelentes resultados:
Jabón de miel para tocador
El proceso es el siguiente: Recuerda trabajar en un lugar con buena ventilación y con las medidas de seguridad apropiadas (guantes, mascarilla y gafas). Vertemos la sosa sobre el agua destilada y removemos sin salpicar.
La temperatura ascenderá a 80ºcelsius aproximadamente y debemos dejar reposar hasta que baje a 40-50º. Mientras seguimos preparando el resto de materiales. Hacer jabones
La formulación para obtener una libra de jabón es:
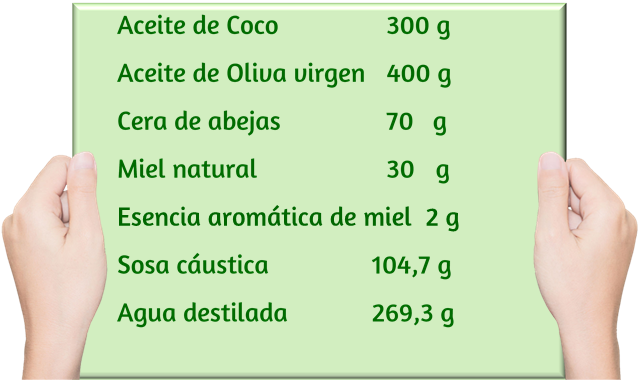
Coloca en un recipiente la cera de abejas para fundirla. Agregue el aceite de coco y dejar que se funda. Apagamos el fuego e incorpora el aceite de oliva vírgen, dejando que el calor del recipiente los vuelva transparentes.
Mientras se espera que se alcance la temperatura para ambas mezclas ponemos la plantilla de la cera de abeja en el fondo del molde y pesamos la esencia aromática en un vaso para tenerlo a mano. Vertemos el aceite en un recipiente amplio que nos permita trabajar la mezcla en él y cuando ambas mezclas se encuentren entre 40-50º introducimos la batidora en el recipiente y mientras batimos suave y
sin salpicar añadimos la mezcla de sosa de una sola vez. Cuando la mezcla adquiera la consistencia tipo puré incorporamos la miel natural y seguimos batiendo para que se integre. Para finalizar, sin dejar de batir añadimos la esencia. Buscamos el punto de traza para la mezcla y cuando esté lista la vertemos en el molde y alisamos la superficie. Dejamos endurecer 24 horas.
Una vez endurecido, lo cortamos en pastillas ya que si esperamos a cortarlo cuando haya saponificado estará demasiado duro y puede quebrarse. Es aconsejable realizar el corte del jabón recién endurecido que todavía tiene una consistencia que permite su manipulación. El jabón antes de utilizarlo debe reposar 4 semanas.
Jabón nutritivo de zanahoria
Notas e importancia de este jabón:
Tenga presente que este jabón cuida la piel, dado que todos los ingredientes a utilizar son naturales y en este caso concreto vamos a hacer uno con zanahoria que sin duda, es bastante bueno.
Es importante saber que las zanahorias no solo nos permite conservar el bronceado de la piel en verano, sino que la presencia de carotenos entre sus componentes nos permite combatir los radicales libres y con ello vamos a retrasar el envejecimiento, además de mantener la piel hidratada y tratar incluso casos de eccema o de cicactrización de heridas.
Su alto contenido en beta-caroteno hace que el jabón de zanahoria sea usado como potente antioxidante, siendo capaz de proteger nuestra piel por ejemplo, ante la acción de los rayos solares y el contacto con el medio ambiente externo. Su vitamina E posibilita que se produzca una regeneración celular óptima, proporcionando un mayor brillo al rostro.
Este jabón es muy recomendable para las personas de piel sensible y no puedan utilizar determinados tipos de jabones o los que son industriales.
Es uno de los jabones naturales que mayores posibilidades ofrece en cuanto a su acción antiinflamatoria se refiere y no deberías obviar esta opción.
La aplicación de este jabón de zanahoria está especialmente indicado para aquellas personas que presentasen debilitamiento en el cabello y quieran tanto nutrirlo como aportarle una mayor hidratación, potenciando su elasticidad. Combate el envejecimiento celular ayudando a prevenir la aparición de incomodas estrías que suelen producirse con el transcurso de los años. Disminuye naturalmente las manchas producidas por el acné, cantidades excesivas de grasas en el cuerpo y favorece la restauración del pH natural de la piel.
El proceso es el siguiente:
Lo primero que debe hacerse es poner en un bol o recipiente, el puré de zanahorias, la sal, el agua y luego poco a poco y con mucho cuidado, la sosa caústica. Con una cuchara o palo, se va mezclando todo y no te asustes con la temperatura ya que la sosa caústica es la que provoca ese aumento de la temperatura. Una vez todo mezclado deja enfriar durante una hora.
Cuando la mezcla está fría,se adicionan los aceites, incluyendo el ylang ylang. Blogverde.com Ellos se deben añadir mientras se está removiendo en círculos y sin parar y hasta que se note que toda la mezcla se vuelve más densa y consistente.
Ahora necesitas un molde, o varios, (de silicona o madera) para agegar alli la mezcla lo mejor es que lo tapemos con un papel para el
proceso de hornear,(la parte brillante hacia afuera) ya que así te será más sencillo desmoldar el jabón. Es necesario dejar transcurrir al menos 48 horas para que el jabón se endurezca. Tras desmoldarlos, se deben colocar en una rejilla y en un lugar aireado para que durante un mínimo de seis semanas se cure el jabón.
Otros aceites que se pueden utilizar para mejorar las características del jabón de zanahorias son: aceite de oliva, aceite de coco y cuatro ingredientes que realzanlas porpiedades y los pueden hacer únicos: manteca de karité, aceite de palma virgen, aceite de zanahoria y, por supuesto, la zanahoria triturada.
La formulación para obtener una libra de jabón es:

Jabón de avena
LA AVENA: la avena ha sido consumida como alimento desde la antigüedad, su nombre es Avena Sativa y pertenece a la familia Poaceae. Es un cereal mayormente cultivado en Europa y Norteamérica.
Su cultivo necesita un clima húmedo y fresco; los principales países productores son Rusia,Canadá, Estado Unidos, Finlandia y Polonia. Su consumo se ha visto ha incrementado en los últimos años.
La avena es un cereal con un valor energético de 361 kcal por 100 g. Es fuente de proteínas de bajo costo y posee un alto contenido en fibra. Si lo comparamos con otros cereales.
En cuanto a los micronutrientes, la avena posee un alto contenido en hierro, magnesio, zinc, fósforo, tiamina (vitamina B1), vitamina B6y folatos, además, de ser fuente de potasio y vitamina E.
Además, este cereal es una buena fuente de componentes no nutritivos/bioactivos como ácidos fenólicos, flavonoides y fitoesteroles. Asimismo, contiene dos tipos de fitoquímicos que son únicos de este alimento: las avenantramidas (AVAs) y las saponinas esteroidales. La avena es un alimento rico en beta glucanos. Éstos son polisacáridos componentes de la fibra dietética, resistentes a la absorción y digestión en elintestino delgado y fermentados en el colon, atenuando el colesterol sérico y la respuesta de glucosa sanguínea.
Desde el año 1997 la Food and Drugs Administration (FDA) en Estados Unidos, declaró que una ingesta diaria de 3 g de beta glucanos de la avena puede disminuir el colesterol sérico total así como el colesterol LDL.
Además, podría tener un efecto anticancerígeno al reducir los compuestos que son agentes causantes de cáncer de colon, reducir los niveles séricos de colesterol y la presión arterial.
Algunos de los micronutrientes y compuestos no nutritivos contenidos en la avena benefician distintos procesos metabólicos esenciales para el organismo. La vitamina E es un compuesto antioxidante conocido por proteger al cuerpo de los efectos de los radicales libres y jugar un papel importante en la prevención de enfermedades como cáncer, artritis, aterosclerosis, cataratas, entre otros.
Los compuestos fenólicos que contiene también tienen efectosimportantes, ya que son conocidos por ser potentes antioxidantes. Estudios recientes han encontrado que dichos compuestos también mejoran la función endotelial, la señalización celular y tienen propiedades anti inflamatorias.
Las avenantramidas (AVAs) son un grupo único de antioxidantes presentes en la avena. Se ha visto que los AVAs tienen una actividad antioxidante de 10 a 30 veces mayor que la de otros compuestos fenólicos. Además, tienen propiedades anti inflamatorias y anti aterogénicas. De igual forma, ayudan a controlar la presión arterial al producir óxido nítrico, el cual actúa como vasodilatador Fundación Española de la Nutrición, FEN..
¿POR QUÉ SE USA EN COSMÉTICA?
La avena posee una composición química compleja, de la cual destacan aquellos componentes que poseen acciones interesantes sobre la piel:
- Las avenantramidas
La avena es el único cereal que contiene las avenantaramidas. Estas son compuestos formados por un ácido antranílico unido con un enlace peptídico a un ácido hidroxicinámico. Estos compuestos poseen propiedades biológicas como actividades antioxidantes, antiinflamatorias, antiaterogénicas, antiirritantes y antiproliferativas, además de prevenir enfermedades coronarias.
las avenantramidas son solubles en agua, su extracto penetrará más profundamente y en mayor cantidad en productos cosméticos con un porcentaje alto de fase acuosa, que en aquellos con un elevado porcentaje de fase grasa.
Estos compuestos presentan actividad antiinflamatoria al inhibir la liberación de citoquinas y de histamina, por lo que su aplicación en productos cosméticos es muy aconsejable a la hora de tratar pieles secas y/O sensibles que sufren irritación de manera frecuente. En estos casos los extractos de avena o la avena coloidal puede mejorar de manera notable la sensación de tirantez, sequedad, O aspereza y minimizar los posibles picores.
- Los Beta-glucanos
El beta-glucano es un tipo de fibra soluble que se encuentra de forma natural en la avena y, aunque también se pueden encontrar en la cebada, algas y setas. Como otros tipos de fibra soluble, en el organismo, el betaglucano forma geles viscosos en el tracto gastrointestinal, retrasando el vaciamiento gástrico e interfiriendo con la actividad de diferentes enzimas pancreáticas, lo que ralentizalos procesos de digestión y absorción de nutrientes e incrementa la excreción de ácidos biliares, además, que contribuye a regenerar la piel, ya que estimula la síntesis de colágeno, y por tanto hace que la piel gane en firmeza.
- Las vitaminas
En la avena encontramos una importante presencia de biotina. Esta es la conocida vitamina H, es parte del grupo de vitaminas del complejo B. Todas las vitaminas B ayudan al cuerpo a convertir los alimentos (carbohidratos) en combustible (glucosa), que se utiliza para producir energía, también ayudan al cuerpo a metabolizar las grasas y las proteínas.
Como todas las vitaminas B, la biotina es soluble en agua, lo que significa que el cuerpo no la almacena. Las vitaminas del complejo B son necesarias para una piel, cabello, ojos e hígado saludables. También ayudan a que el sistema nervioso funcione correctamente.
Esta vitamina es importante para metabolizar los carbohidratos, las grasas y los aminoácidos, los componentes básicos de las proteínas. La biotina se recomienda a menudo para fortalecer el cabello y las uñas, y se encuentra en muchos productos cosméticos para el cabello y la piel.
Esta vitamina participa activamente en la síntesis de queratina, la cual es la proteína que conforma nuestro cabello. Por esta razón sus extractos incorporados en un champú son una buena idea si queremos mantener un cabello sano.
Por todo ello los extractos de avena resultan una opción interesante para incorporar en tu cosmética, ya sea en emulsiones, tónicos, aguas de limpieza o champús.
- Los Oligoelementos
Recordando que la avena es uno de los cereales más completos ya que, es rica en proteínas de alto valor biológico, contiene hidratos de
carbono, grasas, un gran número de vitaminas y minerales. Con esto ya sabemos que el consumo diario de avena nos proporciona una buena dosis de las sustancias necesarias para nuestro organismo, entre oligoelementos y vitaminas, se tiene: 100 g de avena contienen: 5 mg. de sodio, 400 mg. de potasio, 70 mg. de calcio, 430 mg. de fósforo, 140 mg. de magnesio, 4 mg. de hierro, 0,47 mg. de cobre, 4 mg. de cinc, 0,56 mg. de vitamina B1, 0,15 mg. de vitamina B2, 1 mg. de vitamina B3 y 0,16 mg. de vitamina B6. También 1,1 mg. de vitamina E zonadiet.com.
Su formulación es:


JABONES LÍQUIDOS
Jabón Líquido
El jabón líquido se obtiene frecuentemente de la saponificación de aceites o grasas con un alto contenido de ácido oleico y una mezcla proporcional de hidróxido de sodio y de potasio. El resultado es un producto de color oscuro y olor fuerte. Se ha encontrado que utilizando ácidos grasos con una longitud de cadena más grande y ácido sarcosínico, se obtiene un jabón líquido con mejor aroma y color, pero el proceso es bastante costoso.

Los jabones líquidos
Se dice que en 1865, William Shepphard patentó una versión líquida de jabón, que consistió en mezclar una pequeña cantidad de jabón convencional y amoníaco, para hacer que el jabón tuviera una consistencia viscosa, lo patentó bajo el nombre de “Improved Liquid Soap” (Jabón líquido mejorado) el 22 de agosto.
En 1980, el emprendedor Robert R. Taylor, comenzó a vender jabón embotellado bajo un nuevo nombre de marca “Softsoap”, en su empresa The Minnetonka Corporation, ubicada en Chaska, Minnesota. Este producto incluía un dispensador para jabón, de esta manera fue como revolucionó la manera de lavarse las manos.
Fue tan grande el éxito que seis meses de venta de su jabón líquido, Taylor generó 25 millones de dólares en ganancias de Softsoap, para luego vender la marca a Colgate-Palmolive en 1987 Dineroenimagen.com..
Debido a esto, los limpiadores líquidos para manos en el mercado son en realidad surfactantes que los consumidores confunden con jabones líquidos. A esta clase pertenecen también los baños de burbujas, el champú líquido para el cuerpo, y los antibacteriales para manos, entre otros. En general, puede decirse que los jabones líquidos son jabones blandos disueltos en agua, alcohol, glicerina o mezcla de estas sustancias, adicionados o no con esencias que les den olor agradable.
Clasiifcación de los jabones líquidos
Entre estos jabones se puede diferenciar 3 tipos básicos: los jabones líquidos naturales, jabones líquidos semisintéticos y los sintéticos:
- Los jabones líquidos naturales
Basan su composición en mezclas de ácidos grasos de aceites vegetales, como coco y/o palma, a los que se les añade pequeñas cantidades de ácido oleico o ácidos grasos insaturados provenientes de aceites de girasol, soya, u otros. Estos últimos son ricos en glicéridos de ácido oleico. La mezcla se neutraliza generalmente con hidróxido de potasio. No se usa hidróxido de sodio ya que el álcali de potasio genera sales más solubles que las de sodio.
Los jabones líquidos naturales tienen el inconveniente de tener limitada solubilidad en aguas duras y un valor de pH muy alto (9-10) para mantenerse estables. El uso continuo de estos jabones ocasiona sequedad e irritación en la piel.
- Los jabones líquidos semisintéticos
Son mezclas de surfactantes con ácido oleico neutralizados con una amina orgánica como la monoetanolamina. El oleato de monoetanolamina (oleato de etanolamonio) es muy soluble en agua y da sensación de tersura en la piel.
- Los jabones líquidos sintéticos
Están basados en mezclas de surfactantes y agentes espumantes, la mayoría de ellos contienen ligeras fragancias y usualmente otros ingredientes para el cuidado de la piel. Son compatibles con todo tipo de agua y usualmente tienen excelentes propiedades limpiadoras y generan alta espuma aún en agua muy dura. Además dejan la piel tersa y libre de irritación dspace.ups.edu.ec
Función de los jabones líquidos
Una función importante del Jabón es la higiene personal, debido a que radica fundamentalmente para prevenir enfermedades, como puede ser el asentamiento de distintos parásitos y bacterias que además de dañar la piel, resultan contagiosas provocando infecciones respiratorias y estomacales; poniendo en riesgo la salud de otras personas con las que se tiene contacto, así que el lavado de manos es una de las actividades que debe realizarse con frecuencia a lo largo del día. Esta es la parte del cuerpo que se encuentra en contacto frecuente con elementos del exterior, desde el momento en el que se despierta hasta la hora de dormir, y de esta manera también se logra mantener la piel de las manos humectadas.
Actualmente, el jabón líquido es un producto cosmético usado en la higiene de manos y cuerpo de todos los grupos poblacionales, y son preparados con agentes tensoactivos, humectantes, viscosantes, etc., agentes que no generan resequedad en la piel, la espuma es menor y es más fácil evitar que existan residuos en la piel, manteniendo un mejor equilibrio de su pH. Las propiedades ideales del jabón líquido son: facilidad de aplicación siendo lo suficientemente viscoso para permanecer en las manos al aplicar; humectante para mantener la piel saludable y protegida de agresiones externas, enfermedades y envejecimiento.
La Densidad, su importancia en el jabón líquido
Es bueno indicar, que la densidad se trata de una relación que existe entre la masa y el volumen que es ocupado por una sustancia, y se expresa:
$$Densidad = \frac{masa}{volumen}$$.En relación al jabón líquido se debe señalar, que no poseen la misma densidad todos los jabones. Puesto que en algunos casos unos resultan más viscosos, o también más fluidos que otros. Siendo que esto va a afectar a la densidad de los mismos. Se tiene pues para la densidad del jabón líquido, un rango el cual es promedio ubicado entre los 1000 y los 1200 Kg/m3; pero, el jabón líquido cuenta con diversa densidad de acuerdo a su viscosidad, también se compara con la densidad de la miel, la cual igualmente es viscosa.
Sin embargo, su densidad varía en relación más bien a su humedad. Así es que su densidad se ubica en 1.402 gr/ml a unos 1.413 gr/ml. Estando en una temperatura ambiente. Con lo cual la densidad del jabón líquido muestra su diferencia en relación a esta comparativa con la miel.
Fabricando el jabón líquido
La idea de preparar jabón líquido para las manos surge de la necesidad de utilizar este producto para el cuidado y la desinfección de las manos. Cabe destacar que también son más respetuosos con el medio ambiente.
Los jabones líquidos en la actualidad poseen una lista de componentes que va mucho más allá de las grasas y las bases fuertes. Entre los componentes químicos se suelen utilizar en la fabricación de jabón líquido, tenemos:
- Benzoato de sodio y ácido benzóico
El jabón líquido requiere conservantes para evitar la aparición de moho, debido a que se encuentra disuelto en agua, e incluso, si no se encuentra disuelto en agua tiende a una degradación.
El benzoato de sodio es la sal sódica del ácido benzoico y es utilizado como conservante ya que posee propiedades fungicidas y de conservación, prolongando la vida útil del jabón líquido y evitando que los hongos y el moho aparezcan en el producto.
- Glicerina
Humectante que se obtiene de manera comercial, pura o tratada de un sub-producto de cualquier proceso industrial.
- Dodecil sulfato de sodio (SLS)
Sulfato de sodio lauretano (SLS) como también se le conoce, es un tensoactivo y un emulsionante que contribuye a la formación de espuma del jabón líquido. Además, es muy eficaz para eliminar restos de aceites y residuos.
- Metilisotiazolinona y metilclorotiazolinona
La metilisotiazolinona (MIT) y la metilclorotiazolinona (CMIT) son conservantes habituales en muchos jabones líquidos. Ambas sustancias químicas actúan individualmente para inhibir el crecimiento de las bacterias, pero lo más frecuente es que se combinen para un mejor efecto inhibidor de bacterias.
- Cocoamidopropil betaína
La cocoamidopropil betaína (CAPB) es un tensoactivo que ayuda a limpiar el agua de forma eficaz. También, actúa como agente espesante en muchos jabones líquidos, y posee algunas propiedades antisépticas, lo que lo convierte en una adición común en los productos de higiene personal.
- Fragancias
Muchos jabones líquidos contienen alguna fragancia o varias fragancias. Los ingredientes exactos varían de un fabricante a otro, actualmente, la ley no obliga a la industria de las fragancias a revelar los productos químicos específicos que utilizan en sus aromas.
- Ajustadores de pH
Los ajustadores de pH en el jabón líquido permiten equilibrar el pH del jabón para evitar que sean muy alcalinos, los ajustadores de pH más utilizados son el cloruro de sodio y el ácido cítrico.
- Colorantes
En los jabones líquidos, los colorantes dan al jabón un color atractivo. Al igual que las fragancias, los ingredientes exactos de los tintes sintéticos dependen del fabricante específico. A menudo, se derivan químicamente del petróleo y del alquitrán de hulla. El propósito de los tintes es puramente estético, hacen que el producto sea visualmente atractivo y tienen poco o ningún valor funcional Ingeniería Química. Proceso de fabricación de jabón líquido.
Algunas formulaciones para obtener el jabón líquido
El jabón es la combinación de un álcali, el cual puede variar entre hidróxido de sodio e hidróxido de potasio y un ácido, pudiendo ser un aceite vegetal o animal dando lugar a una reacción que se denomina saponificación, generando un producto que tiene como función principal limpiar o lavar por su acción detersiva.
Todos los jabones se originan por la reacción de un álcali y un ácido graso, que genera normalmente una pastilla de jabón sólido, pero por otro lado en los jabones líquidos la reacción se lleva a cabo con hidróxido de potasio el cual es mucho más soluble que el sodio y tiene menor posibilidad de formar cristales, permitiendo el paso de la luz a través del jabón.
Jabón Liquido para Manos
Para este jabón, sus componentes son suaves para la piel, sin causar irritación. Sus caracteristicas hacen del jabón un producto ideal cuando las manos se tienen que lavar continuamente.

PROCEDIMIENTO: En un recipiente plástico de 10 litros colocamos los 716 centímetros cúbicos de agua, al cual le agregamos los 3 gramos de Benzoato de Sodio los cuales medimos con la balanza gramera, procedemos a mezclar muy bien.
Luego se agregan los 5 gramos de Metil Celulosa, previamente medidos en la balanza, y se procede a mezclar continuamente por 5 minutos, preferiblemente con mezclador de madera.
A continuación, le agregamos los 3 centímetros cúbicos de Trietanolamina. (Este reactivo los podemos medir con la probeta de 10 centímetros cúbicos. y seguimos mezclando muy bien hasta que espese.
Luego agregamos el Detersin (191 centímetros cúbicos) previamente medidos con la probeta, y seguimos mezclando. Luego agregamos el Genapol (48 centímetros cúbicos), previamente medidos, continuar mezclando.
En un segundo recipiente (puede ser un Beaker) plástico graduado para líquidos de 250 centímetros cúbicos, ponemos un poquito de agua y mezclamos 2 centímetros cúbicos de Edta con 1 gramo de anilina, y se le adiciona a la mezcla principal y se mezcla todo muy bien.
Ahora se le adiciona a la mezcla principal los 5 centímetros cúbicos de fragancia, continúe mezclando, y empacamos con la ayuda del embudo.
Jabón Liquido para el cuerpo
PROCEDIMIENTO: En un recipiente plástico de 10 litros colocamos los 750 centímetros cúbicos de agua, a la que se le agrega los 2 gramos de Metil Parabeno Sódico el cual medimos con la gramera, proceda a revolver bien un mezclador preferiblemente de manera o vidrio. Luego le agregamos el Anfótero o Probetaina (50 centímetros cúbicos), el Genapol (150 centímetros cúbicos), el Nacarado (40 centímetros cúbicos), y la Glicerina (20 centímetros cúbicos).
Estos componentes requieren ser previamente medidos en una probeta de volumen adecuado, y mezclar muy bien cada uno de ellos.
En un segundo recipiente (Beaker) plástico graduado de 250 centímetros cúbicos, mezclar 2 centímetros cúbicos de EDTA con 1 gramo de anilina y esta mezcla se le adiciona al recipiente plástico grande mezclando muy bien. Luego se le agrega poco a poco el Coperlan (40 centímetros cúbicos) previamente medido, mezclando continuamente hasta que espese.
Luego agregamos los 10 centímetros cúbicos de fragancia al recipiente plástico grande homogenizando muy bien, para luego empacar en un frasco adecuado para jabón líquido con la ayuda del embudo.
Para producir este jabón, se requiere:

Recomendaciones
En la mezcla del jabón líquido para baño, la anilina y el EDTA se mezclan por aparte y luego se adicionan a la mezcla principal. Cuando se vaya a mezclar el Comperlan, se debe echar poquito a poquito, hasta encontrar el grosor ideal del champú, inicialmente se trabaja con 40 centímetros cúbicos, pero en ocasiones no son necesarios. Sí el champú le quedó muy grueso, se le echa 10 centímetros cúbicos de Propilen Glicol para adelgazarlo. El Anfótero o Probetaina es la que se encarga de producir la espuma.
Jabón líquido antibacterial para manos y cuerpo
Para producir este jabón, se requiere:

PREPARACIÓN: En un recipiente plástico, agregamos el agua y disolvemos el Texapón en el agua hasta que éste desaparezca.
Una vez logrado esto, se agrega en orden los otros ingredientes y se mezcla suavemente hasta que los productos queden bien homogenizados. Luego envasar en un recipiente apropiado para el jabón.
Recomendaciones
Si se quiere un jabón un poco más viscoso se debe agregar Cloruro de Sodio (sal) en pequeñas cantidades hasta obtener el resultado esperado.
Muy importante
El Ph se debe ajustar de 6 a 8 con ácido cítrico o con TEA (Trietenolamina), utilizar peachímetro para su lectura.
Jabón líquido para lavar la loza 1
PREPARACIÓN: Primero diluir la sal (cloruro de sodio) completamente en el agua más o menos 2 minutos, mezclar el lauril éter, muy bien.
Adicionar la betaína mezclando para homogenizar muy bien, seguidamente agregar la glicerina sin dejar de mezclar hasta que todo esté muy bien incorporado, luego agregar el aroma, el color continuando con la mezcla hasta que esté muy homogenizado, luego, chequear su pH que ha de estar en 6 a 6.5, ya que el cuerpo tiene un pH aproximado de 5.5 a 6. Para producir este jabón, se requiere:

- Jabón líquido para lavar la loza 2
PROCEDIMIENTO: Integrar el EDTA al agua mezclando para homogenizar muy bien, ir adicionando el agua poco a poco, hasta que al final ya tengas 10 litros de jabón.
Luego adicionar la soda cáustica al 50%, seguidamente agregar el tripolifosfato, sin dejar de mezclar, tenga en cuenta que cuando agregó la soda la solución aumenta su temperatura, ya que es una reacción exotérmica.
Ahora mezcle los 500 ml de ácido sulfónico, seguidamente poner la betaina y cocoamida, el óxido de amina como espumante, chequear el pH posiblemente estará entre 10 u 11, preferiblemente con ácido cítrico, hasta obtener un pH de 8, poner la sal un promedio de 100 a 200 gramos
Para producir este jabón, se requiere:

Fichas técnicas de reactivos
En este apartado, se hace referencia a los usos que se le ha de dar al producto dentro de una formulación, es decir, para qué sirve el producto y en dónde se debe usar.
Si es producto tuviera restricciones, se debe referir dónde no debe ser usado.
Se enumeran algunos productos (reactivos) que se utilizan en las distintas formulaciones, bien sea, para jabones, deetergentes, shampoos, desengrasantes u otras formulaciones..
- TEXAPÓN N-70
(Este es el nombre actualizado y comercial, su nombre científico (Laurilsulfato de Amonio). Es el que brinda la espumosidad al jabón y shampoo. Es un líquido viscoso de ligero color amarillo. Fórmula semidesarrollada es $C_{12}H_{29}NO_4S$. Su Punto de inflamabilidad, conocido como la temperatura más baja en la que puede formarse una mezcla inflamable en contacto con el aire es > 93 ºC, su densidad 0,998, su masa molecular UMA Unidad de Masa Atómica, 283,43 g/mol. Punto de ebullición, que corresponde a la temperatura que debe alcanzar una sustancia para pasar del estado líquido al estado gaseoso es > 100 ºC.
- COMPERLAND KD
(Los nombres comerciales de este producto son: Cocoamida, Genamid). Es un espesante para formulaciones de detergentes líquidos con tensioactivos del grupo de los éter-sulfatos, que además engrasa suavemente la piel ya a concentraciones bajas.
Su gran compatibilidad con la piel hace que sea un constituyente importante en champús y otros cosméticos. Aunque no es realmente soluble en agua es dispersable, y se puede incorporar en frío o bien calentando muy ligeramente. generalmente se utiliza en concentraciones de 1 a 55 para aumentar viscosidad y de 1 a 10% ara estabilizar la espuma en champús y detergentes.
- METIL PARABENO PURO
(Su nombre comercial propil parabeno puro, su nombre científico Metil Puro). Este producto hace que el shampoo se preserve por más tiempo.
- METIL PARABENO SÓDICO
También recibe el nombre de NIPAGÍN, Preservante de preparados farmacéuticos en concentraciones desde 0.05 % hasta 0.25 %. También, se utiliza en la conservación de cosméticos que contienen grasas y aceites vegetales y animales, jabones y shampoo. Preservante en alimentos, bebidas y productos cárnicos a una dosificación de 0.1 % máximo.
FORMA DE APLICACIÓN: Suele disolverse en agua caliente y luego incorporarse en el preparado, pero si la fórmula no contiene agua se puede disolver en alcohol, glicerina y aceites o grasas fundidas.
- CLORURO DE SODIO
Conocido normalmente como sal común o sal de mesa, su fórmula química es Fórmula química: NaCl. Este producto le brinda el 70% de espesor al shampoo. Es un compuesto iónico formado por un catión sodio (Na+) y un anión cloruro (Cl-); Es Incoloro; aunque parece blanco si son cristales finos o pulverizados. Su densidad es de 2160 kg/m³; 2,16 g/cm³; su masa molar es de 58,443 g/mol; el punto de fusión es 1074 K (801 °C)
- ÁCIDO CÍTRICO
También conocido con los sinónimos: Ácido 2-hidroxi-1,2,3-propanotricarboxilico; Ácido beta-hidroxitricarballílico; Aciletten; Ácido cítrico anhidro; Citralite; Citretten; Citro; Hydrocerol A; Ácido 2-hidroxipropanotricarboxílico; Ácido 2-hidroxitricarballílico; Ácido betahidroxi-tricarboxílico. Fórmula química: C6-H8-O6; Peso molecular: 192.14.
Su punto de fusión es de 153 ºC. Su densidad específica es igual a 1.665 g/cm3 a 20 ºC. Su solubilidad en agua es de 3.83 * 105 mg/L a 25 ºC (59.2% a 20 ºC). Es muy soluble en etanol, soluble en éter y acetato de etilo e insoluble en benceno y cloroformo. Su presión de vapor es igual a 1.7 X 10-8 mm de Hg a 25 ºC (valor estimado). Su constante de la ley de Henry es igual a 4.3 X 10-14 atm m3/mol a 25 ºC (valor estimado). En solución 0.1 N presenta un pH de 2.2. Puede ser extraído de frutos cítricos y desechos de piña, o puede ser producido industrialmente por fermentación de melaza.
Este producto es el que regula el Ph o el grado del shampoo y el jabón líquido.
- ÁCIDO BÓRICO
Polvo blanco que se origina del boro; tal como indica su propio nombre. La disolución o mezcla con agua es la que hace posible la utilidad de este mineral en la agricultura, la cosmética. Su fórmula química $H_3BO_3$, su masa molar: 61,83 g/mol; densidad: 1,44 g/cm³; PH: 5,1; soluble en: agua, alcohol; denominación de la IUPAC: Boric acid, Trihydrooxidoboron.
Como nota curiosa, Es un excelente retardante de fuego, de modo que puede ser muy útil para contrarrestar fuego de gran envergadura. Es utilizado por los profesionales en caso de fuegos difíciles de apagar.
- ZINC PIRINITIONE
Su nombre comercial piritionato de zinc. Este producto es el que ayuda a controlar la caspa en el cuero cabelludo obviamente anexado al shampoo. este porducto está diseñado para despegar las células de piel muerta y que resulte más fácil eliminarlas con el lavado.
- TENSOACTIVO ANIÓNICO
Conocido también en el mercado como tensoactivo anfotero. Este producto es el que le brinda el brillo al cabello.
Debido a su poder espumoso, los tensioactivos aniónicos conforman unos detergentes muy eficaces, sobre todo en aguas duras con alto contenido en carbonatos. Se utilizan sobre todo en detergentes para ropa y en productos de limpieza, ya que además de disolver grasas son capaces de desnaturalizar proteínas y romperlas para promover su disolución y aumentar el poder de limpieza.
- EMOLIENTE NATURAL
Comercialmente conocido como plantaren y su nombre científico Elastina. Actúa como acondicionador y a la vez es reconstituyente en la raíz del cuero cabelludo.
Es un líquido viscoso opaco, amarillo pálido. Además, es un tensioactivo alquil poliglucósido de carácter no iónico, compatible con otros tensoactivos.
Puede ser utilizado en la fabricación de limpiadores faciales, geles de ducha, jabón líquido para manos, shampoo para cabello, baño de burbujas, jabones para cuidado de piel sensible.
- GENAMIN ACONDICIONANTE
Su nombre científico Cetilrimetilamonioluoumro, se utiliza para la elaboración de shampoo dos en uno Fichas técnicas de productos químicos..
- TEXAPON N70
También conocido con el nombre de Lauril éter sulfato de sodio AL 70%. es una pasta fluida ligeramente amarilla, es una materia prima detergente aniónica de alta concentración para la industria cosmética, se puede diluir sin problemas con los mezcladores adecuados.
Texapon N70 es un lauril éter-sulfato de sodio que no contieneauxiliares disolventes como alcohol u otros. Este producto, tiene buena capacidad para formar espuma y facilidad para elevar la viscosidad con cloruro de sodio.
Es compatible con otros tensoactivos aniónicos y no iónicos, no se ve afectado por la dureza del agua y aún a bajas temperaturas presenta unaespuma fina y abundante. Entre sus principales propiedades están:
- Buen efecto espumante
- Buen poder humectante
- Resistencia a aguas duras
- Excelente poder detergente
- Propiedades humectantes y emulsificantes
- Compatibilidad con la piel
- Formulación de productos cristalinos
Se utiliza generalmente para la elaboración de detergentes domésticos, jabón liquido, agentes especiales de limpieza, limpiadores multiusos, limpiadores desinfectantes, jabón líquido para coches, jabón para alfombras, así como detergentes industriales.
A este producto, se le agrega que es totalmente soluble en agua, puede emplearse en procesos en frío, cuidando el tipo de agitación para evitar la formación excesiva de espuma. También debe considerarse que por de carácter aniónico es incompatible con los tensoactivos catiónicos convencionales, sinembargo, no presenta problemas con productos catiónicos especialmente diseñados para ser usados con tensoactivos aniónicos TEXAPON N 70. Hoja Técnica..
- COCOAMIDA
La Cocoamida también se conoce con el nombre de propil betaína o (CAPB) es un ácido graso derivado del aceite de coco, físicamente es un líquido viscoso de color claro a ligeramente amarillo. es el mismo comperland.
Las betaínas se clasifican como sustancias tensoactivas anfóteras, se consideran suaves para la piel. Tienen propiedades como agente espumante, humectante, emulsionante y desengrasante, en conjunto con tensoactivos aniónicos, la detergencia mejora en condiciones alcalinas.
- DODIGEN 226
También es conocido en el mercado como cloruro de bensalcinio al 50%, es un agente desinfectante a base de sales de amonio cuaternario, diseñado para el control de bacterias algas, hongos, virus como moquillo, viruela, hepatitis, etc. Obviamente anexado en los desinfectantes de alta concentración para pisos. Es muy comercial el desinfectante con este producto en hospitales y centros institucionales.
- TRIETALONAMIDA
Conocido en el mercado como TEA, utilizado en la fabricación de productos cosméticos, tales como cremas, es cristalizante en el Gel, etc. Soluble en agua, alcohol, acetona y cloroformo.
- TRICLOSAN
(5-cloro-2-(2,4-diclorofenoxi)fenol), recibe el nombre de irgazán, es un potente agente antibacteriano y fungicida.
- SODA CÁUSTICA O SOSA
Su nombre científico NAOH, Hidróxido de sodio, cuando está puro es un sólido cristalino incoloro que funde a 318 grados Celsius (604,4 °F) sin descomponerse, y con un punto de ebullición de 1388 grados Celsius (2530,4 °F) 30. Es altamente soluble en agua, con una menor solubilidad en disolventes polares como etanol y metanol.se utiliza en escama en la fabricación del cloro, jabón de lavar, detergentes, etc. Producto de alto riesgo, manejarlo con cuidado.

BIBLIOGRAFÍA
BIBLIOGRAFÍA
Aquí se presenta la bibliografía básica donde se puede profundizar sobre los conceptos utilizados para describir todos los procesos y recomendaciones que se han presentado a través del texto.
Además, se presentan los créditos para los autores de las imagénes libres de uso.

- Álvarez de Gutiérrez, Marietta. (2000). Taller de Química 1. Colombia. Fondo Educativo Panamericano.
- Atkins, P.& Jones L.(2006).Principios de Química (Los caminos del descubrimiento). Ed. Médica Panamericana, Buenos Aires.
- Bermejo, F..(1995).Problemas de Química General. Paraninfo.
- Brown, T. L., Lemary, Jr. H. E. & Bursten, B. E.(1993).Química: la ciencia central (5a ed.). México: Prentice Hall Hispanoamericana.
- Burns, R. A. (1996).Fundamentos de Química (2a ed.). México: Prentice Hall Hispanoamericana.
- Bruño, G.M (1926).Curso de química con práctica de laboratorio.(2a ed.). París: Procuraduría General.
- Chang, R.Principios Esenciales de Química General.(4a ed.).
- Chang, R., y Collegue, W. (2002).Química (7a ed.). Colombia: McGarw-Hill.
- Daub, G. W., y Seese, W. S. (1996).Química (7a ed.). México: Prentice Hall Hispanoamericana.
- FisquiWeb. (s.f). Cálculos Estequiométricos. Obtenido de https://fisquiweb.es
- FORO QUIMICA Y SOCIEDAD. (2019). Año Internacional de la Tabla Periódica de los Elementos Químicos. Obtenido de https://www.quimicaysociedad.org/
- Hernández, Sandra A. (2020). Cuadernillo de de nivelación de química. Bahía Blanca, Argentina: Universidad Nacional del Sur. Obtenido de http://www.quimica.uns.edu.ar/
- JEAN B. UMLAND; JON M. BELLAMA.(2000) Química General, International Thomson Editores. Mexico.
- Mahan, B.M.; Myers, R.J. (1990).Química.Un Curso Interuniversitario. México: Addison-Wesley Iberoamericana.
- Masterton, W. L. Hurley C. N. (2003).Química Principios y Reacciones.(4a ed.).Thomson Ed.
- Nomenclatura química de los compuestos inorgánicos 1. http://iesfgl.es/: nomenclatura-en-la-quimica-inorganica .
- Núñez González, C. (s.f.). Libro de texto ciencias. Química. En C. Núñez González, Química (págs. 1 - 180). Instituto Profesional Providencia. Obtenido de https://upload.wikimedia.org/
- Patiño Jaramillo, Margarita.(2008).Química básica prácticas de laboratorio (1a ed.).Medellín: Fondo editorial ITM.
- Patiño Jaramillo, Margarita. Valdés Romaña, Nilkar.(2010).Química básica prácticas de laboratorio (2a ed.).Medellín: Instituto Tecnológico Metropolitano.
- Petruci, R. H., Harwood, W. S., & Herring, F. G. (2003).Química General (8a ed.).Madrid: Pearson Educación.
- Price, J., Smoot, R. C. y Smith, R. G. (1998).Química: un curso moderno.Columbus, Ohio: Merril Publishing Co.
Créditos de imágenes
Nota: se hace mención a PNGTREE, productores de imágenes en formato png, a quien se ha comprado la licencia para el uso de las imágenes que hacen honor a la tierra y en general al medio ambiente.
Al inicio de los capitulos tenemos las siguientes referencias:
- Página 16-17
- Página 49-50
Imagen de Matteo Orlandi en Pixabay
- Página 71-72
Imagen de Beverly Buckley en Pixabay
- Página 125-126
Imagen de Alexas_Fotos en Pixabay
- Página 149-150
Imagen de Andreas Hoja from Pixabay


