2. Un espectro de emisión está compuesto por las radiaciones electromagnéticas que emite directamente un cuerpo al excitar sus átomos, por ejemplo mediante una llama, un arco eléctrico, una chispa, etc. Un espectro de absorción es el constituido por las radiaciones que absorbe un cuerpo o sustancia, que puede encontrarse en estado sólido, líquido o gaseoso, aunque se recurre muy frecuentemente a su estudio en disolución. Un ejemplo sería el espectro de luz procedente de una fuente de luz continua tras atravesar un gas.
3. Es la descomposición en radiaciones simples del conjunto de radiaciones emitidas (espectro de emisión) o absorbidas (espectro de absorción) por un cuerpo.
4. Las radiaciones que componen el espectro de emisión y el de absorción de un elemento son características de dicho elemento y pueden servir para identificarlo.
5. Según Bohr: - Los electrones giran en torno al núcleo en órbitas circulares de energía fija. - En éstas órbitas los electrones se mueven sin perder energía. - Sólo están permitidas determinadas órbitas: aquellas cuya energía tome ciertos valores restringidos.
6. Las órbitas permitidas se pueden denominar también niveles de energía o capas.
7. Cuando un electrón absorbe energía electromagnética, pasa a un nivel de energía mayor.
8. Cuando un electrón cae a un nivel de energía inferior, emite energía electromagnética.
9. Sí, puesto que, de la misma forma que el habitante sólo puede vivir en uno de los pisos del edificio, los electrones sólo pueden estar en algunas de las órbitas de energía restringida posibles. Si el habitante se traslada a un piso superior, aumenta su energía potencial. De un modo similar, si el electrón pasa a una órbita más alta, su energía se incrementa en una cantidad determinada.
10. El espectro de absorción se origina cuando un electrón absorbe la energía de un fotón y asciende desde su nivel a otro de mayor energía.
11. Los espectros de emisión se deben a las radiaciones que emite un electrón excitado en un nivel alto al descender a otro nivel de energía inferior.
12. Es una trayectoria definida del electrón. Fue propuesta, con diversas variantes, por Rutherford, Bohr, Sommerfeld y otros investigadores, para explicar el movimiento de los electrones en el átomo.
13. Es una función de onda que describe, en términos de probabilidad, la posición del electrón de una determinada energía. Por extensión, se asigna también este nombre a la zona del espacio en la que existe una probabilidad elevada (99 %) de encontrar el electrón.
14.
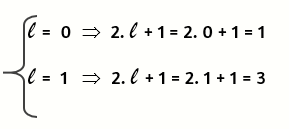
Para n = 2 los valores de ℓ son: en total habrá 1 + 3 = 4 orbitales En total habrá 1 + 3 = 4 orbitales
15.
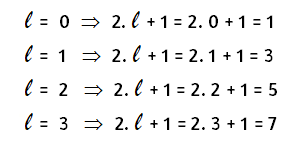
Para n = 4 se tiene que en total habrá: 1 + 3 + 5 + 7 = 16 orbitales
16.
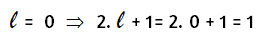
Para n = 3 se tiene: En total habrá 1 orbital. Según el principio de exclusión de Pauli en cada orbital sólo caben, como mucho, dos electrones. Por tanto el número máximo de electrones será: 1 · 2 = 2 electrones
17.
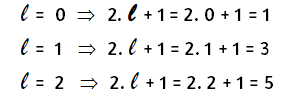
Para n = 3 se tiene:En total habrá 1 + 3 + 5 = 9 orbitales. Según el principio de exclusión de Pauli en cada orbital sólo caben, como mucho, dos electrones. Por tanto el número máximo de electrones será: 9 · 2 = 18 electrones
18. Los orbitales 3px, 3py, y 3pz tienen el mismo número cuántico principal, n = 3, por lo que tienen el mismo tamaño. Por otro lado, también coinciden en su número cuántico secundario ( ℓ = 1, => orbitales p) por lo que coinciden también en su forma. La única diferencia estriba en su orientación; cada uno, según un eje de coordenadas.
19. Los orbitales 2s, 3s, y 4s coinciden en su número cuántico secundario (ℓ = 0 => orbitales s), por lo que tienen la misma forma (esférica, y por tanto, la misma orientación). Se diferencian en el tamaño, pues el número cuántico que indica esta propiedad, n, es distinto para cada uno de los orbitales.
20. En primer lugar, es preciso considerar el número de electrones de que disponemos en cada caso; al ser todos átomos neutros, el número de electrones es el mismo que el número de protones, es decir, Z. Así entonces, el orden de llenado es en orden creciente de números (n+ ℓ), y para valores iguales de éstos, se llena antes el de menor número n.

21. En primer lugar, es preciso considerar el número de electrones de que disponemos en cada caso.
El ion K+ tiene carga +1, por lo que tiene un electrón menos que protones, es decir, 18.
El ion Mg+2 tiene carga +2, por lo que tiene dos electrones menos que protones, es decir, 10.
El ion Fe+3 tiene carga +3, por lo que tiene tres electrones menos que protones, es decir, 23.
El ion Pd+4 tiene carga +4, por lo que tiene cuatro electrones menos que protones, es decir, 42.
El orden de llenado es en orden creciente de números (n+l), y para valores iguales de éstos, se llena antes el de menor número n.
Teniendo en cuenta todo lo anterior, podemos escribir las configuraciones siguientes:

22. a) Esta configuración incluye 4 electrones, por lo que el átomo neutro será el que tiene 4 protones, es decir , el que tenga número atómico Z = 4, que corresponde al berilio (Be).
b) Esta configuración incluye 8 electrones, por lo que el átomo neutro será el que tiene 8 protones, es decir, el que tenga número atómico Z = 8, que corresponde al oxígeno (O).
c) Esta configuración incluye 11 electrones, por lo que el átomo neutro será el que tiene 11 protones, es decir, el que tenga número atómico Z = 11, que corresponde al sodio (Na).
d) Esta configuración incluye 18 electrones, por lo que el átomo neutro será el que tiene 18 protones, es decir, el que tenga número atómico Z = 18, que corresponde al argón (Ar).
23. El cesio es un elemento perteneciente al grupo 1 y periodo 6 del sistema periódico. Le corresponde una estructura electrónica abreviada [Xe] 6s1. De acuerdo con ella, los valores que pueden tomar los números cuánticos de su electrón más externo son:
n = 6 (se encuentra en el 6º periodo o nivel de enegía)
ℓ = 0 (se trata del subnivel s)
m = 0 (se trata de un orbital s)
s = ± 1/2 (según cuál sea el spín del electrón)
24. De acuerdo con los valores que pueden tomar los números cuánticos de un electrón: n = 1, 2, 3, …
ℓ = 0, 1, 2, …, (n – 1)
m = -ℓ,…, 0, …, +ℓ
s = ± 1/2
a) Prohibido. El número cuántico n no puede ser 0.
b) Prohibido. Si n = 1, el valor de ℓ sólo puede ser 0.
c) Permitido. Todos los números cuánticos tienen los valores adecuados.
25. a) Falso. La energía del electrón del átomo de hidrógeno sólo puede valor 0 cuando éste se encuentra a una distancia infinita del núcleo, es decir, fuera de dicho átomo.
b) Falso. Los electrones se encuentran en orbitales, regiones del espacio con cierta energía donde existe una elevada probabilidad de encontrar un electrón. Dicha posición no puede determinarse con exactitud.
c) Verdadero. Los electrones se encuentran en orbitales, regiones del espacio con cierta energía donde existe una elevada probabilidad de encontrar un electrón.
26. Los orbitales d se caracterizan por que el número cuántico secundario, ℓ = 2. Los valores que puede tomar el número cuántico secundario son 0, 1, 2, …, (n – 1). De parejas de valores propuestos la única que corresponde al un orbital d es (3, 2). La respuesta correcta es la d.
27.acuerdo con los conceptos de: - Número atómico: indica el número de protones o de electrones de un átomo neutro. - Número másico: indica el número de protones + neutrones de un átomo. El cloro es un elemento que pertenece al grupo 17 y periodo 3 del sistema periódico por lo que su estructura electrónica es 1s2 2s2 2p6 3s2 3p5. Sumando los superíndices se observa que tiene 17 electrones y por tanto, 17 protones y (35 – 17) = 18 neutrones. Como la especie 35Cl−, anión cloruro, está cargada negativamente, significa que tiene un electrón de más en su última capa, es decir, 18 electrones. La respuesta correcta es la e.
28. Los números cuánticos de un electrón en un orbital 3p son:
n = 3 (se trata del 3er nivel de energía)
ℓ = 1 (se trata de un subnivel p)
mℓ = -1, 0, 1
s = 1/2 o -1/2
29. L Si el número cuántico n = 2 indica que se trata del segundo nivel de energía.
Si el número cuántico ℓ = 1 indica que se trata de un subnivel de energía p.
Si el número cuántico ℓ = 1, los valores posibles del número cuántico magnético m, son 0, 1 y -1, lo que indica que el subnivel de energía p se encuentra triplemente degenerado o lo que es lo mismo que en este subnivel hay 3 orbitales 2p.
Como el número cuántico s sólo puede tener los valores 1/2 y -1/2, quiere decir que en cada orbital caben dos electrones con espines opuestos. Por tanto, el número total de electrones que caben en el subnivel 2p es 6.
La respuesta correcta es la b
30. 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 4f14 5d4 6s2.
31. Cierto
En el átomo de hidrógeno la energía del electrón viene dada por la expresión En = -K/n2, dependiendo únicamente del número cuántico principal n. Los orbitales (o las órbitas en el modelo de Bohr) con el mismo valor del número cuántico n pero diferente valor del número cuántico l, presentan la misma energía y constituyen un único nivel de energía degenerado.
32. Cierto
En un átomo polielectrónico la energía de un electrón depende tanto del número cuántico n como del l, rompiéndose la degeneración que se presenta en el átomo de hidrógeno. Aquí un nivel de energía, caracterizado por n, se subdivide en tantos subniveles como valores toma l.
33.Cierto
34. c. 4d
35. 9
El número de orbitales atómicos para un cierto valor de n es siempre n2.
36.8
Este valor siempre es 2n2. Si n2 es el número de orbitales posibles y en cada orbital caben un máximo de dos electrones (principio de exclusión de Pauli), entonces el máximo de electrones para un cierto valor de n es 2n2.
37. a) 4s
b) 1s2 2s2 2p6 3s2 3p6 4s1
Para el potasio, el orbital 4s tiene menor energia que los 3d, y por tanto el electrón número 19 se situa en el orbital 4s. Después de llenarse el orbital 4s se llenan los orbitales 3d, y entonces tenemos los metales de transición.
38- a
39. c
40. a