| Como hemos visto en la anterior experiencia simulada, manteniendo constantes el nº de partículas del gas y la temperatura, la presión P depende inversamente de V, es decir: Si el volumen se hace el doble, la presión se hace la mitad, si se hace el triple, la presión se hace la tercera parte... Esto se expresa, como Ley de Boyle. En general será:
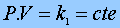
"A temperatura constante, para una determinada cantidad de gas, el producto presión por volumen permanece constante". |
La ley de Boyle, también podemos expresarla así:
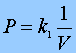
En nuestra experiencia concreta, la constante resulta ser 4,0 , por lo que la ley de Boyle en este caso concreto será : P.V = 4,0 . A otra temperatura la constante tendrá otro valor.
|
Observar la gráfica correspondiente a esta ley para el caso P.V =5.4.
Con las leyes podemos hacer predicciones.
|









